Souhrnné informace o léku - YAZ 0,02 MG/3 MG POTAHOVANÉ TABLETY
1. NÁZEV PŘÍPRAVKU
YAZ 0,02 mg/3 mg potahované tablety
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
24 světle růžových potahovaných tablet:
Jedna potahovaná tableta obsahuje ethinylestradiolum 0,020 mg (ve formě betadexum clathratum) a drospirenonum 3 mg.
Pomocná látka se známým účinkem: laktosa 46 mg
4 bílé placebo (neúčinné) potahované tablety: Tablety neobsahují léčivé látky.
Pomocná látka se známým účinkem: laktosa 22 mg
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Potahované tablety
Tablety s léčivými látkami (účinné) jsou světle růžové, kulaté a bikonvexní; na jedné straně mají vyražena písmena „DS“ uvnitř pravidelného šestiúhelníku.
Tablety placeba jsou bílé, kulaté a bikonvexní; na jedné straně mají vyražena písmena „DP“ uvnitř pravidelného šestiúhelníku.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Perorální kontracepce.
Rozhodnutí předepsat přípravek YAZ by mělo být provedeno po zvážení jednotlivých současných rizikových faktorů ženy, zvláště rizikových faktorů pro žilní tromboembolismus (VTE), a toho, jaké je riziko VTE u přípravku YAZ v porovnání s dalšími přípravky CHC (viz body 4.3 a 4.4).
4.2 Dávkování a způsob podání
Způsob podání: perorální podání
Dávkování
Jak se přípravek YAZ užívá
Tablety se musí užívat každý den přibližně ve stejnou dobu, v pořadí vyznačeném na blistru. Zapíjejí se podle potřeby tekutinou. Tablety se užívají kontinuálně. Užívá se jedna tableta denně po 28 po sobě jdoucích dní. Nový blistr se užívá následující den po užití poslední tablety z předchozího. Krvácení z vysazení začíná obvykle 2. – 3. den užívání placebo tablet (poslední řádka) a nemusí být ukončeno v době zahájení užívání z dalšího blistru.
- Nepředcházelo-li užívání hormonální kontracepce (v předchozím měsíci)
- Přechod z kombinované hormonální kontracepce (kombinovaného perorálního kontraceptiva (COC), vaginálního kroužku nebo transdermální náplasti)
- Přechod z kontracepční metody obsahující pouze progestagen (pilulka obsahující pouze progestagen, injekce, implantát) nebo z nitroděložního systému uvolňujícího progestagen (IUS)
- Užívání po potratu v prvním trimestru
- Užívání po porodu nebo po potratu ve druhém trimestru
Vynechání placebové tablety z poslední (4.) řádky blistru není třeba věnovat zvláštní pozornost. Je však třeba je zlikvidovat, aby nedošlo k neúmyslnému prodloužení placebové fáze. Následující pokyn platí pouze pro vynechané účinné tablety:
Pokud se užití tablety opozdí o méně než 24 hodin, není kontracepční ochrana narušena. Žena musí užít tabletu okamžitě, jakmile si chybu uvědomí a další tabletu pak užije v obvyklou dobu.
Je-li užití tablety opožděno o více než 24 hodin, kontracepční ochrana může být snížena. Další opatření se pak mohou řídit následujícími dvěma základními pravidly:
-
1. Doporučená délka intervalu užívání placebo tablet je 4 dny, užívání tablet nesmí být nikdy přerušeno na dobu delší než 7 dní
-
2. K dosažení dostatečné suprese hypothalamo – hypofyzo – ovariální osy je nutné brát tablety nepřerušeně 7 dní po sobě.
-
V souladu s těmito pravidly lze v běžné praxi poskytnout následující doporučení:
den 1–7
Žena musí užít poslední vynechanou tabletu okamžitě, jakmile si chybu uvědomí, i kdyby to znamenalo užití 2 tablet současně. Poté pokračuje v užívání tablet v obvyklou dobu. Navíc je třeba používat v následujících 7 dnech bariérovou metodu kontracepce jako např. kondom. Pokud během předchozích 7 dní došlo ke styku, je třeba zvážit možnost otěhotnění. Čím více tablet bylo vynecháno a čím blíže byly tyto tablety k placebové fázi, tím vyšší je riziko otěhotnění.
- den 8–14
Žena musí užít poslední vynechanou tabletu okamžitě, jakmile si chybu uvědomí, i kdyby to znamenalo užití 2 tablet současně. Poté pokračuje v užívání tablet v obvyklou dobu. Pokud byly během 7 dní předcházejících opomenutí tablety užívány správně, není nutno podnikat další kontracepční opatření. Pokud došlo k opomenutí více než 1 tablety, doporučuje se použití další kontracepční metody, a to po dobu 7 dní.
- den 15–24
Riziko selhání kontracepce je bezprostřední vzhledem k blížícímu se období placeba. Přesto však upravením schématu užívání lze předejít snížení kontracepční ochrany. Bude-li se žena řídit některým z následujících dvou možných postupů, není třeba používat další kontracepční opatření za předpokladu, že po dobu 7 dnů předcházejících vynechání první tablety užila všechny tablety správně. Pokud nikoli, má žena použít první ze dvou uvedených metod a zároveň použití další kontracepční metodu, a to následujících 7 dní.
-
1. Žena musí užít poslední vynechanou tabletu okamžitě, jakmile si chybu uvědomí, i kdyby to znamenalo užití 2 tablet současně. Poté pokračuje v užívání tablet v obvyklou dobu, dokud nejsou vyčerpány účinné tablety. 4 placebové tablety z poslední řádky je nutno vyřadit. Poté začne okamžitě užívat následující blistr. Krvácení z vysazení se pravděpodobně dostaví až po využívání účinných tablet z druhého blistru, ale během užívání tablet může dojít ke špinění nebo krvácení z průniku.
-
2. Ženě lze také doporučit, aby přerušila užívání účinných tablet ze současného blistru. Má užívat placebo tablety z poslední řádky až po 4 dny – včetně dnů, kdy byly tablety vynechány, a poté začne užívat další blistr.
Pokud žena zapomněla užít několik tablet a během placebové fáze nedojde ke krvácení, mohlo dojít k otěhotnění.
-
V případě závažných gastrointestinálních poruch (tj. zvracení nebo průjmu) nemusí dojít k úplnému vstřebání a je třeba dalších kontracepčních opatření. Dojde-li ke zvracení během 3 – 4 hodin po užití účinné tablety, je třeba co nejdříve užít novou (náhradní) tabletu. Novou tabletu je třeba, pokud možno, užít do 24 hodin od obvyklého času. Pokud uplynulo více než 24 hodin, lze aplikovat postup při vynechání tablety uvedený v bodě 4.2 „Postup při vynechání tablet“. Pokud žena nechce změnit obvyklý způsob užívání tablet, musí si vzít potřebné tablety navíc z dalšího blistru.
Přeje-li si žena oddálit periodu, musí pokračovat v užívání tablet z dalšího blistru přípravku YAZ bez obvyklé fáze užívání placebo tablet. Tak lze pokračovat podle přání až do využívání účinných tablet z druhého blistru. Během tohoto prodloužení může dojít ke špinění či krvácení z průniku. Pravidelné užívání přípravku se pak obnoví po placebové fázi.
Potřebuje-li žena posunout periodu na jiné dny v týdnu, než na který vychází ve stávajícím schématu užívání, může zkrátit nejbližší placebové období o tolik dní, kolik je potřeba. Čím kratší bude interval, tím větší je riziko, že neproběhne pravidelné krvácení a může dojít ke špinění či krvácení z průniku během užívání druhého blistru (podobně jako při oddálení periody).
4.3 Kontraindikace
Kombinovaná hormonální antikoncepce (CHC) by se neměla používat u následujících stavů. Pokud se některý z těchto stavů objeví poprvé v průběhu užívání CHC, užívání přípravku je třeba okamžitě ukončit.
- Přítomnost nebo riziko žilního tromboembolismu (VTE)
o žilní tromboembolismus – současný žilní tromboembolismus (léčený pomocí antikoagulancií) nebo anamnéza VTE (např. hluboká žilní trombóza [DVT] nebo plicní embolie [PE])
o známá dědičná nebo získaná predispozice pro žilní tromboembolismus, jako je rezistence na APC (včetně faktoru V Leiden), deficit antitrombinu III, deficit proteinu C, deficit proteinu S
o velký chirurgický zákrok s déletrvající imobilizací (viz bod 4.4)
o vysoké riziko žilního tromboembolismu v důsledku přítomnosti více rizikových faktorů (viz bod 4.4);
- Přítomnost nebo riziko arteriálního tromboembolismu (ATE)
o arteriální tromboembolismus – současný arteriální tromboembolismus, anamnéza arteriálního tromboembolismu (např. infarkt myokardu) nebo prodromální stav (např. angina pectoris);
o cerebrovaskulární onemocnění – současná cévní mozková příhoda, anamnéza cévní mozkové příhody nebo prodromálního stavu (např. tranzitorní ischemická ataka, TIA);
o známá hereditární nebo získaná predispozice k arteriálnímu tromboembolismu, jako je hyperhomocysteinémie a antifosfolipidové protilátky (antikardiolipinové protilátky, lupus antikoagulans);
o anamnéza migrény s fokálními neurologickými příznaky;
o vysoké riziko arteriálního tromboembolismu v důsledku vícečetných rizikových faktorů (viz bod 4.4) nebo přítomnosti jednoho závažného rizikového faktoru, jako je:
- diabetes mellitus s cévními příznaky;
- závažná hypertenze;
- závažná dyslipoproteinémie.
- Závažné jaterní onemocnění stávající nebo v anamnéze až do navrácení hodnot jaterních funkcí k normálu.
- Závažná renální insuficience nebo akutní renální selhání.
- Existující jaterní tumory nebo jejich výskyt v anamnéze (benigní či maligní).
- Přítomnost pohlavními steroidy ovlivnitelných malignit (tj. pohlavních orgánů nebo prsů) nebo podezření na ně.
- Vaginální krvácení s nediagnostikovanou příčinou.
- Hypersenzitivita na léčivé látky nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Přípravek YAZ je kontraindikovaný při současném užívání léčivých přípravků obsahujících ombitasvir/paritaprevir/ritonavir a dasabuvir (viz body 4.4 a 4.5).
4.4 Zvláštní upozornění a opatření pro použití
Pokud jsou přítomna jakákoli onemocnění nebo rizikové faktory uvedené níže, měla by být vhodnost přípravku YAZ s ženou prodiskutována.
-
V případě zhoršení nebo prvního výskytu jakéhokoli z těchto stavů nebo rizikových faktorů by mělo být ženě doporučeno, aby kontaktovala svého lékaře, který stanoví, zda by měla užívání přípravku YAZ ukončit.
-
V případě podezření nebo potvrzení žilního tromboembolismu (VTE) nebo arteriálního tromboembolismu (ATE) musí být přerušeno užívání kombinované hormonální antikoncepce (CHC). V případě, že je antikoagulační léčba zahájena, měla by být užívána adekvátní alternativní antikoncepce a to z důvodu teratogenních účinků antikoagulační léčby (kumariny).
Riziko žilního tromboembolismu (VTE)
Užívání jakékoli kombinované hormonální antikoncepce (CHC) zvyšuje riziko žilního tromboembolismu (VTE) ve srovnání s jejím neužíváním. Přípravky, které obsahují levonorgestrel, norgestimát nebo norethisteron jsou spojovány s nejnižším rizikem VTE. Další přípravky, jako je přípravek YAZ mohou mít až dvakrát vyšší úroveň rizika. Rozhodnutí používat jakýkoli přípravek jiný než ten, který má nejnižší riziko VTE, by mělo být učiněno po diskusi se ženou, aby se zajistilo, že rozumí riziku VTE u přípravku YAZ, rozumí, jak její současné rizikové faktory toto riziko ovlivňují a že riziko VTE je nejvyšší v prvním roce užívání léku. Existují také některé důkazy, že riziko je zvýšené, když je CHC opětovně zahájena po pauze v užívání trvající 4 týdny nebo déle.
U žen, které neužívají CHC a nejsou těhotné, se asi u 2 z 10 000 vyvine VTE v průběhu jednoho roku. U každé jednotlivé ženy však může být riziko daleko vyšší v závislosti na jejích základních rizikových faktorech (viz níže).
Odhaduje se že z 10 000 žen, které používají CHC obsahující drospirenon se u 9 až 12 žen vyvine VTE během jednoho roku; v porovnání s přibližně 6 případy u žen, které používají CHC obsahující levonorgestrel.
VTE může být fatální v 1–2 % případů.
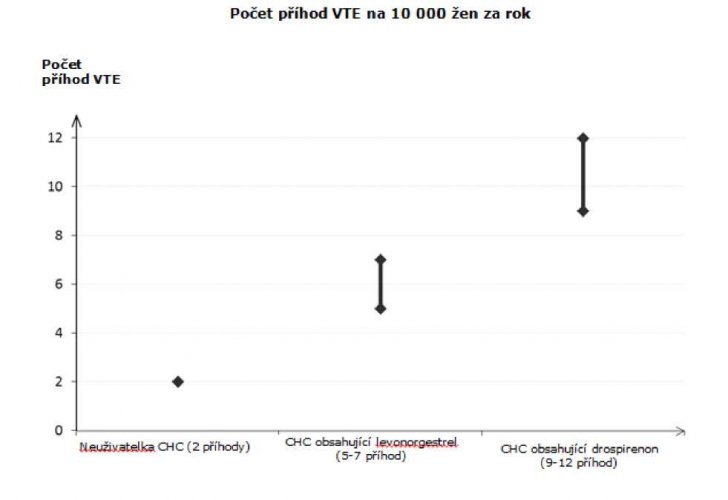
Extrémně vzácně byla hlášena trombóza u uživatelek CHC v dalších cévách, např. jaterních, mezenterických, renálních nebo retinálních žilách a tepnách.
Riziko žilních tromboembolických komplikací u uživatelek CHC se může podstatně zvyšovat u ženy, která má další rizikové faktory, zvláště pokud je přítomno více rizikových faktorů (viz tabulka).
Přípravek YAZ je kontraindikován, pokud má žena více rizikových faktorů, které pro ni představují vysoké riziko žilní trombózy (viz bod 4.3). Pokud má žena více než jeden rizikový faktor, je možné, že zvýšení rizika je vyšší než součet jednotlivých faktorů – v tomto případě by mělo být zváženo její celkové riziko VTE. Pokud je poměr přínosů a rizik považován za negativní, neměla by být CHC předepisována (viz bod 4.3).
Tabulka: Rizikové faktory VTE
| Rizikový faktor | Poznámka |
| Obezita (index tělesné hmotnosti nad 30 kg/m2) | Při zvýšení BMI se významně zvyšuje riziko. Zvláště důležité je zvážit, zda jsou také přítomny další rizikové faktory. |
| Prodloužená imobilizace, velký chirurgický zákrok, jakýkoli chirurgický zákrok na nohách a pánvi, neurochirurgický zákrok nebo větší trauma. | V těchto situacích je doporučeno ukončit užívání pilulky (v případě plánovaného chirurgického výkonu minimálně 4 týdny předem) a nezahajovat užívání do dvou týdnů po kompletní remobilizaci. Měla by se použít další antikoncepční metoda pro zabránění nechtěnému těhotenství. |
| Poznámka: dočasná imobilizace, včetně cestování letadlem > 4 hodiny může být také rizikovým faktorem VTE, zvláště u žen s dalšími rizikovými faktory | Antitrombotická léčba by měla být zvážena, pokud přípravek YAZ nebyl předem vysazen. |
| Pozitivní rodinná anamnéza (žilní tromboembolismus kdykoli u sourozence nebo rodiče, zvláště v relativně nízkém věku např. do 50 let věku). | Pokud je suspektní hereditární predispozice, měla by být žena před rozhodnutím o používání jakékoli CHC odeslána k odborníkovi na konzultaci |
| Další onemocnění související s VTE | Zhoubné onemocnění, systémový lupus erytematodes, hemolyticko-uremický syndrom, chronické zánětlivé onemocnění střev (Crohnova choroba nebo ulcerózní kolitida) a srpkovitá anémie |
| Vyšší věk | Zvláště nad 35 let |
Není žádná shoda o možné roli varixů a povrchové tromboflebitidy v nástupu nebo progresi žilní trombózy.
Zvýšené riziko tromboembolismu v těhotenství a zvláště během šestinedělí musí být zváženo (pro informaci o „Fertilita, těhotenství a kojení“ viz bod 4.6.)
V případě příznaků by mělo být ženě doporučeno, aby vyhledala naléhavou lékařskou péči a informovala lékaře, že užívá CHC.
Příznaky hluboké žilní trombózy (DVT) mohou zahrnovat:
-
– jednostranný otok nohy a/nebo chodidla nebo podél žíly v noze;
-
– bolest nebo citlivost v noze, která může být pociťována pouze vstoje nebo při chůzi;
-
– zvýšenou teplotu postižené nohy, zarudnutí nebo změnu barvy kůže nohy.
-
– náhlý nástup nevysvětlitelné dušnosti nebo rychlého dýchání;
-
– náhlý kašel, který může být spojený s hemoptýzou;
-
– ostrou bolest na hrudi;
-
– těžké točení hlavy nebo závrať způsobené světlem;
-
– rychlý nebo nepravidelný srdeční tep.
Některé z těchto příznaků (např. „dušnost“, „kašel“) nejsou specifické a mohou být nesprávně interpretovány jako častější nebo méně závažné příhody (např. infekce dýchacího traktu).
Dalšími známkami cévní okluze mohou být: náhlá bolest, otok a světle modré zbarvení končetin.
Pokud nastane okluze v oku, mohou se příznaky pohybovat od nebolestivého rozmazaného vidění, které může přejít do ztráty zraku. Někdy může nastat ztráta zraku téměř okamžitě.
Epidemiologické studie spojovaly používání CHC se zvýšeným rizikem arteriálního tromboembolismu (infarkt myokardu) nebo cerebrovaskulární příhody (např. tranzitorní ischemická ataka, cévní mozková příhoda). Arteriální tromboembolické příhody mohou být fatální.
Riziko arteriálních tromboembolických komplikací nebo cerebrovaskulární příhody u uživatelek CHC se zvyšuje u žen s rizikovými faktory (viz tabulka). Přípravek YAZ je kontraindikován, pokud má žena jeden závažný rizikový faktor nebo více rizikových faktorů ATE, které pro ni představují riziko arteriální trombózy (viz bod 4.3). Pokud má žena více než jeden rizikový faktor, je možné, že zvýšení rizika je vyšší než součet jednotlivých faktorů – v tomto případě by mělo být zváženo její celkové riziko. Pokud je poměr přínosů a rizik považován za negativní, neměla by být CHC předepisována (viz bod 4.3).
Tabulka: Rizikové faktory ATE
| Rizikový faktor | Poznámka |
| Vyšší věk | Zvláště nad 35 let |
| Kouření | Ženě by mělo být doporučeno, aby nekouřila, pokud chce používat CHC. Ženám ve věku nad 35 let, které dále kouří, by mělo být důrazně doporučeno, aby používaly jinou metodu antikoncepce. |
| Hypertenze | |
| Obezita (index tělesné hmotnosti nad 30 kg/m2) | Při zvýšení BMI se významně zvyšuje riziko. Zvláště důležité u žen s dalšími rizikovými faktory |
| Pozitivní rodinná anamnéza (arteriální tromboembolismus kdykoli u sourozence nebo rodiče, zvláště v relativně nízkém věku např. do 50 let věku). | Pokud je suspektní hereditární predispozice, měla by být žena odeslána k odborníkovi na konzultaci před rozhodnutím o používání jakékoli CHC |
| Migréna | Zvýšení frekvence nebo závažnosti migrény během používání CHC (což může být prodromální známka cévní mozkové příhody) může být důvodem okamžitého ukončení léčby |
| Další onemocnění související s nežádoucími cévními příhodami | Diabetes mellitus, hyperhomocysteinémie, chlopenní srdeční vada a fibrilace síní, dyslipoproteinémie a systémový lupus erytematodes. |
V případě příznaků by mělo být ženě doporučeno, aby vyhledala naléhavou lékařskou péči a informovala lékaře, že užívá CHC.
Příznaky cévní mozkové příhody mohou zahrnovat:
-
– náhlou necitlivost nebo slabost obličeje, paže nebo nohy, zvláště na jedné straně těla;
-
– náhlé potíže s chůzí, závratě, ztrátu rovnováhy nebo koordinace;
-
– náhlou zmatenost, problémy s řečí nebo porozuměním;
-
– náhlé potíže se zrakem na jednom nebo obou očích;
-
– náhlou, závažnou nebo prodlouženou bolest hlavy neznámé příčiny;
-
– ztrátu vědomí nebo omdlení s nebo bez záchvatu.
-
– bolest, nepříjemný pocit, tlak, těžkost, pocit stlačení nebo plnosti na hrudi, v paži nebo pod hrudní kostí;
-
– nepříjemný pocit vyzařující do zad, čelisti, hrdla, paže, žaludku;
-
– pocit plnosti, poruchu trávení nebo dušení;
-
– pocení, nauzeu, zvracení nebo závratě;
-
– extrémní slabost, úzkost nebo dušnost;
-
– rychlý nebo nepravidelný srdeční tep.
- Nádory
- Ostatní stavy
Před prvním zahájením nebo znovuzahájením léčby přípravkem YAZ by měla být získána kompletní anamnéza (včetně rodinné anamnézy) a musí být vyloučeno těhotenství. Měl by se změřit krevní tlak a mělo by být provedeno tělesné vyšetření při zvážení kontraindikací (viz bod 4.3) a varování (viz bod 4.4). Je důležité, aby byla žena upozorněna na informace o žilní a arteriální trombóze, včetně rizika přípravku YAZ v porovnání s dalšími typy CHC, na příznaky VTE a ATE, známé rizikové faktory a co by měla dělat v případě suspektní trombózy.
Žena by také měla být informována, aby si pečlivě přečetla příbalovou informaci pro uživatele a aby dodržovala uvedené instrukce. Frekvence a povaha vyšetření by měly být založeny na stanovených postupech a upraveny podle individuálních potřeb ženy.
Ženy by měly být informovány, že hormonální antikoncepce nechrání před HIV infekcí (AIDS) a dalšími sexuálně přenosnými chorobami.
Účinnost COC může být snížena například při vynechání účinné tablety (viz bod 4.2), v případě gastrointestinálních poruch při užívání účinných tablet (viz bod 4.2), nebo při současném užívání dalších léků (viz bod 4.5).
Při užívání všech kombinovaných perorálních kontraceptiv (COC) může dojít k nepravidelnému krvácení (špinění či krvácení z průniku mimo periodu), zvláště během prvních měsíců užívání. Z toho důvodu má hledání příčiny nepravidelného krvácení smysl až po adaptačním intervalu přibližně tří cyklů.
Pokud nepravidelnosti v krvácení trvají či se vyskytnou po dosud pravidelných cyklech, je třeba zvážit jiné než hormonální příčiny a provést odpovídající diagnostické kroky k vyloučení malignit a těhotenství. Mohou zahrnovat i kyretáž.
U některých žen nemusí dojít během placebového období ke krvácení. Pokud byly tablety užívány podle pokynů popsaných v bodě 4.2, je otěhotnění ženy nepravděpodobné. Pokud však přípravek před absencí prvního pravidelného krvácení nebyl používán podle pokynů, či pokud dojde k vynechání dvou krvácení po sobě, před dalším užíváním přípravku je třeba vyloučit možnost těhotenství.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Poznámka: aby byly zjištěny možné interakce, mají být prostudovány příbalové informace současně užívaných léků.
Účinky jiných léčivých přípravků na přípravek YazInterakce se mohou objevit s léky, které indukují jaterní enzymy, což může mít za následek zvýšenou clearance pohlavních hormonů a může vést ke krvácení z průniku a/nebo k selhání kontracepce.
Postup
Enzymová indukce může být pozorována již po několika dnech léčby. Maximální enzymová indukce je obvykle pozorována během několika týdnů. Po přerušení léčby může enzymová indukce přetrvávat po dobu okolo 4 týdnů.
Krátkodobá léčba
Ženy, které se léčí některým z enzymy indukujících léků, by měly přechodně používat navíc k COC bariérovou kontracepční metodu nebo použít jinou metodu kontracepce. Bariérová metoda musí být používána po celou dobu léčby souběžně podávaným lékem a dalších 28 dní po ukončení léčby.
Pokud léčba zasáhne do období ukončení užívání účinných tablet COC ze stávajícího blistru, placebo tablety musí být vyřazeny a ihned má být zahájeno užívání dalšího blistru COC.
Dlouhodobá léčba
Pokud je žena na dlouhodobé léčbě léčivou látkou, která indukuje jaterní enzymy, doporučuje se používat jinou spolehlivou nehormonální kontracepci.
V literatuře byly popsány následující interakce.
Látky zvyšující clearance COC (snižují účinnost COC enzymovou indukcí) například: barbituráty, bosentan, karbamazepin, fenytoin, primidon, rifampicin a léky na HIV infekci ritonavir, nevirapin a efavirenz a zřejmě také felbamát, griseofulvin, oxkarbazepin, topiramát a přípravky obsahující třezalku tečkovanou (hypericum perforatum).
Látky s různým účinkem na clearance COC:
Při současném podávání společně s COC mnoho kombinací inhibitorů HIV proteázy a nenukleosidových inhibitorů reverzní transkriptázy včetně kombinací s HCV inhibitory může snižovat nebo zvyšovat plazmatickou koncentraci estrogenu nebo progestinů. Účinek těchto změn může být v některých případech klinicky významný.
Proto by měly být prostudovány informace o přípravku k souběžné léčbě HIV/HCV, aby byly identifikovány možné interakce, a příslušná doporučení. V případě jakýchkoliv pochyb by ženy, které jsou na léčbě inhibitory proteázy nebo nenukleosidovými inhibitory reverzní transkriptázy, měly navíc použít bariérovou kontracepční metodu.
Látky snižující clearance COC (enzymové inhibitory):
Klinický význam potenciálních interakcí s enzymovými inhibitory zůstává neznámý.
Souběžné podávání silných inhibitorů CYP3A4 může zvýšit plasmatickou koncentraci estrogenu nebo progestinu nebo obou hormonů.
Ve studii s opakovanými dávkami kombinace drospirenon (3 mg denně)/ ethinylestradiol (0,02 mg denně), souběžné podání silného inhibitoru CYP3A4 ketokonazolu po dobu 10 dní zvýšilo AUC(0–24 hod) drospirenonu a ethinylestradiolu 2,7krát a 1,4krát.
Bylo zjištěno, že etorikoxib v dávkách 60 až 120 mg denně zvyšuje plasmatickou koncentraci ethinylestradiolu 1,4 až 1,6krát, zejména, je-li užíván současně s kombinovanými hormonálními kontraceptivy obsahujícími 0,035 mg ethinylestradiolu.
- Účinky přípravku YAZ na jiné léčivé přípravky
- Farmakodynamické interakce
- Jiné formy interakce
Laboratorní vyšetření
Užívání kontracepčních steroidů může ovlivnit výsledky některých laboratorních testů, včetně biochemických parametrů jaterních, thyreoidálních, adrenálních a renálních funkcí, plasmatických hladin proteinů (vazebných) např. transkortinu (CBG) a lipid/lipoproteinové frakce, parametrů sacharidového metabolismu, koagulace a fibrinolýzy. Změny obvykle zůstávají v rozmezí normálních laboratorních referenčních hodnot. Drospirenon způsobuje zvýšení plasmatické aktivity reninu a plasmatického aldosteronu svoji mírnou antimineralokortikoidní aktivitou.
4.6 Fertilita, těhotenství a kojení
Těhotenství
Přípravek YAZ není indikován během těhotenství.
Pokud během užívání přípravku dojde k otěhotnění, jeho další užívání musí být ihned ukončeno. Rozsáhlé epidemiologické studie však nezaznamenaly zvýšené riziko vrozených vad u dětí narozených ženám užívajícím COC před otěhotněním, ani teratogenní vliv COC neúmyslně užívaných v časném těhotenství.
Studie na zvířatech ukázaly nežádoucí účinek během těhotenství a kojení (viz bod 5.3). Na základě těchto údajů získaných na zvířatech nelze vyloučit nežádoucí hormonální působení léčivých látek. Všeobecné zkušenosti s užíváním COC během těhotenství však neprokázaly žádný konkrétní nežádoucí účinek u člověka.
Údaje týkající se užívání přípravku YAZ v těhotenství jsou příliš omezené, než aby bylo možno udělat závěry o jeho negativním vlivu na těhotenství, zdraví plodu nebo novorozence. Doposud nejsou k dispozici žádné relevantní epidemiologické údaje.
Zvýšené riziko VTE během poporodního období je třeba brát v úvahu při znovuzahájení užívání přípravku YAZ (viz bod 4.2 a 4.4).
Kojení
Kojení může být ovlivněno kombinovanými perorálními kontraceptivy, která mohou snížit množství mateřského mléka a změnit jeho složení. Užívání perorální kontracepce tedy obecně nelze doporučit, dokud kojící matka dítě zcela nepřevedla na umělou stravu. Malé množství kontracepčních steroidů a /nebo jejich metabolitů může být při jejich užívání vylučováno do mléka. Tato množství mohou mít vliv na dítě.
Fertilita
Přípravek YAZ je indikován k prevenci otěhotnění. Informace o návratu fertility viz bod 5.1.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Studie hodnotící účinky na schopnost řídit a používat stroje nebyly provedeny. Žádné účinky na schopnost řídit vozidlo nebo obsluhovat stroje nebyly u uživatelek COC pozorovány.
4.8 Nežádoucí účinky
Nejzávažnější nežádoucí účinky spojené s užíváním COC viz také bod 4.4.
Během užívání přípravku YAZ byly hlášeny následující nežádoucí účinky:
Následující tabulka uvádí nežádoucí účinky podle tříd orgánových systémů databáze MedDRA. Frekvence jsou založené na údajích z klinických studií. K popisu reakcí a souvisejících stavů byly použity nejvhodnější termíny dle MedDRA.
Nežádoucí reakce spojené s užíváním přípravku YAZ jako perorální kontracepce nebo k léčbě mírné acne vulgaris podle tříd orgánových systémů a terminologie MedDRA.
| Třída orgánových systémů (verze MedDRA 9.1) | Časté (> /100 až < 1/10) | Méně časté (>1/1000 až >1/100) | Vzácné (>1/10 000 až > 1/1000) | Není známo (z dostupných údajů nelze určit) |
| Infekce a infestace | kandidóza | |||
| Poruchy krve a lymfatického systému | anémie trombocytemie | |||
| Poruchy imunitního systému | alergická reakce | hypersensitivita | ||
| Endokrinní poruchy | endokrinní porucha | |||
| Poruchy metabolismu a výživy | zvýšená chuť k jídlu anorexie hyperkalemie hyponatremie | |||
| Psychiatrické poruchy | psychická labilita | deprese nervozita somnolence | anorgasmie nespavost | |
| Poruchy nervového systému | bolesti hlavy | závratě parestézie | vertigo třes | |
| Poruchy oka | zánět spojivek suché oči další oční poruchy | |||
| Srdeční poruchy | tachykardie | |||
| Cévní poruchy | migréna křečové žíly hypertenze | flebitida jiná porucha cév epistaxe synkopa žilní tromboembolismus (VTE) arteriální tromboembolismus (ATE) |
| Třída orgánových systémů (verze MedDRA 9.1) | Časté (> /100 až < 1/10) | Méně časté (>1/1000 až >1/100) | Vzácné (>1/10 000 až > 1/1000) | Není známo (z dostupných údajů nelze určit) |
| Gastrointestinální poruchy | nauzea | bolesti břicha zvracení dyspepsie flatulence gastritida průjem | zvětšené břicho gastrointestinální poruchy plynatost hiátová hernie orální kandidóza zácpa pocit sucha v ústech | |
| Poruchy jater a žlučových cest | bolesti žlučníku cholecystitida | |||
| Poruchy kůže a podkožní tkáně | akné svědění vyrážka | chloasma ekzém alopecie dermatitis acneiform suchá kůže erythema nodosum hypertrichóza kožní poruchy kožní strie kontaktní dermatitida fotosenzitivní dermatitida kožní uzlíky | multiformní erytém | |
| Poruchy pohybového systému a pojivové tkáně | bolest v zádech bolest v končetinách svalové křeče |
| Třída orgánových systémů (verze MedDRA 9.1) | Časté (> /100 až < 1/10) | Méně časté (>1/1000 až >1/100) | Vzácné (>1/10 000 až > 1/1000) | Není známo (z dostupných údajů nelze určit) |
| Poruchy reprodukčního systému prsu | bolest na prsou metroragie* amenorea | vaginální kandidóza pánevní bolesti zvětšení prsů fibrocystické onemocnění prsu děložní a vaginální krvácení* výtok z genitálií návaly horka vaginitida poruchy menstruace dysmenorea hypomenorea menoragie suchost pochvy suspektní nález ve stěru Pap snížení libida | dyspareunie vulvovaginitida krvácení po pohlavním styku krvácení při vysazení léku cysta v prsu hyperplazie prsu novotvary prsu cervikální polyp atrofie endometria ovariální cysty zvětšení dělohy | |
| Celkové poruchy a reakce v místě aplikace | astenie zvýšené pocení edém (celkový edém, periferní edém, edém obličeje) | malátnost | ||
| Vyšetření | zvýšení tělesné hmotnosti | snížení tělesné hmotnosti |
* nepravidelnosti krvácení obvykle vymizí během další léčby
Popis vybraných nežádoucích účinků
U žen užívajících CHC bylo pozorováno zvýšené riziko arteriálních a žilních trombotických a tromboembolických příhod, včetně infarktu myokardu, cévní mozkové příhody, tranzitorních ischemických atak, žilní trombózy a plicní embolie a je podrobněji popsáno v bodě 4.4.
Následující závažné nežádoucí účinky byly hlášeny u žen užívajících COC, které jsou podrobněji uvedeny v bodě 4.4 Zvláštní upozornění a opatření pro použití:
-
– žilní tromboembolické poruchy;
-
– arteriální tromboembolické poruchy;
-
– hypertenze;
-
– tumory jater;
-
– výskyt nebo zhoršování stavů, kde spojitost s COC není jasná: Crohnova choroba, ulcerózní kolitida, epilepsie, děložní myom, porfyrie, systémový lupus erythematodes, herpes gestationis, Sydenhamova chorea, hemolyticko-uremický syndrom, cholestatická žloutenka;
-
– chloasma;
-
– akutní nebo chronické poruchy funkce jater si mohou vyžádat přerušení užívání COC, dokud se hodnoty ukazatelů jaterní funkce nevrátí do normálních hodnot.
– u žen s vrozeným angioedémem mohou exogenní estrogeny indukovat nebo exacerbovat symptomy angioedému.
U uživatelek kombinovaných perorálních kontraceptiv (COC) je lehce zvýšena frekvence rakoviny prsu. Protože rakovina prsu je vzácná u žen pod 40 let věku, počet případů navíc je malý ve vztahu k celkovému riziku rakoviny prsu. Kauzální vztah ke kombinovaným perorálním kontraceptivům není znám. Další informace viz body 4.3 a 4.4.
Interakce
Následkem interakcí jiných léků (enzymových induktorů) s perorální kontracepcí může být krvácení z průniku a/nebo selhání kontracepčního účinku (viz bod 4.5).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
Webové stránky:
4.9 Předávkování
S předávkováním přípravkem YAZ nejsou dosud žádné zkušenosti. Na základě zkušeností s ostatními perorálními kombinovanými kontraceptivy by se v tomto případě mohly vyskytnout tyto příznaky: nauzea, zvracení a krvácení z vysazení. Krvácení z vysazení se může objevit i u mladých dívek, které ještě nemají menstruaci, a které náhodně užily tento přípravek. Antidotum neexistuje a další léčba má být symptomatická.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina (ATC): Gestageny a estrogeny, fixní kombinace
ATC kód: G03AA12
Pearl index selhání metody: 0,41 (horní hranice 95 % intervalu spolehlivosti: 0,85).
Celkový Pearl index (selhání metody + selhání pacientky): 0,80 (horní hranice 95 % intervalu spolehlivosti: 1,30).
Antikoncepční účinek přípravku YAZ je založen na spolupůsobení různých faktorů. Nejdůležitější z nich je inhibice ovulace a změny endometria.
Během tři cykly trvající studie sledující inhibici ovulace a porovnávající podávání drospirenonu 3 mg/ ethinylestradiolu 0,020 mg ve 24 denním dávkovacím režimu oproti 21 dennímu dávkovacímu režimu, vykázal 24 denní režim větší potlačení vývoje folikulů. Po úmyslně vyvolaných chybách dávkování během třetího cyklu léčby se u více žen ve 21 denním režimu prokázala ovariální aktivita, včetně zvýšeného rizika ovulace, ve srovnání se ženami užívajícími 24 denní režim. Ovariální aktivita se vrátila na úroveň před léčbou během cyklu po ukončení léčby u 91,8 % žen, které užívaly 24 denní režim.
Přípravek YAZ je kombinované perorální kontraceptivum obsahující ethinylestradiol a gestagen drospirenon. V terapeutických dávkách má drospirenon také antiandrogenní a mírné antimineralokortikoidní vlastnosti. Nemá estrogenní, glukokortikoidní ani antiglukokortikoidní aktivitu. Tím má drospirenon farmakologický profil výrazně podobný přirozenému hormonu progesteronu.
Z klinických studií vyplynulo, že slabé antimineralokortikoidní vlastnosti přípravku YAZ mají za následek jeho mírný antimineralokortikoidní účinek.
Byly provedeny dvě multicentrické, dvojitě zaslepené, randomizované a placebem kontrolované klinické studie hodnotící účinnost a bezpečnost přípravku YAZ u žen se středně závažnou formou akné.
Po šesti měsících léčby ve srovnání s placebem, přípravek YAZ prokázal statisticky významné snížení výskytu zánětlivých lézí o 15,6 % (49,3 % vs. 33,7 %), nezánětlivých lézí o 18,5 % (40,6 % vs. 22,1 %), a lézí celkem o 16,5 % (44,6 % vs. 28,1 %). Navíc bylo vyšší procento pacientek o 11,8% (18,6 % vs. 6,8 %) s hodnocením „čistá“ nebo „téměř čistá“ na stupnici ISGA (Investigator's Static Global Assessment).
5.2 Farmakokinetické vlastnosti
- Drospirenon
Absorpce
Perorálně podaný drospirenon je rychle a téměř úplně absorbován. Maximální koncentrace látky v séru -asi 38 ng/ml – je dosaženo přibližně za 1 – 2 hodiny po jednorázovém podání. Biologická dostupnost je 76 – 85 %. Na biologickou dostupnost drospirenonu nemá současné požití potravy žádný vliv.
Distribuce
Po perorálním podání klesá sérová hladina drospirenonu s konečným poločasem 31 hodin. Drospirenon je vázán na sérový albumin, není vázán na pohlavní hormony vážící globulin (SHBG) ani na kortikosteroidy vážící globulin (CBG). Jen 3 – 5 % celkové sérové koncentrace účinné látky je přítomno ve formě volného steroidu. Ethinylestradiolem indukované zvýšení SHBG neovlivňuje vazbu drospirenonu na sérové proteiny. Průměrný distribuční objem drospirenonu je 3,7 ± 1,2 l/kg.
Biotransformace
Drospirenon je po perorálním podání z velké části metabolizován. Nejdůležitějšími metabolity v plazmě jsou kyselá forma drospirenonu vzniklá otevřením laktonového kruhu a 4,5-dihydro-drospirenon-3-sulfát, tvořené redukcí a následnou sulfatací. Drospirenon je také předmětem oxidativního metabolismu katalyzovaného CYP3A4.
In vitro má drospirenon schopnost slabě až středně silně inhibovat enzymy CYP1A1, CYP2C9, CYP2C19 a CYP3A4 cytochromu P450.
Eliminace
Rychlost metabolické clearance drospirenonu ze séra je 1,5 ± 0,2 ml/min/kg. Drospirenon je vylučován v nezměněné formě pouze ve stopovém množství. Metabolity jsou vylučovány stolicí a močí v poměru 1,2 až 1,4. Poločas vylučování metabolitů močí a stolicí je asi 40 hodin.
Rovnovážný stav
Během léčebného cyklu je maximální koncentrace drospirenonu v rovnovážném stavu okolo 70 ng/ml dosaženo přibližně po 8 dnech léčby. Hladiny drospirenonu se akumulují přibližně faktorem 3 v důsledku poměru konečného poločasu a dávkovacího intervalu.
Zvláštní skupiny pacientů
Vliv poruchy funkce ledvin
Hladiny drospirenonu v rovnovážném stavu u žen s mírnou poruchou funkce ledvin (clearance creatininu CLcr 50–80 ml/min) byly srovnatelné s ženami, jejichž funkce ledvin byla normální. U žen se středně závažnou poruchou funkce ledvin (Clcr 30–50 ml/min) byly hladiny drospirenonu v průměru o 37 % vyšší ve srovnání s ženami s normální funkcí ledvin. Léčba drospirenonem u žen s mírnou až středně těžkou poruchou funkce ledvin byla také dobře tolerována. Léčba drospirenonem nevykazovala žádný klinicky významný účinek na koncentrace draslíku v séru.
Vliv poruchy funkce jater
U dobrovolnic se středně závažnou poruchou funkce jater byl po jednorázovém podání pozorován asi 50 % pokles perorální clearance ve srovnání s ženami s normální funkcí jater. Pozorovaný pokles clearance drospirenonu u dobrovolnic se středně závažnou poruchou funkce jater ve srovnání se zdravými se neprojevil jako patrný rozdíl koncentrací draslíku v séru. Dokonce ani za přítomnosti diabetes a současné léčby spironolaktonem (dvou faktorů, které predisponují pacienta k hyperkalémii), nebyl pozorován vzestup draslíku nad hranici rozmezí normálních hodnot. Závěrem lze říci, že u pacientek s mírnou nebo středně závažnou poruchou funkce jater (Child-Pugh B) byl drospirenon dobře tolerován.
Etnické skupiny
Nebyly pozorovány žádné klinicky významné rozdíly ve farmakokinetice drospirenonu nebo ethinylestradiolu mezi bílými ženami a Japonkami.
- Ethinylestradiol
Absorpce
Perorálně podaný ethinylestradiol je rychle a kompletně absorbován. Nejvyšší sérové koncentrace okolo 33 pg/ml je dosaženo po jednorázové perorální dávce během 1 – 2 hodin. Absolutní biologická dostupnost je přibližně 60 % následkem presystémové konjugace a first-pass metabolismu. Současné požití stravy snížilo biologickou dostupnost ethinylestradiolu asi u 25 % sledovaných subjektů, zatímco u ostatních nebyly pozorovány žádné změny.
Distribuce
Sérové koncentrace ethinylestradiolu klesají ve dvou fázích, konečná dispoziční fáze je charakterizována poločasem přibližně 24 hodin. Ethinylestradiol je vysoce, ale nespecificky vázán na sérový albumin (přibližně 98,5 %) a indukuje vzestup sérové koncentrace SHBG a kortikoid vázajícího globulinu (CBG). Distribuční objem byl stanoven na cca 5 l/kg.
Biotransformace
Ethinylestradiol podléhá významnému metabolismu prvního průchodu v tenkém střevě a játrech. Ethinylestradiol je primárně metabolizován aromatickou hydroxylací, vzniká však velké množství různých hydroxylovaných a methylovaných metabolitů, které jsou přítomny jako volné metabolity nebo jako konjugáty s glukuronidy a sulfáty. Metabolická clearance ethinylestradiolu je kolem 5 ml/min/kg.
In vitro je ethinylestradiol reversibilní inhibitor CYP2C19, CYP1A1 a CYP1A2 a pevně vázaný inhibitor CYP3A4/5, CYP2C8 a CYP2J2.
Eliminace
Ethinylestradiol není ve významném množství vylučován v nezměněné formě. Metabolity ethinylestradiolu jsou vylučovány močí a žlučí v poměru 4 : 6. Poločas exkrece metabolitů je asi 1 den.
Rovnovážný stav
Rovnovážného stavu je dosaženo během druhé poloviny léčebného cyklu a sérové hladiny ethinylestradiolu se kumulují faktorem od 2,0 do 2,3.
5.3 Předklinické údaje vztahující se k bezpečnosti
U laboratorních zvířat byly účinky drospirenonu a ethinylestradiolu omezeny na ty, které jsou spojeny s jejich známým farmakologickým působením. Zejména studie reprodukční toxicity odhalily u zvířat embryotoxické a fetotoxické účinky, které jsou považovány za druhově specifické. Při expozici drospirenonu v dávkách vyšších, než jaké jsou přijímány v přípravku YAZ, byly pozorovány účinky na diferenciaci pohlaví u plodů potkanů, ale nikoliv u plodů opic.
Studie posuzující riziko pro životní prostředí ukázaly, že ethinylestradiol a drospirenon mají potenciál představovat riziko pro vodní prostředí (viz bod 6.6).
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Účinné potahované tablety (světle růžové):
Placebo potahované tablety (bílé)
monohydrát laktosy mikrokrystalická celulosa magnesium-stearát (E470b)
hypromelóza (E464) mastek (E553b)
oxid titaničitý (E171)
Jádro tablety:
monohydrát laktosy
kukuřičný škrob magnesium-stearát (E470b)
Potahová vrstva tablet:
hypromelóza (E464)
mastek (E553b)
oxid titaničitý (E171)
červený oxid železitý (E172)
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
5 let.
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
6.5 Druh obalu a obsah balení
Průhledný blistr – PVC/Al v kartonovém pouzdru, krabička.
Upozornění:
Text na kartonovém pouzdru je ve slovinštině.
Velikosti balení:
3 × 28 tablet
Každý blistr obsahuje 24 světle růžových účinných potahovaných tablet a 4 bílé placebo potahované tablety.
6.6 Zvláštní opatření pro likvidaci přípravku
Tento léčivý přípravek může představovat riziko pro životní prostředí (viz bod 5.3). Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Bayer d.o.o., Bravničarjeva 13, 1000, Ljubljana, Slovinsko
Chemark s.r.o., U Staré tvrze 285/21, 196 00 Praha 9 – Třeboradice, Česká republika
8. REGISTRAČNÍ ČÍSLO(A)
17/316/08-C/PI/001/15
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
7. 10. 2015
Další informace o léčivu YAZ 0,02 MG/3 MG POTAHOVANÉ TABLETY
Jak
se YAZ 0,02 MG/3 MG POTAHOVANÉ TABLETY
podává: perorální podání - potahovaná tableta
Výdej
léku: na lékařský předpis
Balení: Blistr
Velikost
balení: 3X28
Držitel rozhodnutí o registraci daného léku v České republice:
Bayer d.o.o., Ljubljana
