Souhrnné informace o léku - NELYA
1. NÁZEV PŘÍPRAVKU
Nelya 0,06 mg/0,015 mg potahované tablety
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
24 žlutých potahovaných tablet:
Jedna potahovaná tableta obsahuje gestodenum 0,06 mg a ethinylestradiolum 0,015 mg.
Pomocná látka se známým účinkem: laktóza 39,9 mg
4 bílé tablety placeba (neaktivní):
Tableta neobsahuje léčivé látky.
Pomocná látka se známým účinkem: laktóza 59,5 mg
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Aktivní potahovaná tableta je kulatá žlutá tableta s konvexními stranami.
Tableta placeba je kulatá bílá tableta s konvexními stranami.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Perorální antikoncepce.
Rozhodnutí předepsat přípravek Nelya má být provedeno po zvážení jednotlivých současných rizikových faktorů ženy, zvláště rizikových faktorů pro žilní tromboembolismus (VTE), a toho, jaké je riziko VTE u přípravku Nelya v porovnání s dalšími přípravky kombinované hormonální antikoncepce CHC (viz body 4.3 a 4.4).
4.2 Dávkování a způsob podání
Tablety musí být užívány každý den přibližně ve stejnou dobu, v případě nutnosti s malým množstvím tekutiny, v pořadí uvedeném na blistru. Užívání tablet je kontinuální. Jedna tableta se užívá denně po dobu 28 po sobě jdoucích dnů. Užívání každého dalšího blistru se zahajuje den po užití poslední tablety z předchozího blistru. Krvácení z vysazení obvykle začíná v den 2–3 po zahájení užívání tablet placeba (poslední řada) a může pokračovat i po zahájení užívání dalšího blistru.
- Bez předchozího užívání hormonální antikoncepce (v předchozím měsíci)
- Přechod z kombinované hormonální antikoncepce (kombinované perorální antikoncepce (COC), vaginálního kroužku nebo transdermální náplasti)
- Přechod z kontracepční metody obsahující pouze gestagen (pilulka, injekce či implantát obsahující pouze gestagen) nebo z intrauterinního systému (IUS) uvolňujícího gestagen
- Po potratu v prvním trimestru
- Po porodu nebo po potratu ve druhém trimestru
Tablety placeba z poslední (5.) řady blistru je možno ignorovat. Je třeba je však zlikvidovat, aby nedošlo k neúmyslnému prodloužení fáze s tabletami placeba. Následující informace se týkají pouze vynechaných účinných tablet:
Pokud se uživatelka zpozdila s užíváním kterékoli tablety o méně než 12 hodin, nesnižuje se antikoncepční ochrana. Žena má tabletu užít ihned, jakmile si vzpomene, a další tablety má užít v obvyklé době.
Pokud se uživatelka zpozdila s užíváním kterékoli tablety o více než 12 hodin, antikoncepční ochrana může být snížena. Další opatření se pak mohou řídit následujícími dvěma základními pravidly:
-
1. užívání tablet nesmí být nikdy přerušeno na více než 4 dny;
-
2. aby bylo dosaženo odpovídající suprese hypotalamo-hypofyzárně-ovariální osy, je třeba tablety užívat nepřetržitě 7 dní.
-
V souladu s těmito pravidly lze v běžné praxi poskytnout následující doporučení:
- Den 1–7
- Den 8–14
- Den 15–24
-
1. Uživatelka má užít poslední vynechanou tabletu ihned, jakmile si vzpomene, a to i tehdy, znamená-li to, že užije dvě tablety ve stejnou dobu. Poté pokračuje v užívání tablet v obvyklou dobu, dokud nejsou účinné tablety využívány. Poslední 4 tablety placeba z poslední řady je třeba zlikvidovat. Žena ihned zahájí užívání tablet z dalšího blistru. Uživatelka pravděpodobně nebude mít krvácení z vysazení, dokud nevyužívá účinné tablety z druhého blistru, ale může zaznamenat špinění nebo krvácení z průniku ve dny, kdy užívá tablety.
-
2. Ženě může být rovněž doporučeno, aby přestala užívat účinné tablety z aktuálního blistru. Poté má užívat tablety placeba z poslední řady, a to po dobu maximálně 4 dnů včetně dnů, kdy zapomněla užívat tablety, a následně pokračovat novým blistrem.
V případě závažných gastrointestinálních obtíží (např. zvracení či průjmu) nemusí být vstřebávání tablet účinné a je zapotřebí použít doplňkové antikoncepční metody. Pokud do 3–4 hodin po užití účinné tablety dojde ke zvracení, je třeba co možná nejdříve užít novou (náhradní) tabletu. Novou tabletu je nutno užít pokud možno do 12 hodin od obvyklé doby užívání tablet. Pokud uplyne více než 12 hodin, postupujte podle pokynů týkajících se vynechaných tablet, které jsou uvedeny v bodu 4.2 „Postup při vynechání tablet“. Pokud žena nechce měnit svůj běžný režim užívání tablet, musí si vzít zvláštní tabletu (tablety) z jiného blistru.
Chce-li žena odložit svou periodu, musí pokračovat v užívání tablet z dalšího blistru přípravku Nelya, aniž užije tablety placeba z prvního blistru. Takto lze pokračovat dle přání uživatelky až do využívání účinných tablet z druhého blistru. Během nepřetržitého užívání může žena zaznamenat krvácení z průniku nebo špinění. V normálním režimu užívání přípravku Nelya se potom pokračuje po využívání tablet fáze placeba.
Pokud si chce žena přesunout začátek periody na jiný den v týdnu, než na který je zvyklá při současném režimu užívání, doporučuje se zkrátit nadcházející fázi tablet placeba o příslušný počet dnů. Čím kratší bude pauza, tím vyšší bude riziko, že se nedostaví krvácení z průniku a že se během následujícího blistru objeví krvácení z průniku a špinění (podobně jako při odložení periody).
4.3 Kontraindikace
Kombinovaná hormonální antikoncepce (CHC) se nesmí používat u následujících stavů. Pokud by se takový stav poprvé vyskytl v době užívání COC, musí se užívání okamžitě přerušit:
- Hypersenzitivita na léčivé látky nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
- Přítomnost nebo riziko žilního tromboembolismu (VTE)
o žilní tromboembolismus – současný žilní tromboembolismus (léčený pomocí antikoagulancií) nebo anamnéza VTE (např. hluboká žilní trombóza [DVT] nebo plicní embolie [PE]) 3
o známá dědičná nebo získaná predispozice pro žilní tromboembolismus, jako je rezistence na APC (včetně faktoru V Leiden), deficit antitrombinu III, deficit proteinu C, deficit proteinu S
o velký chirurgický zákrok s déletrvající imobilizací (viz bod 4.4)
o vysoké riziko žilního tromboembolismu v důsledku přítomnosti více rizikových faktorů (viz bod 4.4);
- Přítomnost nebo riziko arteriálního tromboembolismu (ATE)
o arteriální tromboembolismus – současný arteriální tromboembolismus, anamnéza arteriálního tromboembolismu (např. infarkt myokardu) nebo prodromální stav (např. angina pectoris);
o cerebrovaskulární onemocnění – současná cévní mozková příhoda, anamnéza cévní mozkové příhody nebo prodromálního stavu (např. tranzitorní ischemická ataka, TIA);
o známá hereditární nebo získaná predispozice k arteriálnímu tromboembolismu, jako je hyperhomocysteinémie a antifosfolipidové protilátky (antikardiolipinové protilátky, lupus antikoagulans);
o anamnéza migrény s fokálními neurologickými příznaky;
o vysoké riziko arteriálního tromboembolismu v důsledku vícečetných rizikových faktorů (viz bod 4.4) nebo přítomnosti jednoho závažného rizikového faktoru, jako je:
- diabetes mellitus s cévními příznaky;
- závažná hypertenze;
- závažná dyslipoproteinémie
- známé nebo suspektní pohlavními steroidy ovlivněných malignit (např. pohlavních orgánů nebo prsu);
- závažné jaterní poruchy současné nebo v anamnéze, dokud nejsou v normě jaterní testy;
- benigní nebo maligní tumory jater současné nebo v anamnéze;
- nediagnostikované vaginální krvácení;
- pankreatitida nebo anamnéza pankreatitidy spojená se závažnou dyslipoproteinémií.
4.4. Zvláštní upozornění a opatření pro použití
Pokud jsou přítomna jakákoli onemocnění nebo rizikové faktory uvedené níže, má být vhodnost přípravku Nelya s ženou prodiskutována.
V případě zhoršení nebo prvního výskytu jakéhokoli z těchto stavů nebo rizikových faktorů má být ženě doporučeno, aby kontaktovala svého lékaře, který stanoví, zda má užívání přípravku Nelya ukončit.
-
1. Oběhové poruchy
Riziko žilního tromboembolismu (VTE)
Užívání jakékoli kombinované hormonální antikoncepce (CHC) zvyšuje riziko žilního tromboembolismu (VTE) ve srovnání s jejím neužíváním. Přípravky, které obsahují levonorgestrel, norgestimát nebo norethisteron jsou spojovány s nejnižším rizikem VTE. Další přípravky, jako je přípravek Nelya mohou mít až dvakrát vyšší úroveň rizika. Rozhodnutí používat jakýkoli přípravek jiný než ten, který má nejnižší riziko VTE, má být učiněno po diskusi se ženou, aby se zajistilo, že rozumí riziku VTE u přípravku Nelya, rozumí, jak její současné rizikové faktory toto riziko ovlivňují a že riziko VTE je nejvyšší v prvním roce užívání léku. Existují také některé důkazy, že riziko je zvýšené, když je CHC opětovně zahájena po pauze v užívání trvající 4 týdny nebo déle.
U žen, které neužívají CHC a nejsou těhotné, se asi u 2 z 10 000 vyvine VTE v průběhu jednoho roku. U každé jednotlivé ženy však může být riziko daleko vyšší v závislosti na jejích základních rizikových faktorech (viz níže).
Odhaduje se1, že z 10 000 žen, které používají CHC obsahující gestoden se u 9 až 12 žen vyvine VTE během jednoho roku; v porovnání s přibližně 62 případy u žen, které používají CHC obsahující levonorgestrel.
V obou případech je tento počet VTE za rok menší než počet očekávaný u žen během těhotenství nebo po porodu.
VTE může být fatální v 1–2 % případů.
Počet příhod VTE na 10,000 žen za rok
Počet příhod
VTE
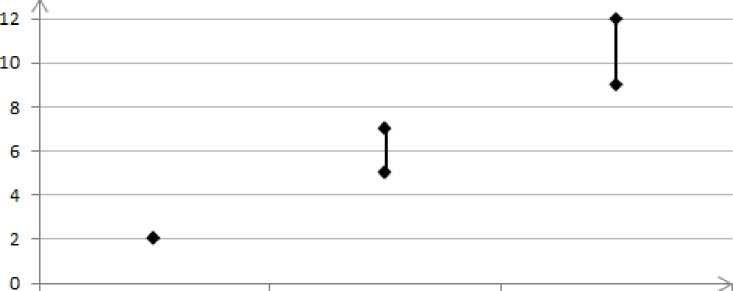
Neuživatelka CHC (2 CHC ohsáhující CHC obsahující gest oděn
příhody) levonořgestrel [5–7 příhod) [9–12 příhod)
Extrémně vzácně byla hlášena trombóza u uživatelek CHC v dalších cévách, např. jaterních, mezenterických, renálních nebo retinálních žilách a tepnách.
Riziko žilních tromboembolických komplikací u uživatelek CHC se může podstatně zvyšovat u ženy, která má další rizikové faktory, zvláště pokud je přítomno více rizikových faktorů (viz tabulka).
Přípravek Nelya je kontraindikován, pokud má žena více rizikových faktorů, které pro ni představují vysoké riziko žilní trombózy (viz bod 4.3). Pokud má žena více než jeden rizikový faktor, je možné, že zvýšení rizika je vyšší než součet jednotlivých faktorů – v tomto případě má být zváženo její celkové riziko VTE. Pokud je poměr přínosů a rizik považován za negativní, nesmí být CHC předepisována (viz bod 4.3).
Tabulka: Rizikové faktory VTE
| Rizikový faktor | Poznámka |
| Obezita (index tělesné hmotnosti nad 30 kg/m2) | Při zvýšení BMI se významně zvyšuje riziko. Zvláště důležité je zvážit, zda jsou také přítomny další rizikové faktory. |
| Prodloužená imobilizace (včetně cestování letadlem > 4 hodiny), velký chirurgický zákrok, jakýkoliv | V těchto situacích je doporučeno ukončit používání/užívání náplasti/pilulky/kroužku (v případě plánovaného chirurgického výkonu minimálně 4 týdny |
1 Tyto incidence byly odhadnuty ze souhrnu dat z epidemiologických studií s použitím relativních rizik pro různé přípravky ve srovnání s CHC obsahující levonorgestrel
2 2Střední bod rozmezí 5–7 na 10 000 WY (žen-roků) na základě relativního rizika pro CHC obsahující levonorgestrel oproti jejímu nepoužívání přibližně 2,3 až 3,6
| chirurgický zákrok na nohách a pánvi, neurochirurgický zákrok nebo větší trauma | předem) a nezahajovat užívání/používání do dvou týdnů po kompletní remobilizaci. Má se použít další antikoncepční metoda pro zabránění nechtěnému těhotenství. Antitrombotická léčba má být zvážena, pokud přípravek Nelya nebyl předem vysazen. |
| Poznámka: dočasná imobilizace, včetně cestování letadlem >4 hodiny může být také rizikovým faktorem VTE, zvláště u žen s dalšími rizikovými faktory | |
| Pozitivní rodinná anamnéza (žilní tromboembolismus kdykoli u sourozence nebo rodiče, zvláště v relativně nízkém věku např. do 50 let věku). | Pokud je suspektní hereditární predispozice, má být žena před rozhodnutím o používání jakékoli CHC odeslána k odborníkovi na konzultaci. |
| Další onemocnění související s VTE | Zhoubné onemocnění, systémový lupus erythematodes, hemolyticko- uremický syndrom, chronické zánětlivé onemocnění střev (Crohnova choroba nebo ulcerózní kolitida a srpkovitá anémie. |
| Vyšší věk | Zvláště nad 35 let |
Není žádná shoda o možné roli varixů a povrchové tromboflebitidy v nástupu nebo progresi žilní trombózy.
Zvýšené riziko tromboembolismu v těhotenství a zvláště během šestinedělí musí být zváženo (pro informaci o „Fertilitě, těhotenství a kojení “ viz bod 4.6).
V případě příznaků má být ženě doporučeno, aby vyhledala naléhavou lékařskou péči a informovala lékaře, že užívá CHC.
Příznaky hluboké žilní trombózy (DVT) mohou zahrnovat:
-
– jednostranný otok nohy a/nebo chodidla nebo podél žíly v noze;
-
– bolest nebo citlivost v noze, která může být pociťována pouze vstoje nebo při chůzi
-
– zvýšenou teplotu postižené nohy, zarudnutí nebo změnu barvy kůže nohy.
-
– náhlý nástup nevysvětlitelné dušnosti nebo rychlého dýchání;
-
– náhlý kašel, který může být spojený s hemoptýzou;
-
– ostrou bolest na hrudi;
-
– těžké točení hlavy nebo závrať způsobené světlem;
-
– rychlý nebo nepravidelný srdeční tep.
Některé z těchto příznaků (např. „dušnost“, „kašel“) nejsou specifické a mohou být nesprávně interpretovány jako častější nebo méně závažné příhody (např. infekce dýchacího traktu).
Dalšími známkami cévní okluze mohou být: náhlá bolest, otok a světle modré zbarvení končetin. Pokud nastane okluze v oku, mohou se příznaky pohybovat od nebolestivého rozmazaného vidění, které může přejít do ztráty zraku. Někdy může nastat ztráta zraku téměř okamžitě.
Epidemiologické studie spojovaly používání CHC se zvýšeným rizikem arteriálního tromboembolismu (infarkt myokardu) nebo cerebrovaskulární příhody (např. tranzitorní ischemická ataka, cévní mozková příhoda). Arteriální tromboembolické příhody mohou být fatální.
Riziko arteriálních tromboembolických komplikací nebo cerebrovaskulární příhody u uživatelek CHC se zvyšuje u žen s rizikovými faktory (viz tabulka). Přípravek Nelya je kontraindikován, pokud má žena jeden závažný rizikový faktor nebo více rizikových faktorů ATE, které pro ni představují riziko arteriální trombózy (viz bod 4.3). Pokud má žena více než jeden rizikový faktor, je možné, že zvýšení rizika je vyšší než součet jednotlivých faktorů – v tomto případě má být zváženo její celkové riziko. Pokud je poměr přínosů a rizik považován za negativní, nesmí být CHC předepisována (viz bod 4.3).
Tabulka: Rizikové faktory ATE
| Rizikový faktor | Poznámka |
| Vyšší věk | Zvláště nad 35 let |
| Kouření | Ženě má být doporučeno, aby nekouřila, pokud chce používat CHC. Ženám ve věku nad 35 let, které dále kouří, má být důrazně doporučeno, aby používaly jinou metodu antikoncepce. |
| Hypertenze | |
| Obezita (index tělesné hmotnosti nad 30 kg/m2) | Při zvýšení BMI se významně zvyšuje riziko. Zvláště důležité u žen s dalšími rizikovými faktory |
| Pozitivní rodinná anamnéza (arteriální tromboembolismus kdykoli u sourozence nebo rodiče, zvláště v relativně nízkém věku např. do 50 let věku). | Pokud je suspektní hereditární predispozice, má být žena odeslána k odborníkovi na konzultaci před rozhodnutím o používání jakékoli CHC. |
| Migréna | Zvýšení frekvence nebo závažnosti migrény během používání CHC (což může být prodromální známka cévní mozkové příhody) může být důvodem okamžitého ukončení léčby |
| Další onemocnění související s nežádoucími cévními příhodami | Diabetes mellitus, hyperhomocysteinémie, chlopenní srdeční vada a fibrilace síní, dyslipoproteinémie a systémový lupus erytematodes. |
V případě příznaků má být ženě doporučeno, aby vyhledala naléhavou lékařskou péči a informovala lékaře, že užívá CHC.
Příznaky cévní mozkové příhody mohou zahrnovat:
-
– náhlou necitlivost nebo slabost obličeje, paže nebo nohy, zvláště na jedné straně těla;
-
– náhlé potíže s chůzí, závratě, ztrátu rovnováhy nebo koordinace;
-
– náhlou zmatenost, problémy s řečí nebo porozuměním;
-
– náhlé potíže se zrakem na jednom nebo obou očích;
-
– náhlou, závažnou nebo prodlouženou bolest hlavy neznámé příčiny;
-
– ztrátu vědomí nebo omdlení s nebo bez záchvatu.
-
– bolest, nepříjemný pocit, tlak, těžkost, pocit stlačení nebo plnosti na hrudi, v paži nebo pod hrudní kostí;
-
– nepříjemný pocit vyzařující do zad, čelisti, hrdla, paže, žaludku;
-
– pocit plnosti, poruchu trávení nebo dušení;
-
– pocení, nauzeu, zvracení nebo závratě;
-
– extrémní slabost, úzkost nebo dušnost;
-
– rychlý nebo nepravidelný srdeční tep.
-
2. Tumory:
Karcinom děložního hrdla
U dlouhodobých uživatelek COC se v některých epidemiologických studiích uvádí zvýšené riziko karcinomu děložního hrdla, ale dosud není jasné, do jaké míry může být tento nález ovlivněn sexuálním chováním a dalšími faktory, jako např. lidským papilomavirem (HPV).
Karcinom prsu
Metaanalýza z 54 epidemiologických studií ukázala, že u žen aktuálně užívajících COC je mírně zvýšené relativní riziko (RR = 1,24) diagnózy karcinomu prsu. Toto zvýšené riziko během 10 let po ukončení užívání COC postupně mizí. Protože u žen do 40 let je karcinom prsu vzácný, je vyšší počet diagnóz karcinomu prsu u současných a nedávných uživatelek COC malý s ohledem na celkové riziko karcinomu prsu.
Tyto studie neposkytují důkaz kauzality. Sledovaný model zvýšeného rizika může být důsledkem časnějšího diagnostikování karcinomu prsu u uživatelek COC, biologických účinků COC nebo kombinací obojího. Karcinomy prsu diagnostikované u uživatelek COC bývají klinicky méně pokročilé než karcinomy diagnostikované u žen, které COC nikdy neužívaly.
Tumory jater
U žen užívajících COC byly hlášeny benigní a maligní tumory jater. Tyto tumory vedou v ojedinělých případech k život ohrožujícímu intraabdominálnímu krvácení. Pokud se v epigastriu objeví silná bolest, pokud je pozorována hepatomegalie nebo jsou přítomny známky intraabdominálního krvácení u žen užívajících COC, je třeba vzít v rámci diferenciální diagnostiky v úvahu tumor jater.
-
3. Další stavy
U žen s hypertriglyceridémií nebo s tímto onemocněním v rodinné anamnéze může být při užívání COC zvýšené riziko pankreatitidy.
V případě akutní nebo chronické poruchy funkce jater je třeba užívání přípravku Nelya přerušit, dokud se jaterní testy nevrátí do normálu. U pacientů s poruchou funkce jater se mohou steroidní hormony špatně metabolizovat.
Přestože byly u mnohých žen užívajících COC hlášeny mírně vyšší hodnoty krevního tlaku, klinicky významný nárůst krevního tlaku je vzácný. Pokud se během užívání COC vyvine stabilní klinická hypertenze, je třeba užívání přerušit a léčit hypertenzi. Je-li to namístě, lze v užívání COC pokračovat tehdy, je-li antihypertenzní terapií dosaženo hodnot normotenze.
Uvádí se, že jak během těhotenství, tak během užívání COC se mohou vyskytnout nebo zhoršit následující stavy, avšak jejich spojitost je neprůkazná: žloutenka a/nebo pruritus v souvislosti s cholestázou; vznik žlučových kamenů; porfyrie; systémový lupus erythematosus; hemolyticko-uremický syndrom; Sydenhamova chorea; herpes gestationis; ztráta sluchu v důsledku otosklerózy.
U žen s hereditárním angioedémem mohou přípravky obsahující estrogeny vyvolat nebo zhoršit příznaky angioedému.
Kombinovaná perorální kontraceptiva mohou mít vliv na periferní inzulínovou rezistenci a glukózovou toleranci. Diabetičky proto mají být během užívání COC přísně sledovány.
Přípravek Nelya obsahuje laktózu. Pacientky se vzácnými dědičnými problémy s intolerancí galaktózy, vrozeným deficitem laktázy nebo malabsorpcí glukózy a galaktózy, které dodržují bezlaktózovou dietu, mají s tímto množstvím počítat.
Během užívání COC bylo hlášeno zhoršování endogenní deprese, epilepsie (viz bod 4.5 Interakce), Crohnovy choroby a ulcerózní kolitidy.
Může se objevit chloasma, zejména u žen s anamnézou chloasma gravidarum. Ženy, které inklinují ke chloasmatu, se mají během užívání COC vyvarovat expozici slunečnímu světlu či ultrafialovému záření.
Účinnost perorálních kontraceptiv může být snížena v případě, že žena zapomene užít tablety, v případě těžkého průjmu nebo zvracení (viz bod 4.2) nebo souběžného užívání jiných léčivých přípravků (viz bod 4.5).
U všech kombinovaných perorálních kontraceptiv se může vyskytnout nepravidelné krvácení (špinění nebo krvácení z průniku), zvláště během prvních měsíců. Proto se má o posouzení nepravidelného krvácení uvažovat až po adaptačním období přibližně 3 cyklů.
Pokud nepravidelnosti v krvácení přetrvávají, je třeba zvážit nasazení COC s vyšším obsahem hormonů. Pokud se nepravidelnosti krvácení objeví po předchozích pravidelných cyklech, je třeba vzít v úvahu nehormonální příčiny a doporučuje se provést odpovídající diagnostická opatření k vyloučení malignity nebo těhotenství.
Během klinických studií byla u 7 % cyklů (tj. u 24 % žen v průběhu celkového trvání klinických studií) pozorována amenorea nesouvisející s těhotenstvím a 3,6 % žen mělo amenoreu v následujících po sobě jdoucích cyklech. Během klinických studií léčbu kvůli amenoree přerušilo pouze 1 % žen.
Pokud byl přípravek Nelya užíván podle doporučení a nastane amenorea, není důvod přerušovat léčbu nebo provádět těhotenský test. Pokud přípravek Nelya nebyl užíván podle doporučení, nebo se amenorea objeví po dlouhém období pravidelných cyklů, je třeba vyloučit těhotenství.
U některých žen se může vyskytnout po ukončení užívání amenorea (která může souviset s anovulačními cykly) nebo oligomenorea, zvláště pokud tento druh symptomu existoval již dříve. Tyto stavy se obyčejně vyřeší spontánně. V případě delšího trvání je třeba před dalším předepsáním přípravku provést vyšetření hypofýzy z hlediska možného onemocnění.
Před prvním zahájením nebo znovuzahájením léčby přípravkem Nelya má být získána kompletní anamnéza (včetně rodinné anamnézy) a musí být vyloučeno těhotenství. Má se změřit krevní tlak a má být provedeno tělesné vyšetření při zvážení kontraindikací (viz bod 4.3) a varování (viz bod 4.4). Je důležité, aby byla žena upozorněna na informace o žilní a arteriální trombóze, včetně rizika přípravku Nelya v porovnání s dalšími typy CHC, na příznaky VTE a ATE, známé rizikové faktory a co má dělat v případě suspektní trombózy.
Žena má být také informována, aby si pečlivě přečetla příbalovou informaci pro uživatele a aby dodržovala uvedené instrukce. Frekvence a povaha vyšetření mají být založeny na stanovených postupech a upraveny podle individuálních potřeb ženy.
Ženy mají být informovány, že perorální antikoncepce nechrání před HIV infekcí (AIDS) a dalšími sexuálně přenosnými chorobami.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Lékové interakce vedoucí ke zvýšené clearance pohlavních hormonů mohou vést ke krvácení z průniku a selhání antikoncepce. Tyto interakce byly potvrzeny u hydantoinů, barbiturátů, primidonu, karbamazepinu a rifampicinu; suspektní jsou také oxkarbazepin, topiramát, griseofulvin, felbamát a ritonavir. Mechanismus této interakce pravděpodobně spočívá v enzym-indukčních vlastnostech těchto léčivých přípravků. Maximální indukce enzymů zpravidla není patrná dříve než za 2–3 týdny po zahájení léčby, ale může přetrvávat nejméně 4 týdny po ukončení léčby.
Ženy podstupující krátkodobou léčbu kteroukoli z výše uvedených skupin nebo jednotlivými léčivými přípravky mají spolu s kontracepčními tabletami dočasně používat bariérovou metodu; tím je míněno období, kdy je užíván současně tento léčivý přípravek a kontracepční tablety, a 7 dnů po ukončení léčby léčivým přípravkem. Ženy léčené rifampicinem mají bariérovou metodu současně s kontracepčními tabletami používat po dobu, kdy jsou léčeny rifampicinem, a dalších 28 dnů po ukončení užívání rifampicinu. Pokud současné užívání jiného léčivého přípravku přesáhne počet tablet v blistru kontracepčních pilulek, má žena zahájit užívání tablet z nového blistru bez dodržení normálního intervalu, kdy tablety neužívá.
Existuje riziko galaktorey z důvodu zvýšené citlivosti prsní tkáně k prolaktinu vlivem flunarizinu.
Troleandomycin může zvýšit riziko výskytu intrahepatické cholestázy při užívání v kombinaci s COC.
U dlouhodobých uživatelek léčivých přípravků, které indukují jaterní enzymy, se doporučuje používat jiné antikoncepční metody.
Pacientky léčené přípravkem Nelya nemají souběžně užívat léčiva/přípravky alternativní medicíny obsahující Hypericum perforatum (třezalka tečkovaná), protože by mohlo dojít ke snížení kontracepčního účinku. Uvádí se případy krvácení z vysazení a nežádoucího těhotenství.
Hypericum perforatum (třezalka tečkovaná) zvyšuje indukcí enzymů množství enzymů, které metabolizují léčivé přípravky. Účinek indukce enzymů může trvat nejméně 1–2 týdny po ukončení léčby třezalkou.
Účinky COC na ostatní léčiva: Perorální kontraceptiva mohou ovlivňovat metabolismus ostatních léčiv. V souladu s tím se mohou jejich plazmatické a tkáňové koncentrace buď zvýšit (např. cyklosporin), nebo snížit (lamotrigin).
Laboratorní testy
Užívání kontracepčních steroidů může ovlivnit výsledky určitých laboratorních testů včetně biochemických parametrů funkce jater, štítné žlázy, nadledvin a ledvin; plazmatických hladin (transportních) proteinů, např. kortikosteroid vázajícího globulinu a lipidové/lipoproteinové frakce; parametrů metabolismu sacharidů a parametrů koagulace a fibrinolýzy. Změny obvykle zůstávají v rámci normálních mezí testů.
4.6 Fertilita, těhotenství a kojení
Těhotenství
V těhotenství se nesmí přípravek Nelya užívat. Pokud během užívání přípravku Nelya dojde k otěhotnění, je třeba přípravek ihned vysadit.
Rozsáhlé epidemiologické studie neodhalily zvýšené riziko vrozených vad u dětí narozených ženám, které před těhotenstvím užívaly COC, ani teratogenní účinky, pokud byla COC užívána nechtěně během těhotenství.
Kojení
Steroidní kontraceptiva mohou ovlivňovat kojení, neboť mohou snižovat množství mateřského mléka a měnit jeho složení. Malá množství steroidních kontraceptiv a/nebo jejich metabolitů mohou být vylučovaná do mateřského mléka. Proto se obecně kojícím matkám nedoporučuje užívat steroidní kontraceptiva, dokud své dítě zcela neodstaví.
Zvýšené riziko VTE během poporodního období je třeba brát v úvahu při znovuzahájení užívání přípravku Nelya (viz bod 4.2 a 4.4).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Přípravek Nelya nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje.
4.8 Nežádoucí účinky
Během užívání estrogen-progestinovými perorálními kontraceptivy byly pozorovány následující nežádoucí účinky:
Během klinických studií byla u 15 % pacientek pozorována amenorea . Mezi nejčastější (> 10 %) nežádoucí účinky, které uváděly pacientky během fáze III klinických studií a v rámci post-marketingových zkušeností s přípravkem, patřily bolesti hlavy včetně migrén a krvácení/špinění.
Popis vybraných nežádoucích účinků
U žen užívajících CHC bylo pozorováno zvýšené riziko arteriálních a žilních trombotických a tromboembolických příhod, včetně infarktu myokardu, cévní mozkové příhody, tranzitorních ischemických atak, žilní trombózy a plicní embolie a je podrobněji popsáno v bodě 4.4.
Během užívání estrogen-gestodenových perorálních kontraceptiv byly zaznamenány další nežádoucí účinky:
| Třídy orgánových systémů | Časté (> 1/100 až < 1/10) | Méně časté (> 1/1000 až < 1/100) | Vzácné (> 1/10000 až < 1/1000) | Velmi vzácné (<1/10000) |
| Infekce | Vaginitida včetně vaginální kandidózy | |||
| Poruchy imunitního systému | Anafylaktické/anafylaktoidní reakce s velmi vzácnými případy kopřivky, angioedému, vážné oběhové a respirační poruchy | |||
| Poruchy metabolismu a výživy | Zadržování vody | Změny v chuti k jídlu (zvětšení či zmenšení) | Intolerance glukózy | |
| Poruchy svalové a kosterní soustavy a pojivové tkáně | Exacerbace systémového lupus erythematosus | |||
| Psychiatrické poruchy | Změny nálad včetně deprese, změny libida, nervozita | |||
| Poruchy nervového systému | Závratě | Exacerbace chorey | ||
| Poruchy oka | Podráždění způsobené kontaktními čočkami | Zánět optického nervu, trombóza sítnicové žíly | ||
| Novotvary benigní, maligní a blíže neurčené (zahrnující cysty a polypy) | Adenom jater, hepatocelulární karcinom |
| Gastrointestinální poruchy | Nauzea, zvracení, bolest břicha | Křeče v břiše, nadýmání | Pankreatitida | |
| Poruchy jater a žlučových cest | Cholestatická žloutenka | Žlučové kameny, cholestáza* | ||
| Poruchy kůže a podkožní tkáně | Akné | Vyrážka, chloasma (melasma) s rizikem přetrvávání, hirsutismus, alopecie | Erythema nodosum | Erythema multiforme |
| Poruchy krve a lymfatického systému | Hemolyticko-uremický syndrom | |||
| Poruchy reprodukčního systému a prsu | Bolest prsou a citlivost, sekrece, dysmenorea, změny vaginální sekrece a menstruace, ektropie na děložním čipku | |||
| Celkové poruchy a reakce v místě podání | Edém | |||
| Vrozené, familiární a genetické vady | Zhoršení porfyrie | |||
| Cévní poruchy | Hypertenze | Arteriální tromboembolismus Venózní tromboembolismus | ||
| Vyšetření | Změny hmotnosti (zvýšení nebo snížení) | Změny plazmatických lipidů včetně hypertriglyceridémie |
* Estrogen-gestodenová perorální kontraceptiva mohou zhoršovat stávající žlučové kameny a cholestázu.
U žen užívajících COC jsou uváděny následující závažné nežádoucí účinky, viz body 4.3 a 4.4:
o onemocnění jater (např. tumory jater);
U uživatelek COC je velmi mírně zvýšená frekvence diagnostikování karcinomu prsu. Vzhledem k tomu, že u žen do 40 let je karcinom prsu vzácný, je počet těchto příhod s ohledem na celkové riziko karcinomu prsu malý. Příčinnost ve spojení s užíváním COC není známa. Další informace jsou uvedeny v bodě 4.3 a
-
4.4.
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
Webové stránky:
4.9 Předávkování
Po požití vysokých dávek estrogen-progestinových kontraceptiv nebyly pozorovány žádné závažné nežádoucí účinky. Obecné zkušenosti s estrogen-progestinovými perorálními kontraceptivy ukazují, že mezi symptomy, které se v takových případech mohou vyskytnout, patří následující: nauzea, zvracení a u mladých žen slabé vaginální krvácení.
Antidotum neexistuje, léčba má být čistě symptomatická.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1. Farmakodynamické vlastnosti
GESTAGENY A ESTROGENY, FIXNÍ KOMBINACE
(pohlavní hormony a léky ovlivňující močopohlavní systém)
ATC kód: G03AA10.
Monofázická estrogen-progestinová kombinace
Celkový index Pearlové: 0,24 (21 521 cyklů)
Antikoncepční účinek kontracepčních pilulek spočívá v interakci nejrůznějších faktorů, z nichž nejdůležitější jsou inhibice ovulace a změny na endometriu. Spolu s ochranou proti otěhotnění mají kombinovaná perorální kontraceptiva několik pozitivních vlastností, které mohou být vedle negativních vlastností (viz bod 4.4 a 4.8 Upozornění, Nežádoucí účinky) užitečné při rozhodování o metodě plánovaného rodičovství. Menstruační cyklus je pravidelnější, menstruace je často méně bolestivá a krvácení je mírnější. Poslední zmiňovaná vlastnost může vést ke snížení výskytu deficience železa.
5.2. Farmakokinetické vlastnosti
Ethinylestradiol
Při perorálním dávkování se ethinylestradiol rychle a zcela vstřebává. Po užití dávky obsahující 15 ^g je vrcholových plazmatických koncentrací 30 pg/ml dosahováno do 1 až 1,5 hodiny. Ethinylestradiol významně podléhá efektu prvního průchodu játry, přičemž existují velké interindividuální odchylky. Absolutní biologická dostupnost je přibližně 45 %.
Zdánlivý distribuční objem ethinylestradiolu je 15 l/kg a vazba na plazmatické proteiny je přibližně 98 %. Ethinylestradiol indukuje jaterní syntézu SHBG a CBG. Během léčby za užití 15 ^g ethinylestradiolu se plazmatická koncentrace SHBG zvyšuje z 86 na přibližně 200 nmol/l.
Ethinylestradiol se zcela metabolizuje (plazmatická clearance metabolitů je přibližně 10 ml/min/kg).
Metabolity jsou vylučovány močí (40 %) a stolicí (60 %).
Poločas vylučování ethinylestradiolu je přibližně 15 hodin. Pouze malá část ethinylestradiolu je vylučována v nezměněné podobě. Metabolity ethinylestradiolu jsou vylučovány močí a žlučí v poměru 4 : 6.
Rovnovážného stavu je dosahováno během druhé poloviny léčebného cyklu a sérové hladiny dosahují faktoru akumulace od 1,4 do 2,1.
Gestoden
Při perorálním dávkování se gestoden rychle a zcela vstřebává. Absolutní biologická dostupnost je přibližně 100 %. Po podání jediné dávky 60 ^g je vrcholových plazmatických koncentrací 2 ng/ml dosahováno přibližně do 1 hodiny. Plazmatické koncentrace silně závisejí na koncentracích SHBG.
Zdánlivý distribuční objem je 1,4 l/kg po jediné dávce 60 ^g. Gestoden se z 30 % váže na plazmatický albumin a z 50 až 70 % na SHBG.
Gestoden se zcela metabolizuje. Metabolická clearance je přibližně 0,8 ml/min/kg po jediné dávce 60 ^g. Neaktivní metabolity jsou vylučovány močí (60 %) a stolicí (40 %).
Zdánlivý poločas vylučování je přibližně 13 hodin. Pokud je gestoden podáván spolu s ethinylestradiolem, prodlužuje se na 20 hodin.
Po opakovaném podání kombinace gestodenu a ethinylestradiolu se plazmatické koncentrace zvýší přibližně 2– až 4 násobně.
5.3 Předklinické údaje vztahující se k bezpečnosti
Ethinylestradiol a gestoden nejsou genotoxické. Studie karcinogenity se samostatným ethinylestradiolem nebo v kombinaci s nejrůznějšími gestageny neprokazují žádné konkrétní karcinogenní riziko pro ženy při užívání dle indikací pro antikoncepci. Je však nutno mít na paměti, že pohlavní hormony mohou zrychlovat růst určitých hormon-dependentních tkání a tumorů.
Studie reprodukční toxicity na plodnost, vývoj plodu nebo schopnost reprodukce se samostatným ethinylestradiolem nebo v kombinaci s gestageny neprokázaly žádné nežádoucí účinky na lidi při užívání dle doporučení.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Žlutá potahovaná tableta (aktivní):
Jádro:
monohydrát laktózy, mikrokrystalická celulóza, draselná sůl polakrilinu, magnesium-stearát
Potahová vrstva:
Suchá potahová soustava 024.15 MS žlutá: hypromelosa, hyprolosa, mastek, hydrogenovaný bavlníkový olej, oxid titaničitý (E 171), žlutý oxid železitý (E 172)
Bílá tableta (placebo):
Starlac (monohydrát laktózy, kukuřičný škrob), magnesium-stearát
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
3 roky
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
6.5 Druh obalu a obsah balení
24 žlutých potahovaných tablet a 4 bílé tablety v blistru (PVC/aluminium); krabička obsahuje 1 blistr.
24 žlutých potahovaných tablet a 4 bílé tablety v blistru (PVC/aluminium); krabička obsahuje 3 blistry.
24 žlutých potahovaných tablet a 4 bílé tablety v blistru (PVC/aluminium); krabička obsahuje 6 blistrů.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Heaton k.s.
Na Pankráci 14
140 00 Praha 4
Česká republika
8. REGISTRAČNÍ ČÍSLO(A)
17/123/10-C
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
5. 5. 2010 / 2. 5. 2017
Další informace o léčivu NELYA
Jak
se NELYA
podává: perorální podání - potahovaná tableta
Výdej
léku: na lékařský předpis
Balení: Blistr
Velikost
balení: 3X28(24+4)
Držitel rozhodnutí o registraci daného léku v České republice:
Heaton k.s., Praha
E-mail: safety@heaton.cz
Telefon: 242 482 690
