Souhrnné informace o léku - KATYA
1. NÁZEV PŘÍPRAVKU
Katya 0,030 mg/0,075 mg obalené tablety
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Léčivé látky:
Jedna obalená tableta obsahuje ethinylestradiolum 0,030 mg a gestodenum 0,075 mg.
Pomocné látky se známým účinkem:
Monohydrát laktosy 38mg, sacharosa 20mg
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Obalená tableta
Bílé kulaté bikonvexní obalené tablety bez značení.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Perorální kontracepce.
Rozhodnutí předepsat přípravek Katya by mělo být provedeno po zvážení jednotlivých současných rizikových faktorů ženy, zvláště rizikových faktorů pro žilní tromboembolismus (VTE), a toho, jaké je riziko VTE u přípravku Katya v porovnání s dalšími přípravky CHC (viz body 4.3 a 4.4).
4.2 Dávkování a způsob podání
Jak užívat přípravek Katya
Tablety se užívají v naznačeném pořadí každý den přibližně ve stejnou dobu. Během 21 po sobě následujících dnů se užívá jedna tableta denně. Užívání z nového balení začíná po sedmidenním intervalu bez užívání tablet, během kterého dojde ke krvácení z vysazení, které se objeví zhruba za 2–3 dny po užití poslední tablety a nemusí být ukončeno před zahájením užívání z dalšího balení.
Jak zahájit užívání přípravku Katya
Nepředcházelo-li užívání hormonální kontracepce (v předchozím měsíci)
Užívání tablet se zahájí první den přirozeného cyklu ženy (tzn. první den jejího menstruačního krvácení). Zahájit lze i během 2.-5. dne, ale doporučuje se použít navíc během prvních 7 dnů prvního cyklu bariérovou metodu kontracepce.
Přechod z jiného kombinovaného perorálního kontraceptiva (COC)
Žena by měla zahájit užívání přípravku Katya nejlépe hned následující den po užití poslední aktivní tablety předchozího kombinovaného perorálního kontraceptiva, nejpozději však v den následujícím po obvyklém intervalu bez užívání tablet nebo po období užívání placebo-tablet předchozího kontraceptiva.
Přechod z kontracepční metody obsahující pouze progestagen (minipilulka, injekce, implantát nebo z nitroděložního systému uvolňujícího progestagen (IUS))
Žena může být převedena z minipilulky kdykoliv. První tableta musí být užita den po užití jakékoli minipilulky. Při přechodu z implantátu nebo z IUS musí být Katya užita v den jeho vyjmutí, při přechodu z injekcí v den, kdy by měla být aplikována další injekce. Ve všech těchto případech je třeba doporučit použít navíc po dobu prvních 7 dnů užívání tablet bariérovou metodu kontracepce.
Užívání po potratu v prvním trimestru
Žena může zahájit užívání okamžitě. Pokud tak učiní, nepotřebuje další kontracepční opatření.
Užívání po porodu nebo po potratu ve druhém trimestru
Kojící ženy viz bod 4.6.
Ženě je třeba doporučit, aby zahájila užívání mezi 21. až 28. dnem po porodu u nekojících žen nebo po potratu ve druhém trimestru. Pokud zahájí užívání později, je třeba doporučit, aby použila navíc bariérovou metodu kontracepce po dobu prvních 7 dnů užívání tablet. Pokud však již předtím došlo k pohlavnímu styku, je třeba před skutečným zahájením užívání vyloučit těhotenství nebo musí žena vyčkat na první menstruační krvácení.
Postup při vynechání tablet
Pokud se užití tablety opozdí o méně než 12 hodin, není kontracepční ochrana narušena. Žena musí užít tabletu okamžitě, jakmile si chybu uvědomí a další tabletu pak užije v obvyklou dobu.
Je-li užití tablety opožděno o více než 12 hodin, kontracepční ochrana může být snížena. Další opatření se pak mohou řídit následujícími základními pravidly:
1. Užívání tablet nesmí být nikdy přerušeno na dobu delší než 7 dnů.
2. K dosažení odpovídající suprese hypothalamo-hypofyzo-ovariální osy je třeba 7 dnů nepřerušeného užívání tablet.
V souladu s těmito pravidly lze v běžné praxi poskytnout následující doporučení:
- 1. týden
Uživatelka musí užít poslední vynechanou tabletu okamžitě, jakmile si chybu uvědomí, i kdyby to znamenalo užití dvou tablet současně. Poté pokračuje v užívání tablet v obvyklou dobu. Navíc je třeba používat v následujících 7 dnech bariérovou metodu kontracepce jako např. kondom. Pokud došlo v předchozích 7 dnech k pohlavnímu styku, je třeba uvážit možnost otěhotnění. Čím více tablet bylo vynecháno a čím blíže byly tyto tablety k pravidelnému intervalu bez užívání, tím větší je riziko otěhotnění.
- 2. týden
Uživatelka musí užít poslední vynechanou tabletu okamžitě, jakmile si chybu uvědomí, i kdyby to znamenalo užití dvou tablet současně. Poté pokračuje v užívání tablet v obvyklou dobu. Pokud žena užívala tablety pravidelně po dobu 7 dnů před první vynechanou tabletou, další kontracepční opatření nejsou nutná. Není-li tomu tak, nebo vynechala-li žena více než 1 tabletu, je třeba doporučit zvláštní kontracepční opatření po dobu 7 dnů.
- 3. týden
Vzhledem k nadcházejícímu intervalu bez užívání tablet je velké nebezpečí snížení spolehlivosti kontracepce. Přesto však upravením schématu užívání lze předejít snížení kontracepční ochrany. Bude-li se pacientka řídit některým z následujících dvou možných postupů, není třeba používat další kontracepční opatření za předpokladu, že po dobu 7 dnů předcházejících vynechání první tablety užila všechny tablety správně. Není-li tomu tak, žena musí zvolit první z následujících dvou možností a použít navíc další kontracepční opatření po dobu 7 dnů.
1. Uživatelka musí užít poslední vynechanou tabletu okamžitě, jakmile si chybu uvědomí, i kdyby to znamenalo užití dvou tablet současně. Poté pokračuje v užívání tablet v obvyklou dobu. Užívání z následujícího balení pak zahájí okamžitě po využívání předchozího, tzn. že mezi baleními není žádná přestávka. Krvácení z vysazení se pravděpodobně dostaví až po využívání druhého balení, ale během užívání tablet může dojít ke špinění nebo krvácení z vysazení.
2. Ženě lze také poradit, aby přerušila užívání tablet ze stávajícího balení. Tím vznikne interval 7 dnů bez užívání tablet včetně dnů, kdy byly tablety vynechány a následuje užívání z dalšího balení.
Pokud žena zapomene užít tablety a následně se nedostaví krvácení z vysazení v prvním normálním intervalu bez užívání tablet, je třeba zvážit možnost těhotenství.
Postup v případě zvracení/průjmu
Dojde-li během 3–4 hodin po užití tablety ke zvracení, nemusí dojít k úplnému vstřebání a lze aplikovat postup při vynechání tablety uvedený výše. Pokud není průjem extrémně silný, absorpci neovlivní, a proto není nutné užívat doplňkovou antikoncepci. Pokud silný průjem trvá 2 a více dnů, musí být aplikován postup při vynechání tablety.
Nechce-li žena měnit obvyklé schéma užívání tablet, musí užít zvláštní tabletu(y) z jiného balení.
Jak posunout nebo oddálit krvácení
Přeje-li si žena oddálit krvácení, musí pokračovat v užívání tablet z dalšího balení přípravku Katya bez obvyklé přestávky bez užívání tablet. Tak lze pokračovat podle potřeby až do využívání druhého balení, ne déle. Během této doby může žena pozorovat krvácení z vysazení nebo špinění. Po sedmidenním intervalu bez užívání tablet pak žena opět pokračuje v pravidelném užívání přípravku Katya.
Přeje-li si žena přesunout periodu na jiný den v týdnu, než na který vychází ve stávajícím schématu užívání, lze jí doporučit, aby zkrátila nastávající interval bez užívání tablet o tolik dnů, o kolik si přeje. Čím kratší bude interval, tím větší je riziko, že nedojde ke krvácení z vysazení, ale že bude docházet během užívání z následujícího balení ke krvácení z průniku nebo špinění (podobně jako při oddálení periody).
4.3 Kontraindikace
Kombinovaná hormonální antikoncepce (CHC) by se neměla používat u následujících stavů. Pokud se některý z těchto stavů objeví poprvé v průběhu užívání kombinovaného hormonálního kontraceptiva, užívání přípravku je třeba okamžitě ukončit.
- Přítomnost nebo riziko žilního tromboembolismu (VTE)
- Přítomnost nebo riziko arteriálního tromboembolismu (ATE)
- diabetes mellitus s cévními příznaky;
- závažná hypertenze;
- závažná dyslipoproteinémie
- Přítomnost pohlavními steroidy ovlivnitelných malignit (pohlavních orgánů nebo prsů) nebo podezření na ně
- Těžké jaterní onemocnění právě probíhající nebo v anamnéze až do navrácení hodnot jaterních funkcí k normálu
- Existující benigní nebo maligní jaterní tumory nebo jejich výskyt v anamnéze
- Vaginální krvácení s nediagnostikovanou příčinou
- Hypersenzitivita na léčivé látky nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
Pokud jsou přítomna jakákoli onemocnění nebo rizikové faktory uvedené níže, měla by být vhodnost přípravku Katya s ženou prodiskutována.
V případě zhoršení nebo prvního výskytu jakéhokoli z těchto stavů nebo rizikových faktorů by mělo být ženě doporučeno, aby kontaktovala svého lékaře, který stanoví, zda by měla užívání přípravku Katya ukončit.
-
1. Cirkulační poruchy
Riziko žilního tromboembolismu (VTE)
Užívání jakékoli kombinované hormonální antikoncepce (CHC) zvyšuje riziko žilního tromboembolismu (VTE) ve srovnání s jejím neužíváním. Přípravky, které obsahují levonorgestrel, norgestimát nebo norethisteron jsou spojovány s nejnižším rizikem VTE. Další přípravky, jako je přípravek Katya mohou mít až dvakrát vyšší úroveň rizika. Rozhodnutí používat jakýkoli přípravek jiný než ten, který má nejnižší riziko VTE, by mělo být učiněno po diskusi se ženou, aby se zajistilo, že rozumí riziku VTE u přípravku Katya, rozumí, jak její současné rizikové faktory toto riziko ovlivňují a že riziko VTE je nejvyšší v prvním roce užívání léku. Existují také některé důkazy, že riziko je zvýšené, když je CHC opětovně zahájena po pauze v užívání trvající 4 týdny nebo déle.
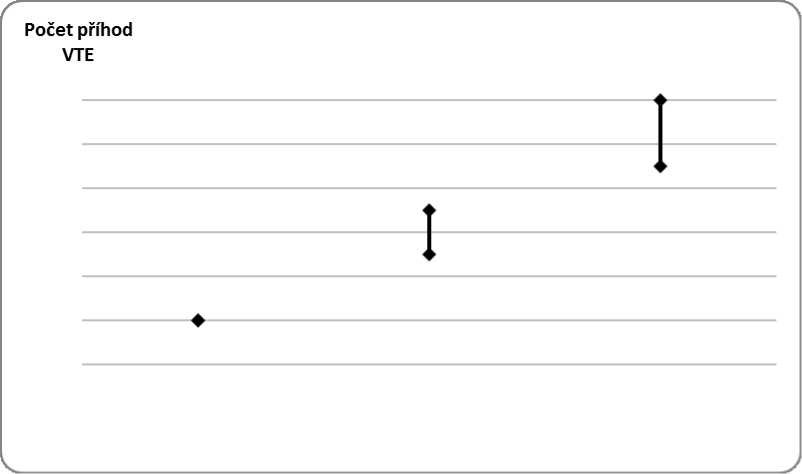
U žen, které neužívají CHC a nejsou těhotné, se asi u 2 z 10 000 vyvine VTE v průběhu jednoho roku. U každé jednotlivé ženy však může být riziko daleko vyšší v závislosti na jejích základních rizikových faktorech (viz níže).
Odhaduje se, že z 10 000 žen, které používají CHC obsahující gestoden se u 9 až 12 žen vyvine VTE během jednoho roku; v porovnání s přibližně 6 případy u žen, které používají CHC obsahující levonorgestrel.
V obou případech je tento počet VTE za rok menší než počet očekávaný u žen během těhotenství nebo po porodu.
VTE může být fatální v 1–2 % případů.
Počet příhod VTE na 10,000 žen za rok
Extrémně vzácně byla hlášena trombóza u uživatelek CHC v dalších cévách, např. jaterních, mezenterických, renálních nebo retinálních žilách a tepnách.
Riziko žilních tromboembolických komplikací u uživatelek CHC se může podstatně zvyšovat u ženy, která má další rizikové faktory, zvláště pokud je přítomno více rizikových faktorů (viz tabulka).
Přípravek Katya je kontraindikován, pokud má žena více rizikových faktorů, které pro ni představují vysoké riziko žilní trombózy (viz bod 4.3). Pokud má žena více než jeden rizikový faktor, je možné, že zvýšení rizika je vyšší než součet jednotlivých faktorů – v tomto případě by mělo být zváženo její celkové riziko VTE. Pokud je poměr přínosů a rizik považován za negativní, neměla by být CHC předepisována (viz bod 4.3).
Tabulka: Rizikové faktory VTE
| Rizikový faktor | Poznámka |
| Obezita (index tělesné hmotnosti nad 30 kg/m2) | Při zvýšení BMI se významně zvyšuje riziko. Zvláště důležité je zvážit, zda jsou také přítomny další rizikové faktory. |
| Prodloužená imobilizace, velký chirurgický zákrok, jakýkoliv chirurgický zákrok, na nohách a pánvi, neurochirurgický zákrok nebo větší trauma | V těchto situacích je doporučeno ukončit používání/užívání náplasti/pilulky/kroužku (v případě plánovaného chirurgického výkonu minimálně 4 týdny předem) a nezahajovat užívání/používání do dvou týdnů po kompletní remobilizaci. Měla by se použít další antikoncepční metoda pro zabránění nechtěnému těhotenství. Antitrombotická léčba by měla být zvážena, pokud přípravek Katya nebyl předem vysazen. |
| Poznámka: dočasná imobilizace, včetně cestování letadlem >4 hodiny může být také rizikovým faktorem VTE, zvláště u žen s dalšími |
| rizikovými faktory | |
| Pozitivní rodinná anamnéza (žilní tromboembolismus kdykoli u sourozence nebo rodiče, zvláště v relativně nízkém věku např. do 50 let věku). | Pokud je suspektní hereditární predispozice, měla by být žena před rozhodnutím o používání jakékoli CHC odeslána k odborníkovi na konzultaci. |
| Další onemocnění související s VTE | Zhoubné onemocnění, systémový lupus erythematodes, hemolyticko- uremický syndrom, chronické zánětlivé onemocnění střev (Crohnova choroba nebo ulcerózní kolitida a srpkovitá anémie. |
| Vyšší věk | Zvláště nad 35 let |
Není žádná shoda o možné roli varixů a povrchové tromboflebitidy v nástupu nebo progresi žilní trombózy.
Zvýšené riziko tromboembolismu v těhotenství a zvláště během šestinedělí musí být zváženo (pro informaci o „Těhotenství a kojení “ viz bod 4.6).
V případě příznaků by mělo být ženě doporučeno, aby vyhledala naléhavou lékařskou péči a informovala lékaře, že užívá CHC.
Příznaky hluboké žilní trombózy (DVT) mohou zahrnovat:
-
– jednostranný otok nohy a/nebo chodidla nebo podél žíly v noze;
-
– bolest nebo citlivost v noze, která může být pociťována pouze vstoje nebo při chůzi
-
– zvýšenou teplotu postižené nohy, zarudnutí nebo změnu barvy kůže nohy.
-
– náhlý nástup nevysvětlitelné dušnosti nebo rychlého dýchání;
-
– náhlý kašel, který může být spojený s hemoptýzou;
-
– ostrou bolest na hrudi;
-
– těžké točení hlavy nebo závrať způsobené světlem;
-
– rychlý nebo nepravidelný srdeční tep.
Některé z těchto příznaků (např. „dušnost“, „kašel“) nejsou specifické a mohou být nesprávně interpretovány jako častější nebo méně závažné příhody (např. infekce dýchacího traktu).
Dalšími známkami cévní okluze mohou být: náhlá bolest, otok a světle modré zbarvení končetin. Pokud nastane okluze v oku, mohou se příznaky pohybovat od nebolestivého rozmazaného vidění, které může přejít do ztráty zraku. Někdy může nastat ztráta zraku téměř okamžitě.
Epidemiologické studie spojovaly používání CHC se zvýšeným rizikem arteriálního tromboembolismu (infarkt myokardu) nebo cerebrovaskulární příhody (např. tranzitorní ischemická ataka, cévní mozková příhoda). Arteriální tromboembolické příhody mohou být fatální.
Riziko arteriálních tromboembolických komplikací nebo cerebrovaskulární příhody u uživatelek CHC se zvyšuje u žen s rizikovými faktory (viz tabulka). Přípravek Katya je kontraindikován, pokud má žena jeden závažný rizikový faktor nebo více rizikových faktorů ATE, které pro ni představují riziko arteriální trombózy (viz bod 4.3). Pokud má žena více než jeden rizikový faktor, je možné, že zvýšení rizika je vyšší než součet jednotlivých faktorů – v tomto případě by mělo být zváženo její celkové riziko. Pokud je poměr přínosů a rizik považován za negativní, neměla by být CHC předepisována (viz bod 4.3).
Tabulka: Rizikové faktory ATE
| Rizikový faktor | Poznámka |
| Vyšší věk | Zvláště nad 35 let |
| Kouření | Ženě by mělo být doporučeno, aby nekouřila, pokud chce používat CHC. Ženám ve věku nad 35 let, které dále kouří, by mělo být důrazně doporučeno, aby používaly jinou metodu antikoncepce. |
| Hypertenze | |
| Obezita (index tělesné hmotnosti nad 30 kg/m2) | Při zvýšení BMI se významně zvyšuje riziko. Zvláště důležité u žen s dalšími rizikovými faktory |
| Pozitivní rodinná anamnéza (arteriální tromboembolismus kdykoli u sourozence nebo rodiče, zvláště v relativně nízkém věku např. do 50 let věku). | Pokud je suspektní hereditární predispozice, měla by být žena odeslána k odborníkovi na konzultaci před rozhodnutím o používání jakékoli CHC. |
| Migréna | Zvýšení frekvence nebo závažnosti migrény během používání CHC (což může být prodromální známka cévní mozkové příhody) může být důvodem okamžitého ukončení léčby |
| Další onemocnění související s nežádoucími cévními příhodami | Diabetes mellitus, hyperhomocysteinémie, chlopenní srdeční vada a fibrilace síní, dyslipoproteinémie a systémový lupus erytematodes. |
-
V případě příznaků by mělo být ženě doporučeno, aby vyhledala naléhavou lékařskou péči a informovala lékaře, že užívá CHC.
Příznaky cévní mozkové příhody mohou zahrnovat:
-
– náhlou necitlivost nebo slabost obličeje, paže nebo nohy, zvláště na jedné straně těla;
-
– náhlé potíže s chůzí, závratě, ztrátu rovnováhy nebo koordinace;
-
– náhlou zmatenost, problémy s řečí nebo porozuměním;
-
– náhlé potíže se zrakem na jednom nebo obou očích;
-
– náhlou, závažnou nebo prodlouženou bolest hlavy neznámé příčiny;
-
– ztrátu vědomí nebo omdlení s nebo bez záchvatu.
-
– bolest, nepříjemný pocit, tlak, těžkost, pocit stlačení nebo plnosti na hrudi, v paži nebo pod hrudní kostí;
-
– nepříjemný pocit vyzařující do zad, čelisti, hrdla, paže, žaludku;
-
– pocit plnosti, poruchu trávení nebo dušení;
-
– pocení, nauzeu, zvracení nebo závratě;
-
– extrémní slabost, úzkost nebo dušnost;
-
– rychlý nebo nepravidelný srdeční tep.
-
2. Nádory
Karcinom děložního hrdla
-
V některých epidemiologických studiích bylo zaznamenáno zvýšené riziko karcinomu děložního hrdla při dlouhodobém užívání kombinovaných perorálních kontraceptiv (COC). Dosud však stále pokračují spory o tom, do jaké míry lze tento výsledek vztahovat k sexuálnímu chování a k dalším faktorům, jako je lidský papilloma virus (HPV).
Karcinom prsu
Meta-analýza z 54 epidemiologických studií hovoří o lehce zvýšeném relativním riziku (RR = 1,24) diagnózy karcinomu prsu u žen, které právě užívají COC. Toto zvýšené riziko postupně klesá během 10 let po ukončení užívání COC. Vzhledem k tomu, že karcinom prsu je vzácný u žen do 40 let, zvýšení počtu diagnostikovaných karcinomů prsu u současných a dřívějších uživatelek COC je malé ve vztahu k celkovému riziku karcinomu prsu.
Tyto studie neposkytují důkaz kauzality. Příčinou pozorovaného zvýšení rizika karcinomu prsu u uživatelek COC může být časnější diagnóza, biologický účinek COC nebo kombinace obojího.
Karcinom prsu diagnostikovaný u současných nebo minulých uživatelek bývá klinicky méně pokročilý než u žen, které COC nikdy nepoužívaly.
Karcinomy jater
-
V ojedinělých případech byly u uživatelek COC diagnostikovány benigní a maligní jaterní tumory. Vzácně byly tyto tumory příčinou život ohrožujícího nitrobřišního krvácení. Objeví-li se silná bolest v nadbřišku, zvětšení jater nebo známky nitrobřišního krvácení u ženy užívající COC, je třeba v diferenciální diagnóze vzít v úvahu možnost hepatálního tumoru.
-
3. Ostatní stavy
U žen, které trpí hypertriglyceridemií, nebo které mají toto onemocnění v rodinné anamnéze, může být v průběhu užívání kombinovaných perorálních kontraceptiv (COC) zvýšené riziko pankreatitidy.
-
V případě akutní nebo chronické poruchy funkce jater musí být užívání Katya zastaveno dokud se jaterní funkční testy nevrátí k normálu. Steroidní hormony mohou být pacientkami s poruchou funkce jater špatně metabolizovány.
Během klinických studií u pacientek léčených pro virovou hepatitidu typu C (HCV) léčivými přípravky obsahujícími ombitasvir/paritaprevir/ritonavir a dasabuvir s ribavirinem nebo bez ribavirinu, došlo k zvýšení aminotransferázy (ALT) na více než pětinásobek horní hranice normálních hodnot (ULN) výrazně častěji u žen, které užívaly léčivé přípravky obsahující ethinylestradiol, jako je kombinovaná hormonální antikoncepce (CHC) (viz body 4.3 a 4.5).
Účinnost kombinovaných perorálních kontraceptiv může být snížena např. při vynechání tablety, v případě závažného průjmu nebo zvracení (viz bod 4.2), nebo při současném užívání dalších léčivých přípravků (viz bod 4.5).
Při užívání kteréhokoliv kombinovaného perorálního kontraceptiva (COC) se může objevit nepravidelné krvácení (špinění nebo krvácení z průniku), a to především během prvních měsíců užívání. Z toho důvodu má hledání příčiny nepravidelného krvácení smysl až po adaptačním intervalu přibližně tří cyklů.
Pokud nepravidelné krvácení pokračuje je potřeba uvážit užívání přípravku s vyšším obsahem hormonů. Pokud se krvácení objeví po období pravidelných cyklů, pak je třeba uvážit možnost nehormonální příčiny a provést odpovídající diagnostické kroky k vyloučení malignity nebo těhotenství.
U některých žen nemusí dojít během intervalu bez užívání tablet ke krvácení z vysazení. Jsou-li tablety užívány podle pokynů popsaných v bodě 4.2, je nepravděpodobné, že je žena těhotná. Pokud však tablety nebyly užívány před prvním vynechaným krvácením pravidelně nebo nedošlo-li ke krvácení z vysazení dvakrát, je třeba před dalším užíváním COC vyloučit těhotenství.
Před prvním zahájením nebo znovuzahájením léčby přípravkem Katya by měla být získána kompletní anamnéza (včetně rodinné anamnézy) a musí být vyloučeno těhotenství. Měl by se změřit krevní tlak a mělo by být provedeno tělesné vyšetření při zvážení kontraindikací (viz bod 4.3) a varování (viz bod 4.4). Je důležité, aby byla žena upozorněna na informace o žilní a arteriální trombóze, včetně rizika přípravku Katya v porovnání s dalšími typy CHC, na příznaky VTE a ATE, známé rizikové faktory a co by měla dělat v případě suspektní trombózy.
Žena by také měla být informována, aby si pečlivě přečetla příbalovou informaci pro uživatele a aby dodržovala uvedené instrukce. Frekvence a povaha vyšetření by měly být založeny na stanovených postupech a upraveny podle individuálních potřeb ženy.
Ženy by měly být informovány, že hormonální antikoncepce nechrání před HIV infekcí (AIDS) a dalšími sexuálně přenosnými chorobami.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Interakce zvyšující clearance pohlavních hormonů mohou vést ke krvácení z průniku a/nebo k selhání kontracepce. To bylo pozorováno u hydantoinů, barbiturátů, primidonu, karbamazepinu, rifampicinu, oxkarbamazepinu, topiramátu, griseofulvinu, felbamátu a ritonaviru. Mechanizmus této interakce je v indukci jaterních enzymů těchto látek. Maximální enzymová indukce je obvykle pozorována až za 2 –3 týdny po zahájení léčby, ale může přetrvávat ještě 4 týdny po ukončení léčby.
Ženy krátkodobě léčené některým z těchto výše uvedených léčivých látek by měly dočasně používat bariérovou metodu kontracepce navíc k perorálnímu kombinovanému kontraceptivu (COC), to znamená po dobu, kdy současně užívají antikoncepci a léčivý přípravek a ještě 7 dnů po ukončení užívání některého z výše uvedených léčivých přípravků. Ženy léčené rifampicinem musí užívat bariérovou antikoncepci ještě 28 dnů po ukončení jeho léčby. Pokud léčba zasáhne do období ukončení užívání tablet COC ze stávajícího balení, pak by další balení COC mělo být načato bez obvyklého intervalu bez užívání tablet.
Při dlouhodobé léčbě induktory jaterních enzymů je vhodné navrhnout jiný způsob antikoncepce.
Ženy užívající Katya nesmí současně užívat produkty alternativní medicíny obsahující třezalku tečkovanou (Hypericum perforatum), jelikož může snížit antikoncepční účinek. Bylo hlášeno vynechání menstruace a nechtěné těhotenství.
Třezalka tečkovaná zvyšuje pomocí enzymové indukce množství enzymů, které přípravek metabolizují. Výsledek enzymové indukce může přetrvávat ještě 1 – 2 týdny po ukončení užívání třezalky.
Perorální kontraceptiva mohou interferovat s metabolismem ostatních léků. Tudíž plasmatické a tkáňové koncentrace mohou být zvýšeny (např. cyklosporinem) nebo sníženy (lamotriginem).
Laboratorní vyšetření
Užívání kontracepčních steroidů může ovlivnit výsledky některých laboratorních testů, včetně biochemických parametrů jaterních, thyreoidálních, adrenálních a renálních funkcí, plasmatických hladin proteinů (vazebných) např. corticosteroid binding globulin a lipid/ lipoproteinové frakce, parametry metabolismu uhlovodanů a parametry koagulace a fibrinolýzy. Změny však obvykle zůstávají v rozmezí normálních laboratorních hodnot.
Farmakodynamické interakce
Současné podávání s léčivými přípravky obsahujícími ombitasvir/paritaprevir/ritonavir a dasabuvir, s ribavirinem nebo bez ribavirinu, může zvýšit riziko zvýšení ALT (viz body 4.3 a 4.4). Proto je třeba uživatelky přípravku Katya před zahájením léčby tímto kombinovaným léčebným režimem převést na alternativní metodu kontracepce (např. kontracepci obsahující jen progestagen nebo nehormonální metody kontracepce). Přípravek Katya je možné znovu začít užívat 2 týdny po ukončení léčby tímto kombinovaným léčebným režimem.
4.6 Těhotenství a kojení
Katya je kontraindikovaná během těhotenství. Pokud během užívání přípravku Katya dojde k těhotenství, další užívání musí být okamžitě ukončeno.
Rozsáhlé epidemiologické studie však nezaznamenaly zvýšené riziko vrozených vad u dětí narozených ženám užívajícím kombinovaná perorální kontraceptiva před otěhotněním, ani teratogenní vliv kombinovaných perorálních kontraceptiv nezáměrně užívaných v těhotenství.
Laktace může být ovlivněna kombinovanými perorálními kontraceptivy, která mohou snižovat množství a měnit složení mateřského mléka. Malá množství kontracepčních steroidů a/nebo jejich metabolitů mohou být vylučována do mateřského mléka. Proto se obecně kojícím matkám nedoporučuje užívat steroidní kontraceptiva, dokud své dítě zcela neodstaví.
Zvýšené riziko VTE během poporodního období je třeba brát v úvahu při znovuzahájení užívání přípravku Katya (viz bod 4.2 a 4.4).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Přípravek Katya nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje.
4.8 Nežádoucí účinky
Nejčastějšími nežádoucími účinky jsou nepravidelné krvácení, nauzea, zvýšení tělesné hmotnosti, citlivost prsu a bolest hlavy. Obvykle se objevují na počátku léčby a jsou přechodné.
Popis vybraných nežádoucích účinků
U žen užívajících CHC bylo pozorováno zvýšené riziko arteriálních a žilních trombotických a tromboembolických příhod, včetně infarktu myokardu, cévní mozkové příhody, tranzitorních ischemických atak, žilní trombózy a plicní embolie a je podrobněji popsáno v bodě 4.4.
| Třídy orgánových systémů | Časté (>1/100 až <1/10) | Méně časté (>1/1000 až <1/100) | Vzácné (>1/10 000 až <1/1000) | Velmi vzácné (<1/10 000) |
| Poruchy nervového systému | Bolesti hlavy Nervozita | |||
| Poruchy oka | Podráždění očí při nošení kontaktních čoček Poruchy vidění | |||
| Poruchy ucha a labyrintu | Otoskleróza | |||
| Gastrointestinální poruchy | Nauzea | Zvracení | Cholelitiáza | Pancreatitis |
| Poruchy kůže a podkožní tkáně | Akné | Chloasma | ||
| Poruchy metabolismu a výživy | Hyperlipidémie | |||
| Cévní poruchy | Migréna | Hypertenze | Venózní tromboembolismus Arteriální tromboembolismus | |
| Celkové poruchy a reakce v místě aplikace | Zvýšení tělesné hmotnosti Retence tekutin | |||
| Poruchy imunitního systému | Lupus erythematosus | |||
| Poruchy reprodukčního systému a prsu | Nepravidelné krvácení Amenorea Hypomenorea Citlivost prsu | Změny vaginálního sekretu | ||
| Psychiatrické poruchy | Změna libida Deprese Podrážděnost |
Následující závažné nežádoucí účinky byly hlášeny u žen užívajících COC, viz body 4.3 a 4.4.
o Venózní tromboembolismus, např. hluboká venózní trombóza v nohách nebo pánvi a plicní embolie
o Arteriální tromboembolická porucha
o Nádory jater
o Poruchy kůže a podkožní tkáně: chloasma
Frekvence diagnózy rakoviny prsu je mezi uživatelkami COC velmi lehce zvýšena. Rakovina prsu žen do 40 let je vzácná, zvýšený výskyt je ve vztahu k celkovému riziku rakoviny prsu nízký. Příčinná souvislost s užíváním COC je neznámá. Další informace v bodu 4.3 a 4.4.
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
Webové stránky: http: /
4.9 Předávkování
Nejsou žádné zprávy o vážných škodlivých účincích z předávkování. Vyskytnout se mohou tyto příznaky: nevolnost, zvracení a vaginální krvácení. Neexistují žádná antidota a další léčba by měla být symptomatická.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: hormonální kontraceptivum pro systémové užití
ATC kód: G03 AA10.
Kontracepční účinek kombinovaných perorálních kontraceptiv (COC) je založen na spolupůsobení různých faktorů. Nejdůležitější z nich je inhibice ovulace a změny v endometriu.
Kromě ochrany proti otěhotnění poskytují COC další výhody, které vedle negativních vlastností (viz bod 4.4 a 4.8.) mohou být užitečné v rozhodování, zda zvolit tuto metodu kontracepce. Cyklus je pravidelnější a krvácení je slabší. Díky tomu může dojít ke snížení výskytu deficitu železa.
5.2 Farmakokinetické vlastnosti
Gestoden
Absorpce
Perorálně podaný gestoden je rychle a kompletně absorbován. Maximální sérové hladiny 4 ng/ml je dosaženo asi za 1 hod po požití jednotlivé dávky. Biologická dostupnost je okolo 99%.
Distribuce
Gestoden je vázán na sérový albumin a na sex hormone binding globulin (SHBG). Pouze 1–2% z celkové sérové koncentrace je přítomno ve formě volného steroidu, 50–70% je specificky vázáno na SHBG. Ethinylestradiolem indukované zvýšení SHBG ovlivňuje množství gestodenu vázaného na sérové proteiny, což má za následek zvýšení frakce vázané na SHBG a snížení frakce vázané na albumin. Distribuční objem gestodenu je 0,7 l/kg.
Biotransformace
Gestoden je kompletně metabolizován obvyklou cestou metabolismu steroidů. Rychlost metabolické clearance ze séra je asi 0,8 ml/min/kg. Nebyla nalezena přímá interakce v případě, kdy byl gestoden podáván spolu s ethinylestradiolem.
Eliminace
Hladina gestodenu klesá ve dvou fázích. Závěrečná fáze je charakterizována poločasem přibližně 1215 hodin.
Gestoden není vylučován v nezměněné formě. Jeho metabolity jsou vylučovány močí a žlučí v poměru přibližně 6:4. Poločas exkrece metabolitů je asi 1 den.
Rovnovážný stav
Farmakokinetika gestodenu je ovlivněna hladinou SHBG v séru, která se zvyšuje třikrát, je-li podáván současně s ethinylestradiolem. Po opakovaném denním podávání sérová hladina stoupá asi čtyřikrát a rovnovážného stavu je dosaženo ve druhé polovině léčebného cyklu.
Ethinylestradiol
Absorpce
Perorálně podaný ethinylestradiol je rychle a kompletně absorbován. Nejvyšší sérové koncentrace okolo 80 pg/ml je dosaženo během 1–2 hodin. Celková biologická dostupnost závisející na presystémové konjugaci a first pass efektu je přibližně 60%.
Distribuce
Během kojení 0,02 % denní dávky přechází do mateřského mléka.
Ethinylestradiol je vysoce, ale nespecificky vázán na sérový albumin (přibližně 98,5%) a indukuje vzestup sérové koncentrace SHBG. Distribuční objem je uváděn kolem 5 l/kg.
Biotransformace
Ethinylestradiol podléhá presystémové konjugaci jak ve stěně tenkého střeva, tak v játrech. Ethinylestradiol je primárně metabolizován aromatickou hydroxylací, vzniká však velké množství různých hydroxylovaných a methylovaných metabolitů, které jsou přítomny jako volné metabolity nebo konjugované s kyselinou glukuronovou a sírovou. Metabolická clearance je uváděna 5 ml/min/kg.
Eliminace
Hladiny ethinylestradiolu klesají ve dvou fázích, druhá s poločasem 24 hodin. Nezměněný ethinylestradiol není vylučován, jeho metabolity jsou vylučovány močí a žlučí v poměru 4:6. Poločas exkrece metabolitů je asi 1 den.
Rovnovážný stav
Rovnovážného stavu je dosaženo po 3 – 4 dnech, sérové hladiny ethinylestradiolu jsou o 30 – 40% vyšší než u jednotlivé dávky.
5.3 Preklinické údaje vztahující se k bezpečnosti
Ethinylestradiol ani gestodem není genotoxický. Studie karcenogenity s ethinylestradiolem samotným nebo v kombinaci s různými progesterony neodhalily karcinogenní riziko pro ženy užívající kontraceptiva. Mělo by však být stále pamatováno na to, že pohlavní steroidy mohou podporovat růst určitých hormon-dependentních tkání a tumorů.
Studie na lidech zkoumající toxický efekt na fertilitu, vývoj plodu nebo na schopnost rozmnožování s ethinylestradiolem samotným nebo v kombinaci s progestageny neprokázaly žádné nežádoucí účinky v případech, že je COC užívána dle doporučení.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Jádro tablety:
Magnesium-stearát, povidon 25, kukuřičný škrob, monohydrát laktosy
Obalová vrstva:
Povidon 360, makrogol 6 000, mastek, uhličitan vápenatý, sacharosa, montanglykolový vosk
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
3 roky
6.4 Zvláštní opatření pro uchovávání
Uchovávejte při teplotě do 30°C.
6.5 Druh obalu a obsah balení
PVC/Al blistr
Velikost balení: 1 × 21 tablet; 3 × 21 tablet, 6 × 21 tablet
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku
Žádné zvláštní požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Heaton k.s.
140 00 Praha 4
Česká republika
8. REGISTRAČNÍ ČÍSLO
17/192/07-C
9. DATUM PRVNÍ REGISTRACE / PRODLOUŽENÍ REGISTRACE
21. 3. 2007/20. 4. 2012
Další informace o léčivu KATYA
Jak
se KATYA
podává: perorální podání - obalená tableta
Výdej
léku: na lékařský předpis
Balení: Blistr
Velikost
balení: 6X21
Držitel rozhodnutí o registraci daného léku v České republice:
Heaton k.s., Praha
E-mail: safety@heaton.cz
Telefon: 242 482 690
