Příbalový leták - CERNEVIT
sp.zn. sukls292991/2018
Příbalová informace: informace pro pacienty
1. Co je přípravek CERNEVIT a účinky
Přípravek CERNEVIT se používá k doplnění vitamínů u pacientů na parenterální výživě. Pouze pro dospělé, dospívající a děti starší 11 let.
Přípravek CERNEVIT je prášek pro injekční nebo infuzní roztok.
Obsahuje 12 vitamínů:
| Retinoli palmitas (Vitamín A) | Pyridoxini hydrochloridum (Vitamín B6) | Acidum ascorbicum (Vitamín C) |
| Thiamine (Vitamín B1) | Biotinum (Vitamín B8) | Colecalciferolum (Vitamín D) |
| Riboflavini natrii phosphas dihydricus (Vitamín B2) | Acidum folicum (Vitamín B9) | Tocoferolum alfa RRR (Vitamín E) |
| Dexpanthenolum (Vitamín B5) | Cyanocobalaminum (Vitamín B12) | Nicotinamidum (Vitamín PP) |
Přípravek CERNEVIT se používá k intravenóznímu doplnění vitamínů u pacientů na parenterální výživě (infuzí).
Přípravek CERNEVIT poskytuje vyvážený obsah vitamínů rozpustných ve vodě a v tucích odpovídající denní potřebě při parenterální výživě.
U pacientů, kterým je podáván přípravek CERNEVIT, se obnovují plazmatické hladiny vitamínů A, D a E a během dlouhodobé parenterální výživy se tyto hladiny udržují v normálním rozmezí.
2. Čemu musíte věnovat pozornost, než začnete přípravek CERNEVIT používat
Nepoužívejte přípravek CERNEVIT
Přípravek CERNEVIT nesmí být podáván:
- jestliže jste alergický(á)/hypersenzitivní na kteroukoli léčivou látku nebo pomocnou látku přípravku CERNEVIT, zejména na vitamín B1 nebo na sójovou bílkovinu nebo arašídovou bílkovinu (viz bod 6, Obsah balení a další informace)
- novorozencům, kojencům a dětem mladším 11 let
- jestliže trpíte hypervitaminózou kteréhokoli z vitamínů obsaženého v přípravku
CERNEVIT
Upozornění a opatření
Před použitím přípravku CERNEVIT informujte svého lékaře, lékárníka nebo zdravotní sestru:
- jestliže máte onemocnění jater
- jestliže máte onemocnění ledvin nebo jste na dialýze
- jestliže máte epilepsii
- jestliže máte Parkinsonovu chorobu
Hypersenzitivní reakce
U přípravku CERNEVIT byly hlášeny mírné až závažné alergické reakce na vitamíny B1, B2, B12, kyselinu listovou a sójový lecithin.
Byly pozorovány zkřížené alergické reakce mezi sójovými a arašídovými bílkovinami.
Pokud se u Vás objeví příznaky alergické reakce jako je pocení, horečka, třesavka, bolest hlavy, kožní vyrážka, kopřivka nebo ztížené dýchání, ihned to sdělte svému lékaři. Lékař infuzi okamžitě ukončí a provede neodkladná opatření.
Předávkování a vitamínová toxicita
Je možné, že bude sledována hladina vitamínů v krvi (zejména vitamínu A, D a E), zvláště pokud dostáváte vitamíny z jiných zdrojů nebo dlouhodobě. Předávkování vitamínem A se může projevit kožními a kostními změnami, zdvojeným viděním a cirhózou. Toto riziko se zvyšuje, pokud trpíte podvýživou, máte dysfunkci jater a ledvin, jste malého vzrůstu nebo užíváte vitamín A dlouhodobě.
Vzhledem k obsahu glykocholové kyseliny v přípravku je třeba při opakovaném dlouhodobém podávání pacientům s hepatálním ikterem nebo signifikantní laboratorní cholestázou pečlivě monitorovat jaterní funkce.
Vzhledem k obsahu kyseliny listové v přípravku CERNEVIT je třeba dodržovat zvláštní opatření při kombinaci s léčbou antiepileptiky obsahujícími fenobarbital, fenytoin nebo primidon (viz Použití s jinými léčivými přípravky).
Vzhledem k obsahu pyridoxinu v přípravku CERNEVIT je třeba dodržovat zvláštní opatření při kombinaci s léčbou levodopou, existuje možnost snížení účinku L-dopy (viz Použití s jinými léčivými přípravky).
Deficit jednoho nebo více vitamínů musí být upraven zvlášť.
Přípravek CERNEVIT neobsahuje vitamín K, který je v případě potřeby nutno podat samostatně.
Další léčivé přípravky a přípravek CERNEVIT
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval(a) nebo které možná budete užívat.
Věnujte zvláštní pozornost, pokud užíváte přípravek obsahující některou z následujících léčivých látek nebo se u Vás vyskytuje některý z následujících stavů:
-
– některá antibiotika (chloramfenikol, ethionamid a tetracyklin) chronická nadměrná konzumace alkoholu
-
– antikonvulziva (léčiv používaná pro léčbu a prevenci epileptických záchvatů (křečí))
-
– látky s protisrážlivým účinkem
-
– vysoké dávky antiretrovirotika (přípravky proti HIV/AIDS)
-
– deferoxamin
-
– fluoropyrimidiny (některé léky určené k léčbě nádorů jako je _5-fluorouracil, apecitabin
-
– antagonisté folátu nebo folátové antimetabolity (jako je methotrxate, sulfosalazin, raltitrexed a jiné)
-
– L-dopa (používaná k léčbě Parkinsonovy choroby)
-
– fenobarbital, fenytoin a primidon (používané k léčbě epilepsie)
-
– antagonisté pyridoxinu (jako je cykloserin, hydralazin a jiné)
-
– retinoidy (sloučeniny, které chemicky odpovídají vitamínu A)
-
– theofylin
-
– přípravky s vysoce koncentrovaným vitamínem E
-
– antagonisté vitamínu K (jako je warfarin)
Ošteřující lékař bude pravděpodobně sledovat hladinu těchto léků ve Vaší krvi a je možné, pokud zahájíte nebo ukončíte podávání přípravku CERNEVIT, že upraví jejich dávku.
Některé léčivé přípravky mohou vzájemně reagovat s vitamíny v dávkách výrazně vyššími než dávkou přijatou z přípravku CERNEVIT. Ošetřující lékař bude upravovat dávky těchto přípravků zvláště, pokud dostanete současně s přípravkem CERNEVIT vitamíny z jiných zdrojů.
Plodnost, těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem dříve, než začnete tento přípravek užívat.
Těhotenství
Přípravek CERNEVIT může být předepsán během těhotenství, je-li to zapotřebí, za předpokladu, že indikace a dávkování jsou sledovány, aby se předešlo předávkování vitamínů. Kojení
Použití přípravku CERNEVIT se během kojení se nedoporučuje vzhledem k možnosti ohrožení novorozence předávkováním vitamínem A.
Plodnost
Nejsou k dispozici žádné údaje o účinku přípravku CERNEVIT na ženskou nebo mužskou fertilitu.
Řízení dopravních prostředků a obsluha strojů
Neexistují žádné informace o účincích přípravku CERNEVIT na schopnost řídit automobil nebo jiné těžké stroje.
Přípravek CERNEVIT obsahuje sójové fosfatidy, jestliže jste alergičtí na arašídy nebo sóju, neužívejte tento léčivý přípravek.
3. Jak se přípravek CERNEVIT používá
Přípravek CERNEVIT Vám bude podán odborným zdravotnickým personálem. Nejspíš dostanete přípravek CERNEVIT jako infuzi do žíly.
Doporučená dávka je 1 lahvička denně.
Akutní nebo chronické předávkování (zejména vitamínů A, B6, D a E) může způsobit hypervitaminózu. Rizika předávkování existují v případech, když přijímáte vitamíny s jinými přípravky a celkové množství vitamínů neodpovídá Vaší potřebě, nebo máte-li sklon k rozvoji hypervitaminózy.
Jestliže bylo podáno více přípravku CERNEVIT, než mělo být
Příznaky předávkování jsou nejčastěji způsobeny podáním nadměrných dávek vitamínu A
Klinické příznaky akutního předávkování vitamínem A (dávky převyšující 150, 000 IU)
- gastrointestinální obtíže (nevolnost, zvracení)
- onemocnění nervového systému (bolesti hlavy, otok zrakového nervu, křeče) v důsledku zvýšeného nitrolebečního tlaku (intrakraniální hypertenze)
- psychiatrické příznaky (iritabilita až křeče)
- kožní onemocnění (zpožděná generalizovaná deskvamace).
Klinické příznaky chronické intoxikace (riziko při dlouhodobém podávání vitamínu A v nadměrných dávkách osobám bez deficitu)
- bolest hlavy způsobená zvýšeným nitrolebečním tlakem
- onemocnění kostí (citlivý nebo bolestivý otok dlouhých kostí. Diagnóza je založena zpravidla na přítomnosti bolestivých subkutánních otoků končetin. RTG vyšetření potvrzuje diafyzální periostální ztluštění ulny, fibuly, klavikul a žeber).
Léčba v případě akutního nebo chronického předávkování
Přerušení podávání přípravku CERNEVIT, snížení přísunu kalcia, zvýšení diurézy a rehydratace.
Pokud jste si všimnul(a) některého z příznaků předávkování, sdělte to svému ošetřujícímu lékaři, který pravděpodobně infuzi přípravku CERNEVIT ukončí.
Máte-li jakékoli další otázky týkající se užívání tohoto přípravku, zeptejte se svého lékaře, lékárníka nebo zdravotní sestry.
4.
Podobně jako všechny léčivé přípravky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Následující nežádoucí účinky jsou časté a mohou se vyskytnout u 1 až 10 pacientů ze 100:
-
– Bolest v místě vpichu
-
– Pocit nevolnosti (nauzea), pocit na zvracení (zvracení)
-
– Alergické reakce s dýchacími obtížemi, bolestí na hrudi, staženým hrdlem, zrychleným dýcháním, kopřivkou, vyrážkou, zarudnutím kůže, břišním dyskomfortem a zrychlenou tepovou frekvencí
-
– Zvýšené hladiny vitamínu A a bílkovinného nosiče vitamínu A v krvi
-
– Poruchy chuti (kovová chuť)
-
– Průjem
-
– Zvýšená hladina jaterních enzymů a žlučových kyselin
-
– Pruritus (svědění)
-
– Horečka, celková bolestivost, reakce v místě vpichu jako je pálení, vyrážka
-
– Těžká alergická reakce (anafylaktická reakce)
Pokud se u Vás vyskytne příznak alergické reakce jako je zhoršené dýchání, bolest na hrudi, stažené hrdlo, kopřivka, vyrážka, zarudnutí kůže, dyskomfort břicha, informujte okamžitě svého lékaře, který ukončí infuzi a nastaví nezbytná neodkladná opatření.
Pokud se kterýkoli z nežádoucích účinků vyskytne v závažné míře, prosím sdělte to svému lékaři.
Hlášení nežádoucích účinků
Pokud se u Vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo zdravotní sestře. Stejně postupujte v případě jakýchkoli nežádoucích účinků, které nejsou uvedeny v této příbalové informaci. Nežádoucí účinky můžete hlásit také přímo na níže uvedenou adresu.
Státní ústav pro kontrolu léčiv, Šrobárova 48, 100 41 Praha 10.
Webové stránky:
Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
5.
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Uchovávejte při teplotě do 25 °C.
Uchovávejte lahvičky v krabičce, aby byl přípravek chráněn před světlem.
Přípravek CERNEVIT nepoužívejte po uplynutí doby použitelnosti uvedené na lahvičce a na vnějším obalu. Doba použitelnosti se vztahuje k poslednímu dni uvedeného měsíce. Zkontrolujte, zda obal není porušen.
Dodržujte zásady aseptické techniky.
Nepoužívejte částečně použité lahvičky nebo přípravek, který je po rozpuštění neobvykle zabarven.
Před smícháním s jinými infuzními roztoky je třeba zkontrolovat kompatibilitu, zvláště je-li přípravek CERNEVIT přidáván do vaků s binární směsí pro parenterální výživu kombinující glukózu, a roztok elektrolytů a aminokyselin, případně do vaků s vícesložkovou směsí kombinující glukózu, roztok elektrolytů a aminokyselin a lipidy.
Po naředění byla prokázána chemická a fyzikální stabilita po dobu 24 hodin při teplotě 25 °C.
Z mikrobiologického hlediska má být přípravek použit ihned po rozpuštění. Není-li použit okamžitě, doba a podmínky uchovávání přípravku před použitím jsou v odpovědnosti uživatele a doba by neměla být delší než 24 hodin při teplotě 2 °C – 8 °C, pokud rozpuštění neproběhlo za kontrolovaných a validovaných aseptických podmínek.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Tato opatření pomáhají chránit životní prostředí.
6. Obsah balení a další informace
Co přípravek CERNEVIT obsahuje
1 lahvička 5 ml přípravku obsahuje:
Léčivé látky:retinoli palmitas colecalciferolum tocoferolum alfa RRR acidum ascorbicum cocarboxylasum tetrahydricum riboflavini natrii phosphas dihydricus pyridoxini hydrochloridum cyanocobalaminum acidum folicum dexpanthenolum biotinum nicotinamidum
3500 IU (1,925 mg)
220 IU (0,0055 mg)
10,200 mg
125,00 mg
5,80 mg
5,67 mg
5,50 mg
0,006 mg
0,414 mg
16,150 mg
0,069 mg
46,0 mg
Pomocné látky:
glycin, kyselina glykocholová, sójové fosfatidy, roztok hydroxidu sodného 1 mol/l a roztok kyseliny chlorovodíkové 1 mol/l k úpravě pH
Lahvička přípravku CERNEVIT obsahuje 24 mg sodíku (1 mmol). Toto je třeba vzít v úvahu u pacientů s kontrolovanou sodíkovou dietou.
Jak přípravek CERNEVIT vypadá a co obsahuje toto balení
- prášek v lahvičce (hnědé sklo, typ I)
- prášek v lahvičce (hnědé sklo, typ I) s BIO-SETEM Krabička s obsahem 1, 10 nebo 20 lahviček
Na trhu nemusí být všechny velikosti balení.
Přípravek CERNEVIT (lahvička bez aplikační sady BIO-SET)
Pomocí injekční stříkačky naplňte lahvičku 5 ml vody na injekci nebo 5 % roztoku glukózy nebo 0,9% roztoku chloridu sodného.
Lehce promíchejte, aby došlo k rozpuštění prášku.
Výsledný roztok je oranžovo-žluté barvy.
Přípravek CERNEVIT BIO-SET
Přípravek CERNEVIT BIO-SET umožňuje přímé rozpouštění ve vacích (jednokomorových nebo vícekomorových plastových vacích) vybavených injekčním vstupem.
Držitel rozhodnutí o registraci a výrobce
DRŽITEL ROZHODNUTÍ O REGISTRACI
BAXTER CZECH spol. s r.o.
Karla Engliše 3201/6, 150 00 Praha 5
Česká republika
VÝROBCE
Baxter S.A., Bd. R. Branquart 80, Lessines, Belgie
Tato příbalová informace byla naposledy schválena: 31. 7. 2018
Následující informace jsou určeny pouze pro zdravotnické pracovníky:
Kvalitativní a kvantitativní složení
Retinoli palmitas (odp. Vitamín A Colecalciferolum (odp. Vitamín D3 Tocoferolum alfa RRR (odp. Vitamín E
Acidum ascorbicum (odp. Vitamín C)
Cocarboxylasum tetrahydricum (odp. Vitamín B1
Riboflavini natrii phosphas dihydricus (odp. Vitamín B2
Pyridoxini hydrochloridum (odp. Vitamín B6
Cyanocobalaminum (odp. Vitamín B12) Acidum folicum (odp. Kyselina listová) Dexpanthenolum
(odp. Kyselina pantothenová Biotinum (odp. Biotin) Nicotinamidum (odp. Vitamín PP)
3 500 IU
-
I, 925 mg)
-
II, 200 IU) 125,000 mg 5,800 mg
3,510 mg)
5,670 mg 4,140 mg) 5,500 mg
4,530 mg 0,006 mg
0,414 mg
16,150 mg 17,250 mg)
0,069 mg 46,000 mg
Pomocné látky: glycin, kyselina glykocholová, sójové fosfatidy, roztok hydroxidu sodného 1 mol/l a roztok kyseliny chlorovodíkové 1 mol/l k úpravě pH
Popis přípravku:oranžovo-žlutý lyofilizát, bez zápachu až téměř bez zápachu. Výsledný roztok po rekonstituci je oranžovo-žluté barvy.
Dávkování a způsob podání:Pouze pro dospělé, dospívající a děti starší 11 let.
Dospělí, dospívající a děti starší 11 let:
1 lahvička denně
Pouze pro intravenózní podání
Způsob podání: viz návod k použití a manipulaci níže
Po rekonstituci: Podávejte v pomalé intravenózní injekci (nejméně 10 minut, viz bod Upozornění) nebo infuzi v roztoku 5% glukózy nebo ve fyziologickém roztoku pro infuzi.
Podávání může pokračovat po celou dobu parenterální výživy.
Přípravek CERNEVIT může být součástí výživových směsí, ve kterých jsou kombinovány cukry, tuky, aminokyseliny a elektrolyty za předpokladu, že kompatibilita a stabilita každé z těchto směsí byla potvrzena tak, aby se splnily výživové potřeby a předešlo se vzniku deficitů a komplikací.
Je třeba vzít v úvahu celkové množství vitamínů ze všech zdrojů, jako jsou zdroje nutriční, vitamínové doplňky stravy nebo léky obsahující vitamíny v neaktivní formě (např. Tipranavir roztok pro perorální podání obsahuje 116 IU/ml vitamínu E).
Je třeba sledovat klinický stav pacienta a monitorovat hladiny vitamínů, aby byly zajištěny jejich odpovídající hodnoty.
Je třeba vzít v úvahu, že některé vitamíny, zejména vitamín A, B2 a B6 jsou citlivé na ultrafialové záření (např. přímé či nepřímé sluneční světlo). Úbytek vitamínů A, B1, C a E se navíc může zvýšit při vyšších hodnotách kyslíku v roztoku. Tyto faktory je třeba uvážit, pokud nejsou dosaženy adekvátní hladiny vitamínů.
Kontraindikace
Přípravek CERNEVIT nesmí být použit:
- u hypersenzitivity na léčivé látky, zejména na vitamín B1 nebo na kteroukoliv na kteroukoli pomocnou látku (uvedenou v bodě 6.1), zahrnující sójové proteiny / přípravky (lecithin ve smíšených micelách je sójového původu) nebo arašídové proteiny / přípravkyu novorozenců, kojenců a dětí mladších 11 let
- u hypervitaminózy (zejména vitamínu A, E a D3)
Zvláštní upozornění a zvláštní opatření pro použití
Upozornění:
Hypersenzitivní reakce
- U přípravku CERNEVIT byly hlášeny mírné až závažné systémové hypersenzitivní reakce na složky přípravku (včetně vitamínů B1, B2, B12, kyselinu listovou a sójový lecithin) (viz bod 4.8).
Byly pozorovány zkřížené alergické reakce mezi sójovými a arašídovými bílkovinami.
- V některých případech mohou být projevy hypersenzitivní reakce během intravenózního podávání multivitamínů závislé na rychlosti podávání. Při intravenózní infuzi je zapotřebí přípravek CERNEVIT podávat pomalu. Při intravenózní injekci je třeba injekci aplikovat pomalu (v průběhu alespoň 10 minut).
- Infuzi nebo injekci je zapotřebí okamžitě ukončit, pokud se vyskytnou projevy či příznaky hypersenzitivní reakce.
Vitamínová toxicita
- Aby nedošlo k předávkování a toxickým účinkům, je zapotřebí monitorovat klinický stav pacienta a koncentrace vitamínů v krvi, obzvláště u vitamínů A, D a E, a to především u pacientů, kteří přijímají navíc vitamíny z jiných zdrojů, nebo užívají jiné přípravky zvyšující riziko vitamínové toxicity.
- Monitorování je důležité především u pacientů podstupujících dlouhodobou suplementaci.
Hypervitaminóza A
-
– Riziko hypervitaminózy A a toxicita vitamínu A (např. abnormality kůže a kostí, diplopie, cirhóza) je vyšší například u pacientů s proteinovou malnutricí, poškozením ledvin (i při nepřítomnosti suplementace vitamínem A), poškozením jater, pacientů s drobnou tělesnou konstitucí (např. u pediatrických pacientů) a pacientů na chronické terapii.
-
– Akutní jaterní onemocnění u pacientů se saturovanými zásobami vitamínu A může vést k manifestaci toxicity vitamínem A.
Hypervitaminóza D
-
– Nadměrné množství vitamínu D může způsobit hyperkalcémii a hyperkalcinurii
-
– Riziko toxicity vitamínem D je zvýšeno u pacientů s hyperparathyroidismem nebo u pacientů s dlouhodobým podáváním vitamínů.
Hypervitaminóza E
-
– I když velmi vzácně, nadměrné dávky vitamínu E nepříznivě ovlivňují hojení rány a podílejí na dysfunkci krevních destiček
-
– Riziko toxicity vitamínem E je zvýšeno u pacientů s poruchou jater, u pacientů, kteří mají poruchu krvácivosti nebo jsou na perorálních antikoagulanciích nebo u pacientů s dlouhodobým podáváním vitamínů.
„Refeeding“ syndrom u pacientů, kterým je podávána parenterální výživa Realimentace velmi nedostatečně živených pacientů může způsobit “refeeding“ syndrom, pro který je charakteristický nitrobuněčný posun draslíku, fosforu a hořčíku, zatímco se pacient stává anabolickým. Může se také rozvinout deficit thiaminu a zadržování tekutin. Pečlivé sledování a pomalé zvyšování příjmu živin při současné eliminaci nadměrného podávání živin může vzniku těchto komplikací zabránit. Při deficitu živin může být opodstatněná odpovídající suplementace.
Precipitáty u pacientů, kterým je podávána parenterální výživa
Plicní vaskulární precipitáty byly hlášeny u pacientů přijímajících parenterální výživu. V některých případech došlo k fatálním následkům. Nadměrné přidávání vápníku a fosfátů zvyšuje riziko tvorby kalcium-fosfátového precipitátu. Precipitáty byly hlášeny dokonce, i když fosfátová sůl nebyla v roztoku přítomna. Byly hlášeny také sraženiny distálně od in-line filtru a suspektní precipitáty v krevním řečišti.
Kromě kontroly roztoku je také třeba pravidelně kontrolovat, zda se sraženiny nenacházejí v infuzní soupravě a v katétru.
Pokud se objeví příznaky plicních potíží, je zapotřebí infuzi zastavit a zahájit lékařské zhodnocení.
Zkontrolujte, zda obal není porušen.
Dodržujte zásady aseptické techniky.
Nepoužívejte částečně použité lahvičky nebo přípravek, který je po rozpuštění neobvykle zabarven.
Zvláštní opatření pro použití
Účinky na játra
- U pacientů užívajících přípravek CERNEVIT se doporučuje monitorovat parametry jaterní funkce. Obzvláště pečlivé monitorování se doporučuje u pacientů se žloutenkou nebo jiným důkazem cholestázy.
- Je známé, že u některých pacientů na parenterální výživě (včetně parenterální výživy doplněné vitamíny) dochází k rozvoji hepatobiliárních poruch včetně cholestázy, steatózy jater, fibrózy a cirhózy, které mohou vést k jaternímu selhání, stejně jako k cholecystitidě a cholelitiáze. Etiologie těchto poruch se považuje za multifaktoriální a u jednotlivých pacientů se může lišit. Pacienty s rozvojem abnormálních laboratorních parametrů nebo jiných příznaků hepatobiliárních poruch by měl včas zhodnotit lékař -hepatolog, který může identifikovat případné kauzální a kontribuční faktory a možnou terapeutickou a profylaktickou intervenci.
Použití u pacientů s poškozenou funkcí jater
Pacienti s poškozením jater mohou vyžadovat individualizovanou vitamínovou suplementaci. Zvláštní pozornost je třeba věnovat prevenci toxicity vitamínem A, protože aktuální jaterní onemocnění je spojeno se zvýšeným sklonem k toxicitě vitamínem A, především v kombinaci s chronicky nadměrnou spotřebou alkoholu (viz také části „Hypervitaminóza A“ a „Účinky na játra“ výše).
Použití u pacientů s poškozením funkce ledvin. Pacienti s poškozením ledvin mohou vyžadovat individualizovanou vitamínovou suplementaci, v závislosti na míře poškození ledvin a průvodním zdravotním stavu. U pacientů se závažným poškozením funkce ledvin je třeba věnovat zvláštní pozornost udržování odpovídajícího stavu vitamínu D a zabránit toxicitě vitamínu A, která se může projevit u pacientů suplementovaných nízkou dávkou vitamínu A, nebo i bez suplementace.
Hypervitaminóza a toxicita pyridoxinu (vitamín B6) (periferní neuropatie, mimovolní pohyby) byla hlášena u pacientů na chronické hemodialýze, kterým jsou podávány nitrožilní multivitamíny obsahující 4 mg pyridoxinu podávaného třikrát týdně.
Všeobecný monitoring
U pacientů, kterým jsou po delší dobu podávány parenterální multivitamíny jako jediný zdroj vitamínů, je zapotřebí sledovat klinický stav a hladiny vitamínů. Zejména důležité je monitorovat odpovídající suplementaci například:
- vitamínu A u pacientů s proleženinami, poraněními, spáleninami, syndromem krátkého střeva nebo cystickou fibrózou
- vitamínu B1 u pacientů na dialýze
- vitamínu B2 u pacientů s rakovinou
- vitamínu B6 u pacientů s poškozením ledvin
- jednotlivých vitamínů, jejichž potřeba může být zvýšena kvůli interakcím s jinými léky (viz bod Interakce s jinými léčivými přípravky).
Deficit jednoho nebo více vitamínů musí být upraven specifickou suplementací.
Přípravek CERNEVIT neobsahuje vitamín K, který je v případě potřeby nutno podat samostatně.
Použití u pacientů s deficitem vitamínu B12
Před zahájením podávání přípravku CERNEVIT se doporučuje pacientům ohroženým deficitem vitamínu B12 a/nebo pokud je plánována suplementace přípravkem CERNEVIT po několik týdnů, vyhodnotit stav vitamínu B12.
Po několika dnech podávání mohou být jednotlivá množství kyanokobalaminu (vitamín B12) a kyseliny listové v přípravku CERNEVIT dostačující, následkem čehož se u některých pacientů s megaloblastickou anémií spojenou s deficitem vitamínu B12 zvyšuje počet červených krvinek, počet retikulocytů a hodnoty hemoglobinu. To může maskovat aktuální deficit vitamínu B12. Účinná léčba deficitu vitamínu B12 vyžaduje vyšší dávky kyanokobalaminu, než které přípravek CERNEVIT obsahuje.
Suplementace kyseliny listové u pacientů s deficitem vitamínu B12, kteří současně neužívají vitamín B12, nezabraňuje rozvoji ani progresi neurologických projevů spojených s deficitem vitamínu B12. Nabízí se, že se neurologické zhoršení může urychlit.
Při interpretaci hladin vitamínu B12 by se mělo vzít v úvahu, že příjem vitamínu B12 v nedávné době může vést k normálním hladinám navzdory tkáňovému deficitu.
Interference laboratorních testů
V závislosti na použitých reagentech může přítomnost kyseliny askorbové v krvi a moči způsobit falešně vysoké nebo nízké hladiny glukózy v některých testech moči a krve, včetně testovacích proužků a ručních glukometrů. Technické informace všech laboratorních testů je třeba konzultovat, aby bylo možné stanovit potenciální interferenci způsobenou vitamíny.
Vzhledem k obsahu kyseliny listové v přípravku CERNEVIT je třeba dodržovat zvláštní opatření při kombinaci s léčbou antiepileptiky obsahujícími fenobarbital, fenytoin nebo primidon.
Vzhledem k obsahu pyridoxinu v přípravku CERNEVIT je třeba dodržovat zvláštní opatření při kombinaci s léčbou levodopou, protože může snížit účinek L-dopy.
Pediatrická populace
Přípravek CERNEVIT je indikován u pediatrických pacientů starších 11 let (viz také bod Zvláštní upozornění a zvláštní opatření pro použití).
Geriatrická populace
Obecně je vhodné u starších pacientů zvážit upravení dávky (snížení dávky a/nebo prodloužení dávkovacích intervalů) odrážející vyšší frekvenci poklesu funkce jater, ledvin nebo srdce, stejně jako průvodních onemocnění nebo užívané medikace.
Obsah sodíku
Přípravek CERNEVIT obsahuje 24 mg sodíku (1 mmol) v každé lahvičce. To je třeba vzít v úvahu u pacientů na kontrolované nízkosodíkové dietě.
Před smícháním s jinými infuzními roztoky je třeba zkontrolovat kompatibilitu, zvláště je-li přípravek CERNEVIT přidáván do vaků s binární směsí pro parenterální výživu kombinující glukózu, a roztok elektrolytů a aminokyselin, případně do vaků s vícesložkovou směsí kombinující glukózu, roztok elektrolytů a aminokyselin a lipidy.
Interakce s jinými léčivými přípravky a jiné formy interakce
Interakce mezi specifickými vitamíny v přípravku CERNEVIT a dalšími přípravky je třeba odpovídajícím způsobem řešit.
K těmto interakcím patří:
- Přípravky, které mohou způsobovat pseudotumor cerebri (idiopatická intrakraniální hypertenze) (včetně určitých tetracyklinů): Zvýšené riziko idiopatické intrakraniální hypertenze při současném podávání vitamínu A.
- Alkohol (chronická nadměrná konzumace): Zvyšuje riziko hepatotoxicity vitamínu A
- Antikonvulziva a kyselina listová: Kyselina listová může zvyšovat metabolismus některých antiepileptik, např. fenobarbitalu, fenytoinu, fosfenytoinu a primidonu, což může zvyšovat riziko záchvatů. Při současném podávání folátů a po jeho ukončení je třeba pečlivě monitorovat plazmatické koncentrace antikonvulziv.
- Vitamín E může podporovat inhibici funkce krevních destiček nebo zesílit antikoagulační účinek přípravků jako jsou aspirin nebo warfarin.
- Kyselina acetylsalicylová (léčba vysokými dávkami) Může snižovat hladiny kyseliny listové zvýšením exkrece močí.
- Určitá antikolvuziva (např. fenytoin, karbamazepin, fenobarbital, valproát): Mohou způsobovat deficit folátu, pyridoxinu a vitamínu D
- Určitá antivirotika: Snížené hladiny vitamínu D jsou spojovány např. s přípravky efavirenz a zidovudin. Snížená tvorba aktivních metabolitů vitamínu D byla spojena s inhibitory proteázy.
- Chloramfenikol: Může inhibovat hematologickou odpověď na léčbu vitamínem B12.
- Deferoxamin: Zvýšené riziko srdečního selhání způsobeného železem z důvodu zvýšené mobilizace železa při suprafyziologické suplementaci vitamínu C. Specifická opatření viz informace o přípravku deferoxamin.
- Etionamid: Může způsobovat deficit pyridoxinu.
- Fluoropyrimidiny (5-fluorouracil, kapecitabin, tegafur): Zvýšená toxicita při kombinaci s kyselinou listovou.
- Antagonisté folátu, např. metotrexát, sulfasalazin, pyrimetamin, triamteren, trimetoprim a vysoké dávky čajových katechinů: blokování konverze folátů na jejich aktivní metabolity a snížení účinnosti suplementace
- Antimetabolity folátu (metotrexát, raltitrexed): Suplementace kyselinou listovou může mít za následek potřebu vyšší dávky těchto látek, aby se dosáhlo požadovaného terapeutického účinku.
- Levodopa: Vitamín B6 může snižovat účinnost levodopy, protože dekarboxylace levodopy vyžaduje enzym závislý na vitamínu B6. Pro zabránění této interakci lze přidat dopa-dekarbolyzovaný inhibitor, jako je karbidopa.
- Antagonisté pyridoxinu, včetně cykloserinu, hydralazinu, isoniazidu, penicillaminu, fenelzinu: Mohou způsobovat deficit pyridoxinu.
- Retionidy, včetně bexarotenu: Zvyšují riziko toxicity, pokud jsou používány současně s vitamínem A (viz bod Zvláštní upozornění a zvláštní opatření pro použití, odstavec Hypervitaminóza A)
- Theofylin: Může způsobovat deficit pyridoxinu
Předávkování
Akutní nebo chronické předávkování vitamínů (zejména A, B6, D a E) může způsobit symptomatické hypervitaminózy.
Riziko předávkování je zvlášť vysoké, jestliže pacient dostává vitamíny z více zdrojů a celkové doplnění vitamínů neodpovídá individuálním požadavkům pacienta a u pacientů se zvýšeným sklonem k hypervitaminóze (viz bod Zvláštní upozornění a zvláštní opatření pro použití).
Příznaky předávkování jsou nejčastěji způsobeny podáním nadměrných dávek vitamínu A. Klinické příznaky akutního předávkování vitamínem A (dávky převyšující 150, 000 IU)
- gastrointestinální obtíže, bolesti hlavy, intrakraniální hypertenze, edém papily, psychiatrické příznaky, iritabilita až křeče, zpožděná generalizovaná deskvamace.
Klinické příznaky chronické intoxikace (riziko při dlouhodobém podávání vitamínu A v nadměrných dávkách osobám bez deficitu)
- intrakraniální hypertenze, kortikální hyperostóza dlouhých kostí. Diagnóza je založena zpravidla na přítomnosti bolestivých subkutánních otoků končetin. RTG vyšetření potvrzuje diafyzální periostální ztluštění ulny, fibuly, klavikul a žeber.
Léčba předávkování vitamínem znamená obvykle jeho vysazení a další opatření, která jsou klinicky indikována (např. snížení příjmu vápníku, zvýšení diurézy a rehydratace).
Farmaceutické údaje
Doba použitelnosti
2 roky
Po naředění byla prokázána chemická a fyzikální stabilita po dobu 24 hodin při teplotě 25 °C. Z mikrobiologického hlediska má být přípravek použit ihned po rozpuštění. Není-li použit okamžitě, doba a podmínky uchovávání přípravku před použitím jsou v odpovědnosti uživatele a doba by neměla být delší než 24 hodin při teplotě 2°C – 8°C, pokud rozpuštění neproběhlo za kontrolovaných a validovaných aseptických podmínek.
Zvláštní opatření pro uchováváníUchovávejte při teplotě do 25°C.
Uchovávejte lahvičky v krabičce, aby byl přípravek chráněn před světlem.
Druh obalu a velikost balení
Prášek v lahvičce z hnědého skla s pryžovou zátkou s nebo bez BIO-SETU.
Krabička s obsahem 1, 10 nebo 20 lahviček.
Na trhu nemusí být všechny velikosti balení.
Podle potřeby prostudujte příslušné reference a pokyny o kompatibilitě. Tento léčivý přípravek nesmí být mísen s jinými léčivými přípravky s výjimkou případů, ve kterých byla kompatibilita a stabilita prokázána. V tomto případě prosím kontaktujte pro další informace držitele rozhodnutí o registraci.
Kompatibilita s roztoky podávanými současně stejnou linkou musí být zkontrolována.
Přípravek CERNEVIT (lahvička bez aplikační sady BIO-SET)
Pomocí injekční stříkačky naplňte lahvičku 5 ml vody na injekci nebo 5 % roztoku glukózy nebo 0,9% roztoku chloridu sodného.
Lehce promíchejte, aby došlo k rozpuštění prášku.
Výsledný roztok je oranžovo-žluté barvy.
PŘÍPRAVEK CERNEVIT BIO-SET
Přípravek CERNEVIT BIO-SET umožňuje přímé rozpouštění ve vacích (jednokomorových nebo vícekomorových plastových vacích) vybavených injekčním vstupem.
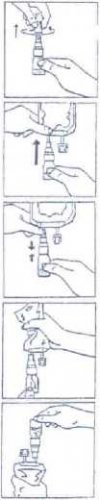
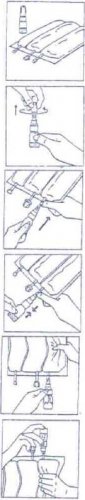
Jednokomorové vaky:
-
1. Sejměte uzávěr pootočením a následným tahem za jisticí pruh uzávěru.
-
2. Aplikační sadu BIO-SET napojte na injekční vstup.
-
3. Tlakem na průhlednou pohyblivou část aplikační sady propíchněte pryžový uzávěr lahvičky.
-
4. Propojený vak a aplikační sadu držte ve vertikální poloze vakem nahoru. Několikrát lehce stlačte vak, čímž naplníte lahvičku (přibližně 5 ml) roztokem. Protřepáním lahvičky dojde k rozpuštění přípravku CERNEVIT.
-
5. Napojený vak a aplikační sadu obraťte vzhůru nohama. Několikrát lehce stlačte vak, čímž dojde k vytlačení vzduchu do lahvičky a roztoku do vaku.
-
6. Body 4 a 5 opakujte, dokud nedojde k vyprázdnění lahvičky.
-
7. Sejměte lahvičku aplikační sady CERNEVIT BIO-SET a zlikvidujte ji.
-
8. Lehce promíchejte.
Vícekomorové vaky:
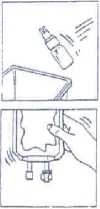
Rozpuštění přípravku CERNEVIT BIO-SET je nutno provést před aktivací vícekomorového vaku (před rozpojením švů a před smícháním obsahu jednotlivých komor).
-
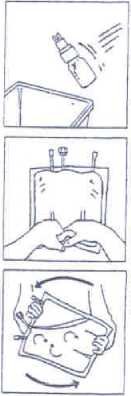
1. Položte vícekomorový vak na vodorovnou plochu.
-
2. Sejměte uzávěr aplikační sady CERNEVIT BIO-SET pootočením a následným tahem za jisticí pruh uzávěru.
-
3. Aplikační sadu BIO-SET napojte na injekční vstup vícekomorového vaku.
-
4. Tlakem na průhlednou pohyblivou část aplikační sady propíchněte pryžový uzávěr lahvičky.
-
5. Lahvičku držte ve vertikální poloze. Několikrát lehce stlačte vak, čímž naplníte lahvičku (přibližně 5 ml) roztokem. Protřepáním lahvičky dojde k rozpuštění přípravku CERNEVIT.
-
6. Propojený vak a aplikační sadu obraťte vzhůru nohama. Několikrát lehce stlačte vak, čímž dojde k vytlačení vzduchu do lahvičky a roztoku do vaku.
-
7. Body 5 a 6 opakujte, dokud nedojde k vyprázdnění lahvičky.
-
8. Sejměte lahvičku aplikační sady CERNEVIT BIO-SET a zlikvidujte ji.
-
9. Nakonec aktivujte vícekomorový vak.
-
10. Otáčením celého vaku (nejméně 3x) důkladně promíchejte.
Další informace o léčivu CERNEVIT
Jak
se CERNEVIT
podává: intravenózní podání - prášek pro injekční/infuzní roztok
Výdej
léku: na lékařský předpis
Balení: Injekční lahvička
Velikost
balení: 10 SET
Držitel rozhodnutí o registraci daného léku v České republice:
BAXTER CZECH spol. s r.o., Praha
E-mail: magdalena_brunova@baxter.com; dana_sladeckova@baxter.com
Telefon: 225774141, 225774143