Souhrnné informace o léku - EZANTRIS
1. NÁZEV PŘÍPRAVKU
Ezantris 10 mg tablety
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna tableta obsahuje ezetimibum 10 mg.
Pomocná látka se známým účinkem
Jedna tableta obsahuje 64 mg monohydrátu laktózy.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Tableta
Bílé až téměř bílé, kulaté, konvexní tablety o průměru přibližně 6 mm.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Primární hypercholesterolemie
Ezantris podávaný spolu s inhibitorem reduktázy HMG-CoA (statinem) je indikován jako přídatná terapie k dietě u pacientů s primární (heterozygotní familiární nebo nefamiliární) hypercholesterolemií, u kterých není dostatečná odpověď na léčbu při podávání statinu samotného.
Ezantris v monoterapii je indikován jako přídatná terapie k dietě u pacientů s primární (heterozygotní familiární nebo nefamiliární) hypercholesterolemií, u kterých není podávání statinu považováno za vhodné nebo není tolerováno.
Prevence kardiovaskulárních příhod
Ezantris je indikován ke snížení rizika kardiovaskulárních příhod (viz bod 5.1) u pacientů s ischemickou chorobou srdeční (ICHS) a s anamnézou akutního koronárního syndromu (AKS), a to jeli přidán k už probíhající léčbě statinem, nebo je-li jeho užívání zahájeno zároveň se statinem.
Homozygotní familiární hypercholesterolemie (HoFH)
Ezantris podávaný spolu se statinem je indikován jako přídatná terapie k dietě u pacientů s HoFH. Pacienti mohou dostávat i přídatnou terapii (např. aferézu LDL).
4.2 Dávkování a způsob podání
Dávkování
Pacient musí dodržovat příslušnou hypolipidemickou dietu a musí v této dietě během léčby přípravkem Ezantris pokračovat.
Přípravek se podává perorálně. Doporučená dávka je jedna tableta Ezantris 10 mg denně. Ezantris lze podávat v kteroukoli denní dobu, spolu s jídlem nebo bez něj.
Pokud je Ezantris přidán ke statinu, mělo by se pokračovat v podávání buď indikované obvyklé počáteční dávky konkrétního statinu, nebo již stanovené vyšší dávky statinu. V tomto případě by měl být brán ohled na pokyny pro dávkování konkrétního statinu.
Použití u pacientů s ischemickou chorobou srdeční a akutním koronárním syndromem v anamnéze Ezantris 10 mg se může podávat zároveň se statinem pro postupné snížení rizika kardiovaskulárních příhod u pacientů s ischemickou chorobou srdeční a akutním koronárním syndromem v anamnéze, přínos této kombinace byl prokázán.
Podávání spolu se sekvestranty žlučových kyselin
Ezantris by měl být podáván buď > 2 hodiny před nebo > 4 hodiny po podání sekvestrantů žlučových kyselin.
Starší osoby
U starších osob není nutno dávku nijak upravovat (viz bod 5.2).
Pediatrická populace
Léčbu je nutno zahájit pod dohledem specialisty.
Děti a dospívající > 6 let: Bezpečnost a účinnost ezetimibu u dětí ve věku 6 až 17 let nebyla dosud stanovena. V současnosti dostupné údaje jsou popsány v bodě 4.4, 4.8, 5.1 a 5.2, ale na jejich základě nelze učinit žádná doporučení ohledně dávkování.
Pokud se Ezantris podává se statinem, je nutno se obeznámit s pokyny o dávkování daného statinu u dětí.
Děti < 6 let: Bezpečnost a účinnost ezetimibu u dětí ve věku < 6 let nebyla dosud stanovena. Nejsou dostupné žádné údaje.
Pacienti s poruchou funkce jater
U pacientů s mírnou poruchou funkce jater (Child-Pugh skóre 5–6) není nutno dávku nijak upravovat. Léčba přípravkem Ezantris se nedoporučuje u pacientů se středně závažnou (Child-Pugh skóre 7–9) nebo závažnou (skóre > 9 podle Child-Pugh) jaterní dysfunkcí (viz body 4.4 a 5.2).
Pacienti s poruchou funkce ledvin
U pacientů s poruchou funkce ledvin není nutno dávku nijak upravovat (viz bod 5.2).
4.3 Kontraindikace
Hypersenzitivita na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Pokud se Ezantris podává spolu se statinem, řiďte se prosím souhrnem údajů o přípravku (SPC) příslušného léčivého přípravku.
Terapie přípravkem Ezantris v kombinaci se statinem je kontraindikována během těhotenství a kojení.
Podávání přípravku Ezantris spolu se statinem je kontraindikováno u pacientů s aktivním jaterním onemocněním nebo nevysvětleným přetrvávajícím zvýšením sérových transamináz.
4.4 Zvláštní upozornění a opatření pro použití
Pokud se Ezantris podává spolu se statinem, řiďte se prosím souhrnem údajů o přípravku (SPC) příslušného léčivého přípravku.
Jaterní enzymy
-
V kontrolovaných studiích společného podávání ezetimibu se statinem bylo opakovaně pozorováno zvýšení transamináz (> 3krát horní hranice normálu [upper limit of normal, ULN]). Pokud se Ezantris podává současně se statinem, je nutno provést při zahájení terapie jaterní testy a řídit se doporučeními pro daný statin (viz bod 4.8).
-
V kontrolované klinické studii, kde bylo více než 9 000 pacientů s chronickým onemocněním ledvin randomizováno do skupiny léčené ezetimibem10 mg v kombinaci se simvastatinem v dávce 20 mg denně (n = 4 650) nebo do skupiny léčené placebem (n = 4 620) (medián doby sledování 4,9 roku), byla incidence následných zvýšení transamináz (> 3 X ULN) 0,7 % u ezetimibu v kombinaci se simvastatinem a 0,6 % u placeba (viz bod 4.8).
Kosterní sval
Po uvedení ezetimibu na trh byly popsány případy myopatie a rhabdomyolýzy. Většina pacientů, u nichž došlo k rozvoji rhabdomyolýzy, užívala spolu s ezetimebem i statin. Nicméně velmi vzácně byla rhabdomyolýza popisována i při monoterapii ezetimibem a také velmi vzácně byla popisována i po přidání ezetimibu k ostatním lékům, o nichž je známo, že jsou spojeny se zvýšeným rizikem rhabdomyolýzy. Pokud existuje podezření na myopatii na základě svalových příznaků nebo je diagnóza myopatie potvrzena zvýšením hladiny kreatinfosfokinázy (CPK) > 10násobek horní hranice normálu (ULN), je nutno Ezantris, všechny statiny a veškeré tyto jiné léky, které pacient současně užívá, okamžitě vysadit. Všechny pacienty, u nichž se zahajuje léčba přípravkem Ezantris, je nutno upozornit na riziko myopatie a požádat je, aby urychleně informovali lékaře o případné nevysvětlitelné svalové bolesti, citlivosti nebo slabosti (viz bod 4.8).
Ve studii IMPROVE-IT bylo randomizováno 18 144 pacientů s ischemickou chorobou srdeční a akutním koronárním syndromem v anamnéze do skupiny léčené ezetimibem/simvastatinem 10 mg/40 mg denně (n = 9 067) nebo 40 mg simvastatinu denně (n = 9 077). Během mediánu sledování 6,0 roku byla incidence myopatie u pacientů s ezetimibem/simvastatinem 0,2 % a u pacientů se simvastatinem 0,1 %, přičemž myopatie byla definována jako nevysvětlená svalová slabost nebo bolest s hladinou sérové kreatinkinázy (CK) > 10násobek ULN nebo s koncentrací CK > 5násobek a zároveň < 10násobek ULN ve dvou následných měřeních. Incidence rhabdomyolýzy byla u pacientů s ezetimibem/simvastatinem 0,1 % a u pacientů se simvastatinem 0,2 %, přičemž rhabdomyolýza byla definována jako nevysvětlená svalová slabost nebo bolest s hladinou sérové CK > 10násobek ULN s prokázaným renálním poškozením, > 5násobek a zároveň < 10násobek ULN ve dvou následných měřeních s prokázaným renálním poškozením nebo > 10 000 IU/l bez prokázaného renálního poškození. (Viz bod 4.8.)
-
V klinické studii, kde bylo více než 9 000 pacientů s chronickým onemocněním ledvin randomizováno do skupiny léčené ezetimibem 10 mg v kombinaci se simvastatinem v dávce 20 mg denně (n = 4 650) nebo do skupiny léčené placebem (n = 4 620) (medián doby sledování 4,9 roku), byla incidence myopatie/rhabdomyolýzy 0,2 % u ezetimibu v kombinaci se simvastatinem a 0,1 % u placeba (viz bod 4.8).
Pacienti s poruchou funkce jater
Vzhledem k neznámým účinkům zvýšené expozice ezetimibu u pacientů se středně závažnou nebo závažnou poruchou funkce jater se Ezantris u těchto pacientů nedoporučuje (viz bod 5.2).
Pediatrická populace
Účinnost a bezpečnost ezetimibu u pacientů ve věku 6 až 10 let s heterozygotní familiární nebo nefamiliární hypercholesterolemií byla vyhodnocována ve 12týdenní placebem kontrolované klinické studii. Účinky ezetimibu při době léčby delší než 12 týdnů nebyly u této věkové skupiny studovány (viz body 4.2, 4.8, 5.1 a 5.2).
Ezetimib nebyl studován u pacientů mladších než 6 let věku (viz body 4.2 a 4.8).
Účinnost a bezpečnost ezetimibu podávaného se simvastatinem pacientům ve věku 10 až 17 let s heterozygotní familiární hypercholesterolemií byla hodnocena v kontrolované klinické studii u dospívajících chlapců (Tannerův stupeň II nebo vyšší) a u dívek, které byly alespoň jeden rok po první menstruaci.
V této omezené kontrolované studii obecně nebyl u dospívajících chlapců a dívek zjištěn žádný detekovatelný vliv na růst nebo pohlavní vyzrávání, ani žádný vliv na délku menstruačního cyklu u dívek. Účinky ezetimibu na růst a pohlavní vyzrávání při trvání léčby > 33 týdnů však nebyly studovány (viz body 4.2. a 4.8.).
Bezpečnost a účinnost ezetimibu podávaného s dávkami simvastatinu vyššími než 40 mg denně nebyly u pediatrických pacientů ve věku 10 až 17 let hodnoceny.
Bezpečnost a účinnost ezetimibu podávaného společně se simvastatinem nebyla studována u pediatrických pacientů mladších než 10 let věku (viz body 4.2 a 4.8).
Dlouhodobá účinnost léčby ezetimibem u pacientů mladších 17 let ohledně snižování morbidity a mortality v dospělosti nebyla hodnocena.
Fibráty
Bezpečnost a účinnost ezetimibu podávaného spolu s fibráty nebyly stanoveny.
Při podezření na cholelitiázu se pacientům dostávajícím Ezantris a fenofibrát indikují vyšetření žlučníku a léčba musí být přerušena (viz body 4.5 a 4.8).
Cyklosporiny
Pokud jsou užívány cyklosporiny, je třeba dbát opatrnosti při zahájení podávání přípravku Ezantris. U pacientů užívajících Ezantris a cyklosporin je nutno sledovat koncentrace cyklosporinu (viz bod 4.5).
Antikoagulancia
Pokud se Ezantris přidá k warfarinu, jiným kumarinovým antikoagulanciím nebo fluindionu, je nutno odpovídajícím způsobem sledovat mezinárodní normalizovaný poměr (International Normalized Ratio, INR) (viz bod 4.5).
Pomocná látka
Pacienti se vzácnými dědičnými poruchami, jako je intolerance galaktózy, vrozený deficit laktázy nebo syndrom malabsorpce glukózy-galaktózy, nesmí tento lék užívat.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
-
V preklinických studiích se ukázalo, že ezetimib neindukuje enzymy cytochromu P450, které metabolizují léky. Nebyly pozorovány žádné klinicky významné farmakokinetické interakce mezi ezetimibem a přípravky, o nichž je známo, že jsou metabolizovány cytochromy P450 1A2, 2D6, 2C8, 2C9 a 3A4 nebo N-acetyltransferázou.
-
V klinických studiích zaměřených na interakce neměl ezetimib při současném podávání žádný vliv na farmakokinetiku dapsonu, dextromethorfanu, digoxinu, perorálních kontraceptiv (ethinylestradiol a levonorgestrel), glipizidu, tolbutamidu nebo midazolamu. Cimetidin podávaný současně s ezetimibem neměl na biologickou dostupnost ezetimibu žádný vliv.
Antacida
Současné podávání antacid snížilo rychlost absorpce ezetimibu, ale na biologickou dostupnost ezetimibu nemělo žádný vliv. Snížená rychlost absorpce se nepovažuje za klinicky významnou.
Kolestyramin
Současné podávání kolestyraminu snížilo průměrnou velikost plochy pod křivkou (AUC) celkového ezetimibu (ezetimib + ezetimib-glukuronid) přibližně o 55 %. Postupné snižování hladin cholesterolu nízkodenzitních lipoproteinů (low-density lipoprotein cholesterol, LDL-C) se jako důsledek přidání přípravku Ezantris ke kolestyraminu může touto interakcí oslabit (viz bod 4.2).
Fibráty
U pacientů dostávajících fenofibrát a Ezantris si lékaři musí být vědomi možného rizika cholelitiázy a onemocnění žlučníku (viz body 4.4 a 4.8).
Při podezření na cholelitiázu se pacientům dostávajícím Ezantris a fenofibrát indikují vyšetření žlučníku a léčba musí být přerušena (viz bod 4.8).
Současné podávání fenofibrátu nebo gemfibrozilu mírně zvýšilo celkové koncentrace ezetimibu (přibližně 1,5krát a 1,7krát v uvedeném pořadí).
Současné podávání ezetimibu s jinými fibráty nebylo studováno.
Fibráty mohou zvýšit vylučování cholesterolu do žluči vedoucí k cholelitiáze. Ve studiích prováděných na zvířatech ezetimib někdy zvýšil hladiny cholesterolu ve žlučníkové žluči, ne však u všech druhů (viz bod 5.3). Litogenní riziko spojené s terapeutickým použitím Ezantris nelze vyloučit.
Statiny
Při současném podávání ezetimibu s atorvastatinem, simvastatinem, pravastatinem, lovastatinem, fluvastatinem nebo rosuvastatinem nebyly zjištěny žádné klinicky významné farmakokinetické interakce.
Cyklosporin
Ve studii u osmi pacientů po transplantaci ledvin s clearance kreatininu > 50 ml/min, kteří byli na stabilní dávce cyklosporinu, vedlo podávání jednotlivé 10mg dávky ezetimibem ke 3,4násobnému (rozmezí 2,3–7,9násobné) zvýšení průměrné AUC celkového ezetimibu ve srovnání se zdravou populací z kontrolní skupiny, která dostávala ezetimib samostatně, z jiné studie (n = 17). V odlišné studii, vedené u pacienta po transplantaci ledvin se závažnou poruchou funkce ledvin, který dostával cyklosporin a další mnohonásobnou terapii, se projevila 12násobně vyšší expozice celkovému ezetimibu ve srovnání se souběžnými kontrolními skupinami, které dostávaly ezetimib samostatně. Ve studii se zkříženým uspořádáním (crossover) ve dvou obdobích, která se provedla s 12 zdravými jedinci, vedlo denní podávání ezetimibu v dávce 20 mg po dobu 8 dní spolu s jednorázovým podáním cyklosporinu v dávce 100 mg sedmý den k průměrnému 15% zvětšení plochy cyklosporinu pod křivkou (AUC) (rozmezí 10% pokles až 51% zvýšení) ve srovnání s jednorázovým podáním 100mg dávky samotného cyklosporinu. Kontrolovaná studie vlivu současného podávání ezetimibu na expozici cyklosporinu u pacientů po transplantaci ledvin nebyla dosud provedena. Při přidání přípravku Ezantris k terapii cyklosporinem je třeba dbát opatrnosti. Koncentrace cyklosporinu musí být sledovány u pacientů užívajících Ezantris a cyklosporin (viz bod 4.4).
Antikoagulancia
Současné podávání ezetimibu (10 mg jednou denně) nemělo žádný statisticky významný vliv na biologickou dostupnost warfarinu a protrombinový čas ve studii s 12 zdravými muži. Po uvedení na trh se však objevily zprávy o zvýšených hodnotách mezinárodního normalizovaného poměru (INR) u pacientů užívajících ezetimib přidaný k warfarinu nebo fluindionu. Pokud je Ezantris přidán k warfarinu, jiným kumarinovým antikoagulanciím nebo fluindionu, musí být INR patřičně sledován (viz bod 4.4).
Pediatrická populace
Studie interakcí byly provedeny pouze u dospělých.
4.6 Fertilita, těhotenství a kojení
Ezantris podávaný spolu se statinem je kontraindikován během těhotenství a kojení (viz bod 4.3), prosím, seznamte se s SPC konkrétního statinu.
Těhotenství
Ezantris by měl být podáván těhotným ženám, pouze pokud je to nezbytně nutné. Ohledně použití ezetimibu během těhotenství nejsou k dispozici žádné klinické údaje. Studie se zvířaty zabývající se použitím ezetimibu v monoterapii nepřinesly žádný důkaz přímých ani nepřímých škodlivých účinků na těhotenství, embryofetální vývoj, porod ani postnatální vývoj (viz bod 5.3).
Kojení
Ezantris nesmí být užíván během kojení. Studie na potkanech prokázaly, že se ezetimib vylučuje do mateřského mléka. Není známo, zda se ezetimib vylučuje do mateřského mléka žen.
Fertilita
O vlivu ezetimibu na lidskou fertilitu nejsou k dispozici žádné údaje z klinických studií. Ezetimib neměl žádný vliv na fertilitu samců ani samic potkanů (viz bod 5.3).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Studie hodnotící účinky na schopnost řídit a obsluhovat stroje nebyly provedeny. Pokud však řídíte vozidla nebo ovládáte stroje, měli byste brát v úvahu, že byla hlášena závrať.
4.8 Nežádoucí účinky
Tabulkový seznam nežádoucích účinků (klinické studie a zkušenosti po uvedení na trh)
V klinických studiích, které trvaly až 112 týdnů, byl ezetimib v dávce 10 mg denně podáván samostatně 2 396 pacientům, spolu se statinem 11 308 pacientům nebo s fenofibrátem 185 pacientům. Nežádoucí účinky byly obvykle mírné a přechodné. Celková incidence uváděných nežádoucích účinků byla u ezetimibu podobná jako u placeba. Podobně častost vysazení pro nežádoucí účinky ezetimibu a placeba byla srovnatelná.
Ezetimib podávaný samostatně nebo společně se statinem:
U pacientů užívajících ezetimib samostatně (n = 2 396) byly popsány následující nežádoucí účinky s častějším výskytem než u placeba (n = 1 159), nebo u pacientů užívajících ezetimib současně se statinem (n = 11 308) byly popsány následující nežádoucí účinky s častějším výskytem než u statinu podávaného samostatně (n = 9 361). Nežádoucí účinky při použití po uvedení na trh byly odvozeny z hlášení týkajících se ezetimibu podávaného v monoterapii nebo se statinem.
Četnosti výskytu byly definovány jako: velmi časté (> 1/10); časté (> 1/100 až < 1/10); méně časté (> 1/1 000 až <1/100); vzácné (> 1/10 000 až <1/1 000), velmi vzácné (< 1/10 000) a není známo (z dostupných údajů nelze určit)
| Monoterapie Ezantris | ||
| Třída orgánových systémů | Nežádoucí účinky | Frekvence |
| Vyšetření | zvýšení ALT a/nebo AST; zvýšení krevní CPK; zvýšení gamma-glutamyltransferázy; abnormální hodnoty testu jaterních funkcí | Méně časté |
| Respirační, hrudní a mediastinální poruchy | kašel | Méně časté |
| Gastrointestinální poruchy | bolest břicha; průjem; flatulence | Časté |
| dyspepsie; gastroezofageální refluxní nemoc; nauzea | Méně časté | |
| Poruchy svalové a kosterní soustavy a pojivové tkáně | artralgie; svalové spasmy; bolest krku | Méně časté |
| Poruchy metabolismu a výživy | snížená chuť k jídlu | Méně časté |
| Cévní poruchy | návaly horka; hypertenze | Méně časté |
| Celkové poruchy a reakce v místě aplikace | únava | Časté |
| Bolest na hrudi; bolest | Méně časté | |
| Další nežádoucí účinky při užívání | přípravku Ezantris současně se statinem | |
| Třída orgánových systémů | Nežádoucí účinky | Frekvence |
| Vyšetření | zvýšení ALT a/nebo AST | Časté |
| Poruchy nervového systému | Bolest hlavy | Časté |
| parestezie | Méně časté | |
| Gastrointestinální poruchy | sucho v ústech; gastritida | Méně časté |
| Poruchy kůže a podkožní tkáně | pruritus; vyrážka; kopřivka | |
| Poruchy svalové a kosterní soustavy a pojivové tkáně | myalgie | Časté |
| bolest zad; svalová slabost; bolest končetin | Méně časté | |
| Celkové poruchy a reakce v místě aplikace | astenie; periferní edém | Méně časté |
| Zkušenosti po uvedení na trh (se statinem nebo bez něj) | ||
| Třída orgánových systémů | Nežádoucí účinky | Frekvence |
| Poruchy krve a lymfatického systému | trombocytopenie | Není známo |
| Poruchy nervového systému | závrať; parestezie | Není známo |
| Respirační, hrudní a mediastinální poruchy | dyspnoe | Není známo |
| Gastrointestinální poruchy | pankreatitida; zácpa | Není známo |
| Poruchy kůže a podkožní tkáně | erythema multiforme | Není známo |
| Poruchy svalové a kosterní soustavy a pojivové tkáně | myalgie; myopatie/rhabdomyolýza (viz bod 4.4) | Není známo |
| Celkové poruchy a reakce v místě aplikace | astenie | Není známo |
| Poruchy imunitního systému | přecitlivělost, včetně vyrážky, kopřivky, anafylaxe a angioedému | Není známo |
| Poruchy jater a žlučových cest | hepatitida; cholelitiáza; cholecystitida | Není známo |
| Psychiatrické poruchy | deprese | Není známo |
Ezantris podávaný společně s fenofibrátem
Gastrointestinální poruchy: bolest břicha (časté)
-
V multicentrické, dvojitě zaslepené, placebem kontrolované klinické studii u pacientů se smíšenou hyperlipidemií se léčilo 625 pacientů po dobu až 12 týdnů a 576 pacientů po dobu až jednoho roku.
-
V této studii 172 pacientů léčených ezetimibem a fenofibrátem dokončilo 12 týdnů léčby a 230 pacientů léčených ezetimibem a fenofibrátem (včetně 109 pacientů, kteří dostávali ezetimib samostatně prvních 12 týdnů) dokončilo 1 rok léčby. Tato studie nebyla provedena ke srovnání léčebných skupin z hlediska málo často se vyskytujících příhod. Výskyt (95% CI) klinicky významných zvýšení (> 3× ULN, vyskytující se po sobě) sérových transamináz dosáhl po korekci na expozici léčbě při monoterapii fenofibrátem 4,5 % (1,9–8,8) a při podávání ezetimibu spolu s fenofibrátem 2,7 % (1,2–5,4). Odpovídající výskyt po cholecystektomii dosáhl při monoterapii fenofibrátem 0,6 % (0,0–3,1) a při podávání ezetimibu spolu s fenofibrátem 1,7 % (0,6–4,0) (viz body 4.4 a 4.5).
Pediatrická populace (ve věku 6 až 17 let)
Ve studii zahrnující pediatrické (6 až 10 let věku) pacienty s heterozygotní familiární nebo nefamiliární hypercholesterolemií (n = 138) bylo zvýšení ALT a/nebo AST (> 3násobek ULN, několikrát po sobě) pozorováno u 1,1 % (1 pacient) pacientů léčených ezetimibem ve srovnání s 0 % ve skupině léčené placebem. Neobjevilo se žádné zvýšení CPK (> 10násobek ULN). Nebyly hlášeny žádné případy myopatie.
-
V samostatné studii zahrnující dospívající (ve věku 10 až 17 let) pacienty s heterozygotní familiární hypercholesterolemií (n = 248) byla u 3 % (4 pacienti) pacientů léčených kombinací ezetimib/simvastatin pozorována zvýšení ALT a/nebo AST (> 3násobek ULN, několikrát po sobě)
v porovnání se 2 % (2 pacienti) ve skupině léčené simvastatinem v monoterapii; ohledně zvýšení CPK (> 10násobek ULN) byla tato čísla v uvedeném pořadí 2 % (2 pacienti) a 0 %. Nebyly hlášeny žádné případy myopatie.
Tato hodnocení nebyla uspořádána k porovnání vzácných nežádoucích účinků.
Pacienti s ischemickou chorobou srdeční a akutním koronárním syndromem v anamnéze
Ve studii IMPROVE-IT (viz bod 5.1), která zahrnovala 18 144 pacientů léčených ezetimibem/simvastatinem 10/40 mg (n = 9 067, z toho 6 % bylo titrováno na ezetimib/simvastatin 10/80 mg) nebo simvastatinem v dávce 40 mg (n = 9 077, z toho 27 % bylo titrováno na 80 mg simvastatinu), byly bezpečnostní profily během mediánu sledování 6,0 roku podobné. Kvůli výskytu nežádoucích účinků ukončilo léčbu 10,6 % pacientů léčených ezetimibem/simvastatinem a 10,1 % pacientů léčených simvastatinem. Incidence myopatie byla u pacientů s ezetimibem/simvastatinem 0,2 % a u pacientů se simvastatinem 0,1 %, přičemž myopatie byla definována jako nevysvětlená svalová slabost nebo bolest s hladinou sérové CK > 10násobek ULN nebo s koncentrací CK > 5násobek a zároveň < 10násobek ULN ve dvou následných měřeních. Incidence rhabdomyolýzy byla u pacientů s ezetimibem/simvastatinem 0,1 % a u pacientů se simvastatinem 0,2 %, přičemž rhabdomyolýza byla definována jako nevysvětlená svalová slabost nebo bolest s hladinou sérové CK > 10násobek ULN s prokázaným renálním poškozením, > 5násobek a zároveň < 10násobek ULN ve dvou následných měřeních s prokázaným renálním poškozením nebo > 10 000 IU/l bez prokázaného renálního poškození. Incidence následných zvýšení hladin transamináz (> 3 X ULN) byla 2,5 % u ezetimibu/simvastatinu a 2,3 % u simvastatinu. (Viz bod 4.4.) Nežádoucí účinky související se žlučníkem byly hlášeny u 3,1 % pacientů léčených ezetimibem/simvastatinem a u 3,5 % pacientů léčených simvastatinem. Incidence hospitalizace kvůli cholecystektomii byla v obou skupinách 1,5 %. Rakovina (definovaná jako jakákoli nová malignita) byla během studie diagnostikována u 9,4 % pacientů léčených ezetimibem/simvastatinem oproti 9,5 % pacientů léčených simvastatinem.
Pacienti s chronickým onemocněním ledvin
Ve studii „Study of Heart and Renal Protection“ (SHARP) (viz bod 5.1), která zahrnovala více než 9 000 pacientů léčených fixní dávkou ezetimibu 10 mg se simvastatinem 20 mg denně (n = 4 650) nebo placebem (n = 4 620), byly po dobu sledování s mediánem trvání 4,9 roku bezpečnostní profily srovnatelné. V této studii byly zaznamenávány pouze závažné nežádoucí účinky a ukončení léčby kvůli jakýmkoli nežádoucím účinkům. Míry ukončení léčby v důsledku nežádoucích účinků byly srovnatelné (10,4 % u pacientů léčených ezetimibem se simvastatinem, 9,8 % u pacientů léčených placebem). Incidence myopatie/rhabdomyolýzy byla 0,2 % u pacientů léčených ezetimibem se simvastatinem a 0,1 % u pacientů léčených placebem. Následné zvýšení transamináz (> 3 x ULN) se vyskytlo u 0,7 % pacientů léčených ezetimibem se simvastatinem v porovnání s 0,6 % pacientů léčených placebem. (Viz bod 4.4.) V této studii nebyla žádná statisticky významná zvýšení incidence předem specifikovaných nežádoucích účinků, včetně rakoviny (9,4 % u ezetimibu se simvastatinem, 9,5 % u placeba), hepatitidy, cholecystektomie nebo komplikací žlučníkových kamenů či pankreatitidy.
Laboratorní hodnoty:
-
V kontrolovaných klinických studiích monoterapie byla incidence klinicky významných zvýšení sérových transamináz (ALT a/nebo AST > 3krát ULN, opakovaně) podobná u ezetimibu (0,5 %) i placeba (0,3 %). Ve studiích současného podávání byla incidence 1,3 % u pacientů léčených ezetimibem spolu se statinem, a 0,4 % u pacientů léčených samotným statinem. Tato zvýšení byla obecně asymptomatická, nebyla spojena s cholestázou, a vrátila se po vysazení terapie nebo při pokračování léčby k normálu (viz bod 4.4).
V klinických studiích byla CPK > 10× ULN hlášena u 4 z 1 674 (0,2 %) pacientů při podávání samotného ezetimibu vs 1 ze 786 (0,1 %) pacientů při podávání placeba, a u 1 z 917 (0,1 %) pacientů při podávání ezetimibu v kombinaci se statinem vs 4 z 929 (0,4 %) pacientů při podávání samotného statinu. Při užívání ezetimibu nedošlo ke zvýšenému výskytu myopatie ani rhabdomyolýzy ve srovnání s hodnotami v odpovídajícím kontrolním rameni studie (placebo nebo samotný statin) (viz bod 4.4.).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
Webové stránky:
4.9 Předávkování
Podávání ezetimibu v klinických studiích v dávce 50 mg/den 15 zdravým dobrovolníkům po dobu až 14 dní, nebo 40 mg/den 18 pacientům s primární hypercholesterolemií po dobu až 56 dní, bylo celkově dobře snášeno. U zvířat nebyla po jednorázových perorálních dávkách 5 000 mg/kg ezetimibu potkanům a myším a 3 000 mg/kg psům pozorována žádná toxicita.
Bylo hlášeno několik případů předávkování ezetimibem; většina nebyla spojena s nežádoucími příhodami. Hlášené nežádoucí příhody nebyly závažné. V případě předávkování je nutno přijmout symptomatická a podpůrná opatření.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: jiné látky upravující hladinu lipidů, ATC kód: C10A X09
Mechanismus účinku
Ezantris patří mezi hypolipidemické látky nové skupiny, které selektivně inhibují intestinální absorpci cholesterolu a příbuzných rostlinných sterolů. Ezantris je účinný po perorálním podání a má mechanismus účinku, který se liší od mechanismu účinku jiných skupin látek snižujících hladiny cholesterolu (např. statiny, sekvestranty žlučových kyselin [pryskyřice], deriváty kyseliny fibrové a rostlinné stanoly). Molekulárním cílem ezetimibu je přenašeč sterolu, Niemann-Pick C1-Like 1 (NPC1L1), který je odpovědný za intestinální absorpci cholesterolu a fytosterolů.
Ezetimib se lokalizuje v kartáčovém lemu tenkého střeva a inhibuje absorpci cholesterolu, což vede ke snížení přísunu cholesterolu ze střev do jater; statiny snižují syntézu cholesterolu v játrech a dohromady tyto rozdílné mechanismy zajišťují vzájemně se doplňující snížení hladiny cholesterolu. Ve dvoutýdenní klinické studii u 18 pacientů s hypercholesterolemií inhiboval Ezantris intestinální absorpci cholesterolu ve srovnání s placebem o 54 %.
Farmakodynamické účinky
Byla provedena řada preklinických studií s cílem zjistit selektivitu ezetimibu při inhibici absorpce cholesterolu. Ezetimib inhiboval absorpci [14C]-cholesterolu bez účinku na absorpci triglyceridů, mastných kyselin, žlučových kyselin, progesteronu, ethinylestradiolu nebo v tucích rozpustných vitamínů A a D.
Epidemiologické studie prokázaly, že kardiovaskulární morbidita a mortalita se mění přímo úměrně s hladinou celkového cholesterolu a LDL-C, a nepřímo úměrně s hladinou HDL-C.
Užívání přípravku Ezantris zároveň se statinem účinně snižuje riziko kardiovaskulárních příhod u pacientů s ischemickou chorobou srdeční a akutním koronárním syndromem v anamnéze.
Klinická účinnost a bezpečnost
-
V kontrolovaných klinických studiích ezetimib podávaný jako monoterapie nebo spolu se statinem významně snižoval celkový cholesterol (total-C), cholesterol s nízkou hustotou lipoproteinu (LDL-C), apolipoprotein B (Apo B) a triglyceridy (TG) a zvyšoval cholesterol s vysokou hustotou lipoproteinu (HDL-C) u pacientů s hypercholesterolemií.
Primární hypercholesterolemie
-
V dvojitě zaslepené, placebem kontrolované, 8týdenní studii bylo 769 pacientů s hypercholesterolemií, kteří již dostávali statin v monoterapii, a nedosáhli cílové hodnoty LDL-C podle Národního programu pro osvětu ve snižování hladin cholesterolu (National Cholesterol Education Program – NCEP) – (2,6
-
4,1 mmol/l, 100–160 mg/dl, podle výchozích charakteristik) randomizováno do skupin, které dostávaly buď ezetimib 10 mg nebo placebo navíc k již probíhající léčbě statiny.
-
V multicentrické, dvojitě zaslepené, kontrolované klinické studii (ENHANCE) bylo randomizováno 720 pacientů s heterozygotní familiární hypercholesterolemií do skupiny léčené po dobu 2 let ezetimibem v dávce 10 mg v kombinaci se simvastatinem v dávce 80 mg (n = 357) nebo simvastatinem v dávce 80 mg (n = 363). Primárním cílem studie bylo zjištění účinku léčby kombinací ezetimib/simvastatin na tloušťku intimy-medie (intima-media thickness – IMT) karotidy v porovnání s monoterapií simvastatinem. Vliv tohoto náhradního markeru na kardiovaskulární morbiditu a mortalitu stále není prokázán.
Primární cílový ukazatel, změna průměrné hodnoty IMT ve všech šesti segmentech karotidy, se mezi oběma léčenými skupinami významně nelišil (p = 0,29), jak bylo změřeno pomocí ultrazvuku v B-modu. U ezetimibu v dávce 10 mg v kombinaci se simvastatinem v dávce 80 mg nebo u samotného simvastatinu v dávce 80 mg se za 2 roky trvání studie tloušťka intimy-medie zvětšila o 0,0111 mm, respektive o 0,0058 mm (výchozí průměrná hodnota IMT karotidy 0,68 mm, respektive 0,69 mm).
Ezetimib v dávce 10 mg v kombinaci se simvastatinem v dávce 80 mg snižoval LDL-C, celkový cholesterol, Apo B a TG významně více než samotný simvastatin v dávce 80 mg. Procentuální vzestup HDL-C byl v obou léčených skupinách podobný. Nežádoucí účinky hlášené u ezetimibu v dávce 10 mg v kombinaci se simvastatinem v dávce 80 mg byly konzistentní s jeho známým bezpečnostním profilem.
Pediatrická populace
-
V multicentrické, dvojitě zaslepené, kontrolované studii bylo 138 pacientů (59 chlapců a 79 dívek) ve věku 6 až 10 let (střední hodnota věku 8,3 roku) s heterozygotní familiární nebo nefamiliární hypercholesterolemií (HeFH, Heterozygous familial hypercholesterolaemia) s výchozími hladinami LDL-C mezi 3,74 a 9,92 mmol/l randomizováno buď do skupiny léčené ezetimibem 10 mg, nebo placebem po dobu 12 týdnů.
-
V multicentrické, dvojitě zaslepené, kontrolované studii bylo 142 chlapců (Tannerův stupeň II a vyšší) a 106 dívek po první menstruaci, ve věku 10 až 17 let (střední hodnota věku 14,2 roku) s heterozygotní familiární hypercholesterolemií (HeFH) s výchozími hodnotami LDL-C mezi 4,1 a 10,4 mmol/l, randomizováno buď do skupiny léčené ezetimibem 10 mg v kombinaci se simvastatinem (10, 20 nebo 40 mg) nebo do skupiny léčené simvastatinem (10, 20 nebo 40 mg) samotným po dobu 6 týdnů, do skupiny léčené kombinací ezetimibu a 40 mg simvastatinu nebo do skupiny léčené 40 mg simvastatinu samotného po dobu dalších 27 týdnů a do skupiny léčené v otevřeném uspořádání ezetimibem a simvastatinem (10 mg, 20 mg nebo 40 mg) po následujících 20 týdnů.
-
V 6. týdnu ezetimib v kombinaci se simvastatinem (všechny dávky) v porovnání se simvastatinem (všechny dávky) samotným významně snižoval celkový cholesterol (38 % vs 26 %), LDL-C (49 % vs 34 %), Apo-B (39 % vs 27 %) a non-HDL-C (47 % vs 33 %). Výsledky byly ohledně TG a HDL-C (-17 % vs –12 % a +7 % vs +6 %, v uvedeném pořadí) u obou skupin podobné. Ve 33. týdnu byly výsledky konzistentní s výsledky v 6. týdnu, přičemž významně více pacientů léčených kombinací ezetimibu a 40 mg simvastatinu (62 %) dosáhlo ideálního cíle NCEP AAP (< 2,8 mmol/l [110 mg/dl]) ohledně LDL-C v porovnání s pacienty léčenými 40 mg simvastatinu (25 %). V 53. týdnu, což je konec otevřeného prodloužení studie, byly účinky na parametry lipidů zachovány.
Účinnost a bezpečnost ezetimibu podávaného s dávkami simvastatinu vyššími než 40 mg denně nebyla u pediatrických pacientů ve věku 10 až 17 let hodnocena. Bezpečnost a účinnost ezetimibu podávaného současně se simvastatinem nebyla u pediatrických pacientů ve věku < 10 let studována. Dlouhodobá účinnost léčby ezetimibem u pacientů mladších 17 let ohledně snižování morbidity a mortality v dospělosti nebyla hodnocena.
Prevence kardiovaskulárních příhod
IMProved Reduction of Outcomes: Vytorin Efficacy International Trial (IMPROVE-IT) byla multicentrická randomizovaná dvojitě zaslepená studie s aktivním komparátorem, do níž bylo zařazeno 18 144 pacientů během 10 dnů po hospitalizaci kvůli akutnímu koronárnímu syndromu (AKS; buď infarktu myokardu, nebo nestabilní angině pectoris). Hladina LDL-C při projevení AKS byla < 3,2 mmol/l (< 125 mg/dl) u pacientů, kteří neužívali hypolipidemickou léčbu, nebo < 2,6 mmol/l (< 100 mg/dl) u pacientů, kteří dostávali hypolipidemickou léčbu. Všichni pacienti byli v poměru 1:1 randomizováni do skupiny léčené ezetimibem/simvastatinem 10/40 mg (n = 9 067) nebo simvastatinem 40 mg (n = 9 077) a sledováni po medián doby sledování 6,0 roku.
Průměrný věk pacientů byl 63,6 roku, 76 % tvořili muži, 84 % byli běloši a 27 % pacientů mělo diabetes mellitus. Průměrná hodnota LDL-C při příhodě, která byla kvalifikující pro zařazení do studie, byla 2,1 mmol/l (80 mg/dl) u pacientů, kteří dostávali hypolipidemickou léčbu (n = 6 390), a 2,6 mmol/l (101 mg/dl) u těch, kteří předtím nedostávali hypolipidemickou léčbu (n = 11 594). Před hospitalizací kvůli příhodě AKS kvalifikující ke vstupu do studie užívalo 34 % pacientů statin. Po jednom roce byla průměrná hodnota LDL-C u pacientů, kteří pokračovali v léčbě, 1,4 mmol/l (53,2 mg/dl) ve skupině s ezetimibem/simvastatinem a 1,8 mmol/l (69,9 mg/dl) ve skupině se samotným simvastatinem. Hladiny lipidů byly obecně získány u pacientů, kteří pokračovali v léčbě v rámci studie.
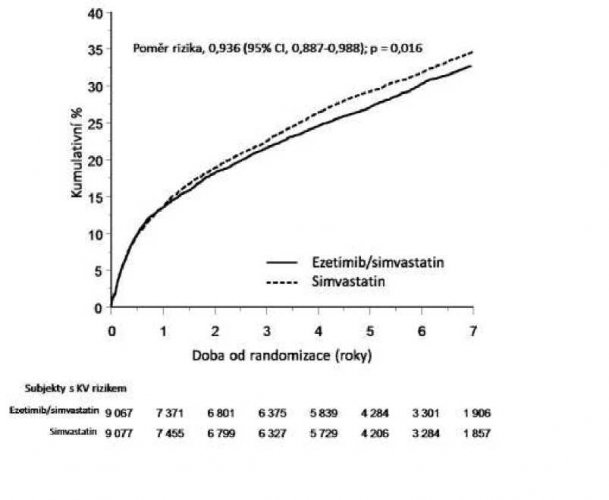
Primárním cílovým ukazatelem byl složený ukazatel zahrnující úmrtí z kardiovaskulárních příčin, velké koronární příhody (definované jako nefatální infarkt myokardu, popsaná nestabilní angina pectoris vyžadující hospitalizaci, nebo jakákoli koronární revaskularizace prováděná nejméně 30 dní po randomizaci) a nefatální cévní mozkovou příhodu. Studie prokázala, že léčba ezetimibem přidaným k simvastatinu ve srovnání se samotným simvastatinem poskytuje rostoucí přínos ve formě snížení výskytu primárního cílového ukazatele složeného z úmrtí z kardiovaskulárních příčin, velké koronární příhody a nefatální cévní mozkové příhody (relativní snížení rizika je 6,4 %, p = 0,016). Primární cílový ukazatel se vyskytl u 2 572 z 9 067 pacientů ze skupiny s ezetimibem/simvastatinem (pravděpodobnost výskytu za 7 let byla dle Kaplan-Meierovy (KM) metody 32,72 %) a u 2 742 z 9 077 pacientů ze skupiny se samotným simvastatinem (pravděpodobnost výskytu za 7 let byla dle KM metody 34,67 %). (Viz Graf 1 a Tabulka 1.) Předpokládá se, že podobný rostoucí přínos poskytuje také kombinace s jinými statiny účinnými ve snížování rizika kardiovaskulárních příhod. Celková úmrtnost se v této vysoce rizikové skupině nezměnila (viz Tabulka 1).
Ve studii byl pozorován celkový přínos pro všechny typy cévní mozkové příhody, nicméně bylo zaznamenáno malé nesignifikantní zvýšení rizika u hemoragické cévní mozkové příhody ve skupině s ezetimibem a simvastatinem ve srovnání se skupinou se samotným simvastatinem (viz Tabulka 1). Riziko hemoragické cévní mozkové příhody pro ezetimib podávaný se statiny s vyšší účinností nebylo hodnoceno v dlouhodobých studiích.
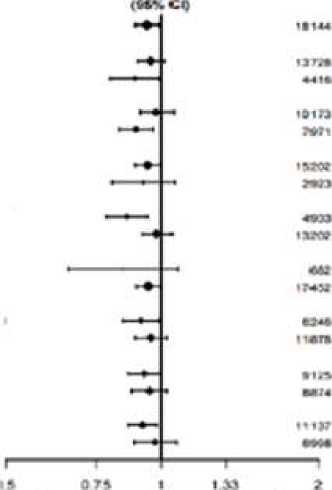
Léčebný účinek kombinace ezetimib/simvastatin byl obecně konzistentní napříč celkovými výsledky mnoha podskupin, dělených podle pohlaví, věku, rasy, diabetu mellitus v anamnéze, počáteční hladiny lipidů, předchozí léčby statiny, cévní mozkové příhody v anamnéze a hypertenze.
Graf 1: Účinek ezetimibu/simvastatinu na primární cílový ukazatel složený z úmrtí z kardiovaskulárních příčin, velké koronární příhody nebo nefatální cévní mozkové příhody
Poměr rFúka, 0.536 (95H CL 0.887 0,983); p – 0.01G
Sutjcktv s KV ruifctnri
Lzatunib/siniMartatin rjuij/
*^'iiva\ljl!ii gfl Jf
3301
3284
1 «K
1 os?
p 25
3 20 E
“15’
2 3 4 5
Doba ad randomizace (.roky)
7 37t
Z4M>
---- Ezet imib/simvastatin ----- Simvastatin
ÉBOl
6 rx
6 375
6 32/
5630
!j m
4284
4206
Podskupina
Všecinv podskupiny
Pohla w'

prodělaná mrtvce
Ejclim ib/iiivrnailaím {fZ/SJ ilc nicni
Simvasíladn ($] zlepšeni
KAvkajska
Nekavkai&kd] biabetřs Mellltus v anamnéze
Přřčhdhůit užíváni Statinů
Terapie ilatinem ipči vi
0«?i terapie štafl nem <xi vstupu to tfudie
Výchozí hodnota LDL-C Ifng./dLi
<95 (mediáni
>95 (mediáni
HfVP^Ttmrp v a namnoze
Anči
Ne
Tabulka 1
Velké kardiovaskulární příhody podle skupin u všech pacientů randomizovaných v IMPROVE-IT
| Výsledek | Ezetimib/Simvastatin 10/40 mga (n=9067) | Simvastatin 40 mgb (n=9077) | Poměr rizika (95% CI)p-hodnota |
| n K-M % c | n K-M % c |
Primární složený cílový ukazatel účinnosti
(Úmrtí z kardiovaskulárních příčin, velké koronární příhody a nefatální cévní mozková 2572 příhoda)______________________________________
Sekundární složený cílový ukazatel účinnosti
Úmrtí z důvodu ICHS, nefatální infarkt myokardu, urgentní koronární revaskularizace po 30 dnech_____________________
Velká koronární příhoda, nefatální cévní mozková příhoda, úmrtí (z jakékoli příčiny)________________________
Úmrtí z kardiovaskulárních příčin, nefatální infarkt myokardu, nestabilní angina pectoris vyžadující hospitalizaci, 2716 jakákoli revaskularizace, nefatální cévní mozková příhoda________
Složky primárního složeného cílového ukazatele a vybrané cílové ukazatele účinnosti (první výskyt dané příhody v jakékoli chvíli)___________
Úmrtí z kardiovaskulárních příčin______________________
Velká koronární příhoda:
32.72%
2742 34.67%0.936 (0.887,0.016
0.988)
1322
3089
537
17.52%
1448
18.88%0.912 (0.847,0.016
0.983)
38.65%
34.49%
6.89%
3246 40.25%0.948 (0.903,0.035
0.996)
0.945 (0.897,
2869 36.20%0.945 (0.897,0.035
0.996)
538
6.84%
1.000 (0.887,
1.127)
| – nefatální infarkt myokardu | 945 | 12.77% | 1083 | 14.41% | 0.871 (0.798, 0.950) | 0.002 |
| – nestabilní angina pectoris vyžadující hospitalizaci | 156 | 2.06% | 148 | 1.92% | 1.059 (0.846, 1.326) | 0.618 |
| – koronární revaskularizace | 1690 | 21.84% | 1793 | 23.36% | 0.947 (0.886, | 0.107 |
| po 30 dnech | 1.012) | |||||
| Nefatální cévní mozková | 245 | 3.49% | 305 | 4.24% | 0.802 (0.678, | 0.010 |
| příhoda | 0.949) | |||||
| Infarkt myokardu (fatální i nefatální) | 977 | 13.13% | 1118 | 14.82% | 0.872 (0.800, 0.950) | 0.002 |
| Cévní mozková příhoda (fatální i nefatální) | 296 | 4.16% | 345 | 4.77% | 0.857 (0.734, 1.001) | 0.052 |
| – nehemoragická cévní mozková příhoda d | 242 | 3.48% | 305 | 4.23% | 0.793 (0.670, 0.939) | 0.007 |
| – hemoragická cévní mozková příhoda | 59 | 0.77% | 43 | 0.59% | 1.377 (0.930, 2.040) | 0.110 |
| Úmrtí z jakékoli příčiny | 1215 | 15.36% | 1231 | 15.28% | 0.989 (0.914, 1.070) | 0.782 |
a 6% pacientů bylo titrováno na ezetimib/simvastatin 10/80 mg.
b 27% pacientů bylo titrováno na simvastatin 80 mg.
c Kaplan-Meierův odhad pro 7 let.
d zahrnuje ischemickou cévní mozkovou příhodu nebo cévní mozkovou příhodu neurčeného typu
Prevence velkých cévních příhod při chronickém onemocnění ledvin
Studie „Study of Heart and Renal Protection“ (SHARP) byla mezinárodní, randomizovanou, placebem kontrolovanou, dvojitě zaslepenou studií provedenou na 9 438 pacientech s chronickým onemocněním ledvin, z nichž třetina byla při zahájení studie na dialýze. Do skupiny léčené ezetimibem 10 mg se simvastatinem v dávce 20 mg bylo randomizováno celkem 4 650 pacientů a do skupiny léčené placebem 4 620 pacientů, přičemž medián doby sledování pacientů byl 4,9 let. Střední hodnota věku pacientů byla 62 let, přičemž 63 % z nich byli muži, 72 % běloši, 23 % diabetici, přičemž u těch pacientů, kteří nebyli na dialýze, byla střední hodnota odhadované rychlosti glomerulární filtrace (eGFR) 26,5 ml/min/1,73 m2. Kritéria pro zařazení týkající se lipidů nebyla stanovena. Střední hodnota LDL-C při zařazení byla 108 mg/dl. V porovnání s placebem došlo po jednom roce, a to i u pacientů, kteří již nepodstupovali hodnocenou léčbu, ke snížení LDL-C o 26 % u simvastatinu 20 mg samotného a o 38 % u ezetimibu 10 mg se simvastatinem v dávce 20 mg.
Primární porovnání specifikované v protokolu studie SHARP byla analýza léčených dle záměru (intention-to-treat analysis) s ohledem na „velké cévní příhody“ (definované jako nefatální infarkt myokardu nebo srdeční smrt, cévní mozková příhoda nebo revaskularizace) pouze u těch pacientů, kteří byli původně randomizováni do skupiny léčené ezetimibem se simvastatinem (n = 4 193) nebo placebem (n = 4 191). Sekundární analýzy zahrnovaly stejné složené kritérium analyzované u celé kohorty randomizované (na začátku studie nebo po 1 roce) do skupiny léčené ezetimibem se simvastatinem (n = 4 650) nebo placebem (n = 4 620), stejně jako komponenty tohoto složeného kritéria.
Analýza primárních kritérií hodnocení prokázala, že ezetimib se simvastatinem významně snižoval riziko velkých cévních příhod (749 pacientů s příhodami ve skupině léčené placebem vs. 639 ve skupině léčené ezetimibem a simvastatinem) s relativním snížením rizika 16 % (p = 0,001).
Uspořádání této studie nicméně neumožnilo zjistit samostatný podíl monokomponentního ezetimibu na účinnosti, jež vedla k významnému snížení rizika velkých cévních příhod u pacientů s chronickým onemocněním ledvin.
Jednotlivé typy velkých cévních příhod u všech randomizovaných pacientů jsou uvedeny v Tabulce 2. Ezetimib v kombinaci se simvastatinem významně snižoval riziko cévní mozkové příhody a jakékoli revaskularizace při nevýznamných numerických rozdílech upřednostňujících ezetimib v kombinaci se simvastatinem při nefatálním infarktu myokardu a srdeční smrti.
Tabulka 2
iVelkécévní£ríhodydleJéčené skupinyuíVŠechrandomizovaných£a£ientůve studiiíSHARPa
| Výsledek | Ezetimibe 10 mg kombinovaný se simvastatinem 20 mg (n=4650) | Placebo (n=4620) | Poměr rizik (95% CI) | p-hodnota |
| Velké cévní příhody | 701 (15.1%) | 814 (17.6%) | 0.85 (0.77–0.94) | 0.001 |
| Nefatální infarkt myokardu | 134 (2.9%) | 159 (3.4%) | 0.84 (0.66–1.05) | 0.12 |
| Srdeční smrt | 253 (5.4%) | 272 (5.9%) | 0.93 (0.78–1.10) | 0.38 |
| Jakákoli cévní mozková příhoda | 171 (3.7%) | 210 (4.5%) | 0.81 (0.66–0.99) | 0.038 |
| Nehemoragická cévní mozková příhoda | 131 (2.8%) | 174 (3.8%) | 0.75 (0.60–0.94) | 0.011 |
| Hemoragická cévní mozková příhoda | 45 (1.0%) | 37 (0.8%) | 1.21 (0.78–1.86) | 0.40 |
| Jakákoli revaskularizace | 284 (6.1%) | 352 (7.6%) | 0.79 (0.68–0.93) | 0.004 |
| Velké aterosklerotické příhodyb | 526(11.3%) | 619(13.4%) | 0.83 (0.74–0.94) | 0.002 |
aAnalýza podle léčebného záměru (Intention-to-treat analysis) u všech pacientů studie SHARP randomizovaných do skupiny léčené ezetimibem v kombinaci se simvastatinem nebo placebem buď na začátku studie, nebo po 1 roce bVelké cévní příhody; definovány jako složené kritérium zahrnující nefatální infarkt myokardu, koronární smrt, nehemoragickou cévní mozkovou příhodu nebo jakoukoli revaskularizaci
Celkové snížení LDL cholesterolu dosažené podáním ezetimibu kombinovaného se simvastatinem bylo nižší u pacientů s nižší výchozí hladinou LDL-C (< 2,5 mmol/l) a pacientů, kteří byli při vstupu do studie na dialýze, než u ostatních pacientů a odpovídající snížení rizika u těchto dvou skupin bylo potlačeno.
Homozygotní familiární hypercholesterolemie (HoHF)
Do dvojitě zaslepené, randomizované 12týdenní studie bylo zařazeno 50 pacientů s klinickou a/nebo genotypovou diagnózou HoFH, kteří dostávali atorvastatin nebo simvastatin (40 mg), se současnou aferézou LDL nebo bez ní. Ezetimib, podávaný spolu s atorvastatinem (40 nebo 80 mg) nebo se simvastatinem (40 nebo 80 mg) snížil, ve srovnání se zvýšením dávky simvastatinu nebo atorvastatinu v monoterapii ze 40 na 80 mg, statisticky významně LDL-C o 15 %.
Stenóza aorty
Studie The Simvastatin and Ezetimibe for the Treatment of Aortic Stenosis (SEAS) byla
multicentrickou, dvojitě zaslepenou, placebem kontrolovanou studií s mediánem doby trvání 4,4 roku, která se prováděla na 1 873 pacientech s asymptomatickou stenózou aorty (AS), doloženou Dopplerovým efektem měřenou maximální výtokovou rychlostí z aorty v rozmezí od 2,5 do 4,0 m/s. Do studie byli zařazeni pouze pacienti, u kterých se nemělo za to, že potřebují léčbu statiny za účelem snížení rizika aterosklerotického kardiovaskulárního onemocnění. Pacienti byli randomizováni v poměru 1:1 do skupiny léčené placebem nebo ezetimibem v dávce 10 mg a simvastatinem v dávce 40 mg denně.
Primárním cílovým ukazatelem byla kombinace závažných kardiovaskulárních příhod (major cardiovascular event; MCE) sestávajících z kardiovaskulárního úmrtí, náhrady aortální chlopně (aortic valve replacement – AVR), městnavého srdečního selhání (congestive heart failure – CHF) v důsledku progrese AS, nefatálního infarktu myokardu, koronárního arteriálního bypassu, perkutánní koronární intervence, hospitalizace kvůli nestabilní angině pectoris a nehemoragické cévní mozkové příhody. Klíčovými sekundárními cílovými ukazateli byla kombinace podskupin kategorií příhod primárních cílových ukazatelů.
V porovnání s placebem kombinace ezetimib/simvastatin v dávce 10/40 mg významně nesnižovala riziko MCE. Primární výsledek se objevil u 333 pacientů (35,3 %) ve skupině léčené kombinací ezetimib/simvastatin a u 355 pacientů (38,2 %) ve skupině léčené placebem (poměr rizik ve skupině léčené kombinací ezetimib/simvastatin, 0,96; 95% interval spolehlivosti, 0,83 až 1,12; p = 0,59). Náhrada aortální chlopně byla provedena u 267 pacientů (28,3 %) ve skupině léčené kombinací ezetimib/simvastatin a u 278 pacientů (29,9 %) ve skupině léčené placebem (poměr rizik, 1,00; 95% interval spolehlivosti, 0,84 až 1,18; p = 0,97). Méně pacientů bylo postiženo ischemickými kardiovaskulárními příhodami ve skupině léčené kombinací ezetimib/simvastatin (n = 148), než ve skupině léčené placebem (n = 187) (poměr rizik, 0,78; 95% interval spolehlivosti, 0,63 až 0,97; p = 0,02), zejména díky menšímu počtu pacientů, kterým byl zaveden koronární arteriální bypass.
Ve skupině léčené kombinací ezetimib/simvastatin se vyskytla častěji rakovina (105 oproti 70, p = 0,01). Klinická relevance tohoto zjištění není jasná, protože ve větší studii SHARP se celkový počet pacientů s jakoukoli vyskytnuvší se rakovinou (438 ve skupině léčené kombinací ezetimib/simvastatin oproti 439 ve skupině léčené placebem) nelišil. Navíc ve studii IMPROVE-IT se celkový počet pacientů s jakoukoli novou malignitou signifikantně nelišil (853 ve skupině s ezetimibem/simvastatinem oproti 863 ve skupině se simvastatinem), a proto zjištění studie SEAS nemohla být studií SHARP, ani studií IMPROVE-IT potvrzena.
5.2 Farmakokinetické vlastnosti
Absorpce
Po perorálním podání se ezetimib rychle vstřebává a ve velké míře se váže na farmakologicky aktivní fenolový glukuronid (ezetimib-glukuronid). Průměrných maximálních plazmatických koncentrací (C max ) se dosahuje během 1 až 2 hodin u ezetimibu-glukuronidu a 4 až 12 hodin u ezetimibu. Absolutní biologickou dostupnost ezetimibu nelze určit, protože látka je prakticky nerozpustná ve vodných médiích vhodných pro injekční podání.
Současné podávání jídla (jídla s vysokým obsahem tuků nebo bez tuku) nemělo na perorální biologickou dostupnost ezetimibu žádný vliv, pokud se podal ve formě Ezantris 10 mg tablety. Ezantris lze podávat s jídlem nebo bez něj.
Distribuce
Ezetimib a ezetimib-glukuronid se vážou z 99,7 % a 88 až 92 % na bílkoviny v lidské plazmě (v uvedeném pořadí).
Biotransformace
Ezetimib je metabolizován převážně v tenkém střevě a v játrech cestou konjugace s glukuronidem (reakce II. fáze), s následným vyloučením žlučí. Minimální oxidativní metabolismus (reakce I. fáze) byl pozorován u všech hodnocených živočišných druhů. Ezetimib a ezetimib-glukuronid jsou hlavními látkami vznikajícími z léčivé látky, které lze zjistit v plazmě, a představují přibližně 10–20 % a 80–90 % celkového množství léčivé látky v plazmě (v uvedeném pořadí). Jak ezetimib, tak i ezetimib-glukuronid se pozvolna vylučují z plazmy s prokazatelnou významnou enterohepatální recyklací. Poločas pro ezetimib a ezetimib-glukuronid je přibližně 22 hodin.
Eliminace
Po perorálním podání 14C-ezetimibu (20 mg) lidem představoval celkový ezetimib přibližně 93 % celkové radioaktivity v plazmě. Přibližně 78 % a 11 % podané radioaktivity bylo v průběhu 10denního sběrného období izolováno ze stolice a z moči (v uvedeném pořadí). Po 48 hodinách nebyly v plazmě žádné detekovatelné hladiny radioaktivity.
Speciální populace
Pediatrická populace
Farmakokinetika ezetimibu je u dětí starších 6 let i u dospělých podobná. Farmakokinetické údaje pro pediatrickou populaci < 6 let věku nejsou k dispozici. Klinické zkušenosti u pediatrických a dospívajících pacientů zahrnují pacienty s HoFH nebo HeFH.
Starší pacienti
Plazmatické koncentrace celkového ezetimibu jsou u starších osob (> 65 let) přibližně dvakrát vyšší než u mladých osob (18 až 45 let). Snížení LDL-C a profil bezpečnosti u starších a mladých jedinců léčených Ezantris jsou srovnatelné. Proto není nutno dávku u starších jedinců nijak upravovat.
Porucha funkce jater
Po jednorázové 10mg dávce ezetimibu se průměrná AUC pro celkový ezetimib u pacientů s mírnou poruchou funkce jater (skóre 5–6 podle Child-Pugh) zvětšila ve srovnání se zdravými jedinci přibližně 1,7krát. Ve 14denní studii s více dávkami (10 mg denně) u pacientů se středně závažnou poruchou funkce jater (skóre 7–9 podle Child-Pugh) byla 1. a 14. den průměrná hodnota AUC pro celkový ezetimib ve srovnání se zdravými jedinci přibližně čtyřnásobná. U pacientů s mírnou poruchou funkce jater není nutno dávku nijak upravovat. Vzhledem k neznámým účinkům zvýšené expozice ezetimibu u pacientů se středně závažnou nebo závažnou (skóre > 9 podle Child-Pugh) poruchou funkce jater se nedoporučuje těmto pacientům Ezantris podávat (viz bod 4.4).
Porucha funkce ledvin
Po jednorázové 10mg dávce ezetimibu pacientům se závažným onemocněním ledvin (n = 8; průměrná hodnota CrCl < 30 ml/min/1,73 m2), byla průměrná hodnota AUC pro celkový ezetimib ve srovnání se zdravými jedinci (n = 9) zvětšená přibližně 1,5krát. Tento výsledek není považován za klinicky významný. U pacientů s poruchou funkce ledvin není nutno dávku nijak upravovat.
Další pacient v dané studii (po transplantaci ledvin, který dostával více přípravků, včetně cyklosporinu) vykazoval 12násobně větší expozici celkovému ezetimibu.
Pohlaví
Plazmatické koncentrace celkového ezetimibu jsou u žen mírně vyšší (přibližně 20 %) než u mužů. Snížení LDL-C a profil bezpečnosti jsou u mužů i žen léčených přípravkem Ezantris srovnatelné. Proto není nutno dávku podle pohlaví nijak upravovat.
5.3 Předklinické údaje vztahující se k bezpečnosti
Studie se zvířaty hodnotící chronickou toxicitu ezetimibu nezjistily žádné cílové orgány pro toxické účinky. U psů, jimž byl podáván po dobu 4 týdnů ezetimib (> 0,03 mg/kg/den), se koncentrace cholesterolu ve žlučníkové žluči zvýšila 2,5 až 3,5krát. V jednoleté studii u psů, kteří dostávali dávky až 300 mg/kg/den, však nebyla pozorována zvýšená incidence cholelitiázy ani jiné hepatobiliární účinky. Význam těchto dat pro člověka není znám. Litogenní riziko v souvislosti s terapeutickým používáním ezetimibu nelze vyloučit.
Ve studiích kombinované terapie ezetimibem a statiny byly pozorovány toxické účinky v podstatě stejné jako účinky normálně dávané do souvislosti se statiny. Některé z toxických účinků byly výraznější než ty, které byly pozorovány během léčby samotnými statiny. To se připisuje farmakokinetickým a farmakodynamickým interakcím při kombinované terapii. V klinických studiích k těmto interakcím nedocházelo. Myopatie se vyskytly u potkanů pouze po expozici dávkám několikanásobně vyšším než je terapeutická dávka pro člověka (přibližně 20násobek hodnoty AUC pro statiny a 500 až 2 000násobek hodnoty AUC pro aktivní metabolity).
V řadě analýz in vivo a in vitro nevykazoval ezetimib, podávaný samostatně nebo v kombinaci se statiny, žádný genotoxický potenciál. Dlouhodobé testy karcinogenity ezetimibu byly negativní. Ezetimib neměl žádný vliv na plodnost samců ani samic potkanů, ani se neukázal být teratogenní u potkanů nebo králíků, ani neovlivňoval prenatální a postnatální vývoj. U březích samic potkanů a králíků, jimž byly podány opakovaně dávky 1 000 mg/kg/den, procházel ezetimib placentární bariérou. Současné podávání ezetimibu a statinů nebylo u potkanů teratogenní. U březích samic králíků byl pozorován malý počet skeletálních deformit (srůst hrudních a kaudálních žeber, zmenšený počet kaudálních žeber). Podávání ezetimibu s lovastatinem vedlo k embryoletálním účinkům.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Monohydrát laktózy
Mikrokrystalická celulóza
Kopovidon
Krospovidon
Natrium-lauryl-sulfát
Magnesium-stearát
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
30 měsíců
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní teplotní podmínky uchovávání. Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
6.5 Druh obalu a obsah balení
Protlačovací blistry z čirého Triplex (PVC/PE/PVDC)/hliníku v baleních po 7, 10, 14, 20, 28, 30, 50, 84, 90, 98, 100 nebo 300 tabletách.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku
Žádné zvláštní požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
XANTIS PHARMA LIMITED
Lemesou 5, EUROSURE TOWER,
1st floor, Flat/Office 101
2112, Nicosia, Kypr
8. REGISTRAČNÍ ČÍSLO(A)
31/335/17-C
Další informace o léčivu EZANTRIS
Jak
se EZANTRIS
podává: perorální podání - tableta
Výdej
léku: na lékařský předpis
Balení: Blistr
Velikost
balení: 7
Držitel rozhodnutí o registraci daného léku v České republice:
Xantis Pharma Limited, Nicosia
E-mail: info.cz@xantispharma.com
Telefon: +420 607 091 223
