Souhrnné informace o léku - COMBAIR NEXTHALER
1. NÁZEV PŘÍPRAVKU
Combair Nexthaler 100 mikrogramů/6 mikrogramů/dávka prášek k inhalaci
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna odměřená dávka 10 mg prášku k inhalaci obsahuje: beclometasoni dipropionas 100 mikrogramů, formoteroli fumaras dihydricus 6 mikrogramů.
To odpovídá podané dávce (z dávkovače) beclometasoni dipropionas 81,9 mikrogramů a formoteroli fumaras dihydricus 5,0 mikrogramů
Pomocná látka se známým účinkem:
Jedna odměřená dávka obsahuje 9,9 mg monohydrátu laktózy.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
3. LÉKOVÁ FORMAPrášek k inhalaci.
Vícedávkový inhalátor obsahuje bílý nebo téměř bílý prášek.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Astma
Combair Nexthaler je indikován pro pravidelnou udržovací léčbu astmatu, kde je vhodná kombinace léků (inhalačního kortikosteroidu a P2-mimetika s dlouhodobým účinkem):
-
– u pacientů, kde léčba inhalačními kortikosteroidy a P2-agonisty s rychlým účinkem podle potřeby nedosáhla dostatečné kontroly,
-
– u pacientů, kteří jsou adekvátně léčeni jak inhalačními kortikosteroidy, tak P2-agonisty s dlouhodobým účinkem.
Combair Nexthaler je indikován u dospělých pacientů.
Poznámka: Nejsou k dispozici relevantní klinické údaje k použití přípravku Combair Nexthaler v léčbě akutních astmatických záchvatů.
Chronická obstrukční plicní nemoc (CHOPN)
Symptomatická léčba pacientů s těžkou chronickou obstrukční plicní nemocí (FEV1 <50 % předpokládané normální hodnoty) s anamnézou opakujících se exacerbací, kteří mají významné příznaky navzdory pravidelné léčbě dlouhodobě působícími bronchodilatátory.
4.2 Dávkování a způsob podání
COMBAIR NEXTHALER JE URČEN K INHALAČNÍMU POUŽITÍ.
ASTMA
Dávkování přípravku Combair Nexthaler je individuální a má být upraveno podle závažnosti onemocnění. To by mělo platit nejen při zahájení kombinované léčby, ale také při každé úpravě dávky. Pokud pacient vyžaduje jinou kombinaci dávek, než je dostupná v kombinovaném inhalátoru, je nutné předepsat požadované dávky P2-agonistů a/nebo kortikosteroidů v samostatných inhalátorech.
Vzhledem k distribuci extrémně malých (extra fine) částic je nutná úprava dávkování při převádění pacientů na inhalační prášek Combair Nexthaler z lékové formy, která neobsahuje tyto velmi malé částice. Při přechodu z předchozí léčby je třeba vzít v úvahu, že doporučená celková denní dávka beklometasonu dipropionátu u přípravku Combair Nexthaler je nižší, než je současná celková denní dávka beklometasonu dipropionátu u produktů bez velmi malých částic, a dávka má být upravena podle individuálních potřeb pacienta. Nicméně pacienti převádění na prášek k inhalaci Combair Nexthaler z inhalačního roztoku v tlakovém obalu Combair Nexthaler nepotřebují úpravu dávky.
Doporučené dávkování pro dospělé ve věku 18 let a starší
-
1 nebo 2 inhalace dvakrát denně.
Maximální denní dávka jsou 4 inhalace denně.
Doporučené dávkování pro děti a dospívající mladší 18 let
Bezpečnost a účinnost přípravku Combair Nexthaler u dětí a dospívajících mladších 18 let nebyla dosud stanovena. Nejsou dostupné údaje u dětí mladších 11 let. Aktuálně dostupné údaje u dospívajících ve věku 12 až 17 let jsou shrnuty v bodech 4.8 a 5.1, nejedná se však o doporučení ohledně dávkování.
Pacienti musí být pravidelně kontrolováni lékařem, zda dávkování přípravku Combair Nexthaler zůstává optimální. Dávkování je povoleno upravit pouze na lékařské doporučení. Dávku je třeba titrovat na nejnižší dávku, při které se zachová účinná kontrola příznaků. Pokud je kontrola příznaků zajištěna při nejnižší doporučené dávce, další krok může zahrnovat použití samotného inhalačního kortikosteroidu.
Pacienty je nutné upozornit, aby užívali Combair Nexthaler každý den, a to i v případě, že jsou asymptomatičtí.
Chronická obstrukční plicní nemoc (CHOPN)
Doporučené dávkování pro dospělé ve věku 18 let a starší
-
2 inhalace dvakrát denně.
Zvláštní skupiny pacientů
U starších pacientů není nutné upravovat dávkování.
Nejsou k dispozici žádné údaje o použití přípravku Combair Nexthaler u pacientů s poruchou funkce jater nebo ledvin (viz bod 5.2).
Způsob podání
Nexthaler je vdechem ovládaný inhalátor. U pacientů se středně těžkým až těžkým astmatem a CHOPN se prokázalo, že jsou schopni vytvořit dostatečný nádech na uvolnění dávky ze systému Nexthaler (viz bod 5.1). Uvolněná dávka z přípravku Combair Nexthaler není závislá na rozmezí inspiračního průtoku, kterého je schopna tato skupina pacientů dosáhnout přes inhalátor.
Aby byla léčba úspěšná, je nezbytné správné použití inhalátoru Nexthaler. Pacienta je nutné poučit, aby si pozorně přečetl příbalovou informaci a postupoval podle pokynů k použití, jak jsou uvedeny v příbalové informaci. Pro potřebu předepisujícího lékaře jsou tyto pokyny uvedeny v části 6.6.
Při používání inhalátoru je třeba, aby pacient, pokud je to možné, seděl vzpřímeně nebo stál.
U inhalátoru Nexthaler je dávka k dispozici pro inhalaci pouze v případě, že je kryt zcela otevřený. Otevření krytu, inhalace a zavření krytu v tomto pořadí řídí mechanismus dávkovače. Pacienta je nutné poučit, aby kryt vždy zcela zavřel. Počet dávek uvedených v okénku pod krytem se nesníží uzavřením krytu, pokud pacient neinhaloval přes inhalátor.
Pacienta je nutné poučit, aby otvíral kryt inhalátoru pouze v případě potřeby. V případě, že pacient otevřel inhalátor, ale neprovedl inhalaci a kryt uzavřel, dávka se vrátí zpět do zásobníku prášku v inhalátoru; další dávku lze bezpečně inhalovat.
Optimálního dodání do plic se dosáhne, pokud pacient inhaluje přes inhalátor rychle a hluboko. Doporučená doba zadržení dechu před výdechem je 5–10 sekund (nebo tak dlouho, jak to pacient zvládne).
Pacienta je nutné upozornit, že nemá vydechovat přes Nexthaler před inhalací dávky nebo po ní, protože by to mohlo ovlivnit funkčnost inhalátoru.
Po inhalaci si pacienti musí vypláchnout ústa vodou, vykloktat si vodou nebo si vyčistit zuby (viz bod 4.4).
4.3 Kontraindikace
Přecitlivělost na beklometason-dipropionát, formoterol-fumarát nebo na kteroukoli pomocnou látku uvedenou v bodu 6.1.
4.4 Zvláštní upozornění a opatření pro použití
4.4 Zvláštní upozornění a opatření pro použitíPři ukončení léčby se doporučuje dávkování snižovat postupně, léčba se nesmí náhle ukončit.
Při léčbě astmatu se musí dodržovat postupné kroky na základě klinické odpovědi pacienta a funkčních vyšetření plic.
Pokud se pacient domnívá, že je léčba neúčinná, musí vyhledat lékaře. Zvýšené použití záchranných bronchodilatátorů ukazuje na zhoršení kontroly astmatu a vyžaduje přehodnocení léčby astmatu. Náhlé a progresivní zhoršení kontroly astmatu může ohrožovat život a pacient se musí okamžitě podrobit lékařskému vyšetření. Je třeba zvážit potřebu zvýšit dávky kortikosteroidů, buď inhalační, nebo perorální léčbou, nebo v případě podezření na infekci přidat do léčby antibiotika.
U pacientů nesmí být zahájena léčba inhalátorem Combair Nexthaler během exacerbace nebo při výrazném či akutním zhoršení astmatu. Během léčby inhalátorem Combair Nexthaler se mohou vyskytnout závažné, s astmatem spojené nežádoucí účinky a exacerbace. Pacienty je třeba upozornit, aby pokračovali v léčbě, ale vyhledali lékařskou pomoc, pokud příznaky astmatu neustoupí nebo se při léčbě přípravkem Combair Nexthaler zhorší.
Podobně jako u jiných inhalačních terapií se může po podání dávky vyskytnout paradoxní bronchospazmus projevující se okamžitým zvýšením sípání, kašlem a dyspnoí. Takový stav je nutné okamžitě léčit inhalačním bronchodilatátorem s rychlým účinkem. Léčba inhalátorem Combair Nexthaler se má okamžitě přerušit, stav pacienta přehodnotit a podle potřeby se má podat alternativní léčba.
Combair Nexthaler není určen k úvodní léčbě astmatu.
Pacienty je nutné požádat, aby s sebou vždy nosili bronchodilatátor s krátkodobým účinkem pro případ potřeby léčby akutních astmatických záchvatů.
Pacienty je nutné upozornit, aby užívali Combair Nexthaler každý den podle předpisu, a to i v případě, že jsou asymptomatičtí.
Po dosažení kompenzace příznaků astmatu lze zvážit postupné snížení dávky přípravku Combair Nexthaler. Pravidelné kontroly pacientů při snižování dávky léčby jsou velice důležité. Používejte nejnižší účinnou dávku přípravku Combair Nexthaler (viz bod 4.2).
Pneumonie u pacientů s CHOPN
U pacientů s CHOPN používajících inhalační kortikosteroidy došlo ke zvýšení incidence pneumonie, včetně pneumonie vyžadující hospitalizaci. Existují určité důkazy pro zvýšené riziko pneumonie se zvyšující se dávkou steroidů, výsledky různých klinických hodnocení však nejsou přesvědčivé.
Žádné jednoznačně klinicky prokázané rozdíly ve výši rizika pneumonie mezi jednotlivými inhalačními kortikosteroidy neexistují.
Lékaři by měli pečlivě sledovat případný rozvoj pneumonie u pacientů s CHOPN, jelikož se klinické známky takových infekcí překrývají s příznaky exacerbací CHOPN.
Rizikové faktory pneumonie u pacientů s CHOPN zahrnují kouření v současnosti, vyšší věk, nižší body mass index (BMI) a závažnější CHOPN.
Mohou se rozvinout systémové účinky inhalačních kortikosteroidů, hlavně u vysokých dávek předepisovaných po delší dobu. Tyto účinky jsou výrazně méně pravděpodobné než u perorálních kortikosteroidů. Mezi možné systémové účinky patří: Cushingův syndrom, Cushingoidní rysy, suprese nadledvin, růstová retardace u dětí a dospívajících, snížená kostní denzita, katarakta, glaukom a vzácněji různé psychologické nebo behaviorální účinky, včetně psychomotorické hyperaktivity, poruch spánku, úzkosti, deprese nebo agrese (hlavně u dětí). Dávku inhalačního kortikosteroidu je tudíž nutné titrovat na nejnižší dávku zajišťující kontrolu příznaků astmatu.
Dlouhodobá léčba pacientů vysokými dávkami inhalačních kortikosteroidů může vést k supresi nadledvin a akutní adrenální krizi. Děti a dospívající mladší 16 let užívající inhalačně vyšší, než doporučované dávky beklometason-dipropionátu mohou mít zvláště zvýšené riziko. Situace, které by mohly potenciálně vést k akutní adrenální krizi, zahrnují trauma, operaci, infekci nebo jakékoli rychlé snížení dávky. Úvodní příznaky jsou typicky vágní a mohou zahrnovat anorexii, bolesti břicha, pokles hmotnosti, únavu, bolesti hlavy, nevolnost, zvracení, hypotenzi, sníženou úroveň vědomí, hypoglykemii a záchvaty. Další krytí systémovými kortikosteroidy je nutné zvážit během období spojených se stresem nebo plánovaným chirurgickým výkonem.
Pacienti převádění z perorálních na inhalační kortikosteroidy mohou mít po významnou dobu přetrvávající zvýšené riziko narušené adrenální rezervy. Vyšší riziko mohou mít také pacienti, kteří vyžadovali vysokou akutní kortikosteroidní terapii v minulosti nebo podstoupili delší léčbu vysokými dávkami inhalačních kortikosteroidů. . Na tuto možnost reziduálního postižení je nutné vždy myslet v akutních případech a plánovaných situacích, které budou pravděpodobně spojené se stresem, a je nutné zvážit vhodnou kortikosteroidní léčbu. Rozsah adrenálního postižení může před plánovanými zákroky vyžadovat konzultaci se specialistou.
Combair Nexthaler je nutné podávat s opatrností u pacientů s aktivní nebo latentní plicní tuberkulózou, mykotickými a virovými infekcemi v dýchacích cestách.
Combair Nexthaler je nutné používat opatrně (může zahrnovat sledování) u pacientů se srdečními arytmiemi, hlavně atrioventrikulární blokádou třetího stupně a tachyarytmiemi, idiopatickou subvalvulární aortální stenózou, hypertrofickou obstrukční kardiomyopatií, ischemickou chorobou srdeční, závažným srdečním selháním, závažnou arteriální hypertenzí a aneuryzmatem.
Při léčbě pacientů se známým nebo suspektním prodloužením intervalu QTc, kongenitálním nebo farmakogenním (QTc >0,44 s), je nutné postupovat také opatrně. Samotný formoterol může indukovat prodloužení intervalu QTc.
Opatrně je také nutné postupovat při použití přípravku Combair Nexthaler u pacientů s thyreotoxikózou, diabetem mellitem, feochromocytomem a neléčenou hypokalémií.
Důsledkem terapie beta2-agonisty může být potenciálně závažná hypokalémie. Zvláštní pozornost je nutná u závažného astmatu, protože hypoxie může tento účinek potencovat. Hypokalémie může být také akcentována souběžnou terapií jinými léky, které mohou hypokalémii vyvolávat, jako např. deriváty xantinu, steroidy a diuretika (viz část 4.5). U nestabilního astmatu, kdy lze používat několik „záchranných“ bronchodilatátorů, je také nutné postupovat opatrně. V takových situacích doporučujeme sledovat sérové hladiny draslíku.
Inhalace formoterolu může vést ke zvýšení glykemie. Z toho důvodu je u pacientů s diabetem nutné pečlivě sledovat glykemii.
Pokud je plánována anestezie halogenovanými anestetiky, je nutné zabránit podání přípravku Combair Nexthaler po dobu minimálně 12 hodin před zahájením anestezie, jelikož hrozí srdeční arytmie.
Pacientům je třeba doporučit, aby si po inhalaci předepsané dávky vypláchli ústa, vykloktali vodou nebo si vyčistili zuby kartáčkem a minimalizovali tak riziko orofaryngeálních mykotických infekcí a dysfonie.
Laktóza obsahuje malé množství mléčných proteinů, které mohou vést k alergickým reakcím.
-
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Farmakokinetické interakce
Beklometason-dipropionát prochází velice rychlým metabolismem esterázovými enzymy.
Beklometason je méně závislý na metabolismu CYP3A než některé jiné kortikosteroidy a obecně jsou interakce nepravděpodobné. Nelze však zcela vyloučit riziko systémových účinků při konkomitantním použití silných inhibitorů CYP3A (např. ritonavir, cobicistat) a z toho důvodu je při použití takových látek nutné příslušné sledování.
Farmakodynamické interakce
Astmatici nesmí užívat žádné beta-blokátory (včetně očních kapek). Pokud budou ze závažných důvodů podávány beta-blokátory, účinek formoterolu bude snížen nebo zcela zrušen.
Použití jiných beta-adrenergních léků může mít potenciálně aditivní účinky. Z toho důvodu je při léčbě teofylinem nebo jinými beta-mimetiky předepisovanými společně s formoterolem nutné postupovat opatrně.
Souběžná léčba chinidinem, disopyramidem, prokainamidem, fenothiaziny, určitými antihistaminiky (např. tefrenadinem), inhibitory monoaminooxidázy a tricyklickými antidepresivy může prodloužit interval QTc a zvýšit riziko komorových arytmií.
Kromě toho mohou L-dopa, L-thyroxin, oxytocin a alkohol narušit srdeční toleranci vůči beta2-sympatomimetikům.
Souběžná léčba inhibitory monoaminooxidázy, včetně látek s podobnými vlastnostmi jako např. furazolidon a prokarbazin, může vést k hypertenzním reakcím.
Pacienti postupující souběžnou anestezii halogenovanými uhlovodíky mají zvýšené riziko arytmií.
Souběžná léčba deriváty xantinu, steroidy nebo diuretiky může potencovat hypokalemické účinky beta2-agonistů (viz bod 4.4). Hypokalémie může zvýšit predispozici na arytmie u pacientů léčených digitalisovými glykosidy.
4.6 Fertilita, těhotenství a kojení
4.6 Fertilita, těhotenství a kojeníFertilita
Nejsou k dispozici žádné údaje pro člověka. Ve zvířecích studiích u potkanů byla přítomnost beklometason-dipropionátu ve vysokých dávkách v kombinaci spojena se sníženou fertilitou samic a embryotoxicitou (viz bod 5.3).
Těhotenství
Neexistují žádné relevantní klinické údaje o použití přípravku Combair Nexthaler u těhotných žen. Zvířecí studie používající kombinaci beklometason-dipropionátu a formoterolu prokázaly při vysoké systémové expozici známky reprodukční a fetální toxicity (viz bod 5.3). Vysoké dávky kortikosteroidů podávané březím zvířatům vedou k abnormalitám vývoje plodu, včetně rozštěpu patra a zpomalení nitroděložního růstu. Vzhledem k tokolytickým účinkům beta2-sympatomimetik je nutné krátce před porodem postupovat zvláště opatrně. Formoterol se nedoporučuje k použití během těhotenství a hlavně na konci těhotenství nebo během porodu, ledaže by neexistovala žádná jiná (bezpečnější) zavedená alternativa.
Podání přípravku Combair Nexthaler během těhotenství je vhodné zvážit pouze za předpokladu, že očekávané benefity převáží potenciální rizika.
Kojení Neexistují žádné relevantní klinické údaje o použití přípravku Combair Nexthaler během kojení u člověka.
I když nejsou k dispozici žádné údaje ze zvířecích studií, racionálně lze předpokládat, že beklometason-dipropionát se vylučuje do mléka jako jiné kortikosteroidy.
I když není známo, jestli formoterol prochází do lidského mateřského mléka, byl zjištěn v mléku kojících zvířat.
Podání přípravku Combair Nexthaler u kojících žen je vhodné zvážit pouze za předpokladu, že očekávané benefity převáží potenciální rizika. Je nutné rozhodnout, jestli přestat s kojením, nebo vysadit přípravek Combair Nexthaler. Je třeba zvážit benefit kojení pro dítě a benefit terapie pro ženu.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Combair Nexthaler nemá žádný nebo má jenom minimální vliv na schopnost řídit a obsluhovat stroje.
4.8 Nežádoucí účinky
Nejčastější nežádoucí reakcí je třes. Ve 12týdenním klinickém hodnocení s přípravkem Combair Nexthaler byl třes pozorován pouze u nejvyššího dávkovacího režimu (2 inhalace 2× denně). Rozvinul se nejčastěji na začátku léčby a měl mírnou intenzitu. Žádný pacient nebyl kvůli třesu z klinického hodnocení vyřazen.
Klinická hodnocení - zkušenosti u pacientů s astmatem
Bezpečnost přípravku Combair Nexthaler byla hodnocena v klinických hodnoceních s aktivní kontrolou a kontrolou placebem, ve kterých bylo 719 pacientům ve věku 12 let a starších s astmatem různé závažnosti podáno léčivo. Incidence nežádoucích účinků v tabulce níže se vztahuje k pacientům s astmatem ve věku 12 let a starších a je založena na bezpečnostních zjištěních dvou pivotních klinických hodnocení, kde byl Combair Nexthaler podáván v dávkách doporučovaných v tomto souhrnu údajů o přípravku po dobu 8 až 12 týdnů. V klinických hodnoceních s přípravkem Combair Nexthaler nebyly pozorovány žádné psychiatrické poruchy, jsou však zařazeny do tabulky jako potenciální účinek skupiny inhalačních kortikosteroidů .
Nežádoucí účinky spojené s beklometason-dipropionátem a formoterolem podávaných ve fixní kombinaci (Combair Nexthaler) jsou uvedené níže v seznamu podle orgánových tříd. Frekvence jsou definovány následovně: velmi časté (^ 1/10), časté (^ 1/100 až <1/10), méně časté (1/1 000 až <1/100), vzácné 1/10 000 až <1/1 000) a velmi vzácné (<1/10 000), není známo (z dostupných údajů nelze určit).
| Třída orgánových systémů | Nežádoucí účinek | Frekvence |
| Infekce a infestace | Nasofaryngitida | Méně časté |
| Ústní kandidóza | Méně časté | |
| Pneumonie (u pacientů s CHOPN) | Časté | |
| Poruchy metabolismu a výživy | Hypertriglyceridémie | Méně časté |
| Psychiatrické poruchy | Psychomotorická hyperaktivita, poruchy spánku, úzkost, deprese, agresivita, behaviorální změny (především u dětí) | Frekvence není známa |
| Poruchy nervového systému | Třes | Časté |
| Bolest hlavy | Méně časté | |
| Srdeční poruchy | Tachykardie | Méně časté |
| Sinusová bradykardie | Méně časté | |
| Angina pectoris | Méně časté | |
| Ischemie myokardu | Méně časté | |
| Respirační, hrudní a mediastinální poruchy | Podráždění hrdla, exacerbace astmatu | Méně časté |
| Dyspnoe | Méně časté | |
| Orofaryngeální bolest | Méně časté | |
| Dysfonie | Méně časté | |
| Kašel | Méně časté | |
| Gastrointestinální poruchy | Nevolnost | Méně časté |
| Celkové poruchy a reakce v místě aplikace | Únava | Méně časté |
| Podrážděnost | Méně časté | |
| Vyšetření | Prodloužení QT podle elektrokardiogramu | Méně časté |
| Snížená hladina volného kortizolu v moči | Méně časté | |
| Snížená hladina kortizolu v krvi | Méně časté |
| Zvýšená kalémie | Méně časté | |
| Zvýšená glykemie | Méně časté | |
| Opožděný nárůst kmitu R na elektrokardiogramu | Méně časté |
Mezi pozorované nežádoucí účinky typicky spojené s formoterolem patří: třes, bolesti hlavy, tachykardie, sinusová bradykardie, angina pectoris, ischemie myokardu, prodloužení QT.
Mezi pozorované nežádoucí účinky typicky spojené s beklometason-dipropionátem patří: nasofaryngitida, ústní kandidóza, dysfonie, podráždění krku, iritabilita, snížená hladina volného kortizolu v moči, snížená hladina kortizolu v krvi, zvýšená glykemie.
Další nežádoucí účinky nepozorované v rámci klinického použití přípravku Combair Nexthaler, ale typicky spojené s inhalačním podáním beklometason-dipropionátu jsou ústní mykózy a pneumonie. Během terapie inhalačními kortikostereoidy byly vzácněji pozorovány poruchy chuti.
Opatření za účelem minimalizace ústních mykóz, ústní kandidózy a dysfonie naleznete v bodu 4.4.
Systémové účinky inhalačních kortikosteroidů (např. beklometason-dipropionát) se mohou rozvinout hlavně při podání ve vysokých dávkách předepisovaných po delší období. Mohou zahrnovat následující: Cushingův syndrom, Cushingoidní rysy, supresi nadledvin, sníženou kostní minerálovou denzitu, růstovou retardaci u dětí a dospívajících, kataraktu a glaukom (viz také bod 4.4).
Další nežádoucí účinky nebyly u terapeutických dávek přípravku Combair Nexthaler v klinické praxi pozorovány, jsou však typicky spojené s podáváním beta2-agonistů, jako je např. formoterol: palpitace, fibrilace síní, komorové extrasystoly, tachyarytmie, potenciálně závažná hypokalémie a zvýšení/snížení krevního tlaku. Insomnie, závratě, neklid a úzkost byly vzácněji hlášeny během inhalační terapie formoterolem. Formoterol může také způsobovat svalové křeče a myalgii.
Byly také hlášené reakce z přecitlivělosti, včetně vyrážky, kopřivky, svědění, zarudnutí a otoku očí, obličeje, rtů a hrdla (angioedém).
Podobně jako u jiných inhalačních terapií se může vyskytnout po podání dávky paradoxní bronchospazmus projevující se okamžitým zvýšením sípání, kašlem a dyspnoí (viz také bod 4.4).
Pediatrická populace
Nejsou k dispozici žádné informace o bezpečnosti přípravku Combair Nexthaler u dětí mladších 11 let. Dostupné jsou pouze omezené informace pro dospívající ve věku 12 až 17 let. Ve 12týdenním randomizovaném klinickém hodnocení u dospělých a dospívajících dostalo 162 dospívajících ve věku 12 až 17 let se středně závažným až závažným astmatem přípravek Combair Nexthaler nebo příslušný inhalační roztok v tlakovém aplikátoru, 1 nebo 2 inhalace 2× denně. Frekvence, typ a závažnost nežádoucích lékových reakcí se u dospívajících a dospělých nelišily.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
Webové stránky:
4.9 Předávkování
4.9 PředávkováníNejvyšší doporučená dávka přípravku Combair Nexthaler v jednom podání jsou 2 inhalace. U pacientů s astmatem byly hodnoceny 4 kumulativní inhalace přípravku Combair Nexthaler (celková dávka beklometason-dipropionátu 400 mikrogramů, formoterolu 24 mikrogramů podaná v jedné dávce). Kumulativní léčba nevedla k abnormálním klinicky relevantním účinkům na životní funkce a nebyly pozorovány závažné ani těžké nežádoucí reakce (viz také bod 4.8).
U inhalačního roztoku v tlakovém aplikátoru byly u pacientů s astmatem hodnoceny inhalované dávky s až 12 kumulativními aktivacemi (celková dávka beklometason-dipropionátu 1 200 mikrogramů, formoterolu 72 mikrogramů). Kumulativní léčba nevedla k abnormálním účinkům na životní funkce a nebyly pozorovány závažné ani těžké nežádoucí reakce.
Nadměrné dávky formoterolu mohou vést k účinkům typickým pro beta2-agonisty, jako jsou: nauzea, zvracení, bolesti hlavy, třes, somnolence, palpitace, tachykardie, komorové arytmie, prodloužení intervalu QTc, metabolická acidóza, hypokalémie, hyperglykemie.
V případě předávkování formoterolem je indikována podpůrná a symptomatická léčba. Závažné případy je třeba hospitalizovat. Lze zvážit použití kardioselektivních beta-blokátorů. V takovém případě je nutné postupovat zvláště opatrně, jelikož použití beta-blokátorů může vyvolat bronchospazmus. Je třeba sledovat sérovou hladinu draslíku.
Akutní inhalace dávek beklometason-dipropionátu přesahujících doporučenou hodnotu může vést k dočasné supresi nadledvinových funkcí. Tato změna nevyžaduje akutní zásah, jelikož se nadledvinové funkce obnoví za několik dní, co lze ověřit podle plazmatické hladiny kortizolu. U těchto pacientů je potřeba pokračovat v léčbě v dávce dostatečné pro kontrolu astmatu.
Chronické předávkování inhalovaným beklometason-dipropionátem: riziko suprese nadledvin (viz bod 4.4). Může být nutné sledovat adrenální rezervu. V léčbě je třeba pokračovat v dávce dostatečné pro kontrolu astmatu.
Jednorázové supraterapeutické dávky beklometason-dipropionátu do 800 mikrogramů a do 48 mikrogramů formoterolu podané pomocí aplikátoru Combair Nexthaler jsou obecně bezpečné a dobře tolerované.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: adrenergní přípravky, inhalační přípravky: formoterol a jiná léčiva onemocnění spojených s obstrukcí dýchacích cest.
ATC kód: R03AK08.
Mechanismus účinku a farmakodynamické účinky
Přípravek Combair Nexthaler obsahuje beklometason-dipropionát a formoterol ve formulaci jako suchý prášek, díky čemu vzniká extra jemný (extra-fine) aerosol s průměrným hmotnostním mediánovým aerodynamickým průměrem (MMAD) v rozmezí 1,4 až 1,5 mikrometru a s ko-depozicí dvou komponent. Aerosolové částečky přípravku Combair Nexthaler jsou v průměru mnohem menší než částečky obsažené v jiných non-extra-fine formulacích přípravků.
Studie ukládání radiofarmaka u dospělých pacientů prokázaly, že vysoký podíl léku (odhadem 42 % nominální dávky) se ukládá v plicích s homogenním uložením v dýchacích cestách. Tyto charakteristiky aplikace podporují použití nízké dávky kortikosteroidu se zvýšenými lokálními farmakodynamickými účinky, které jsou prokazatelně ekvivalentní příslušnému inhalačnímu roztoku v tlakových aplikátorech (viz Klinické zkušenosti).
Dvě látky obsažené v přípravku Combair Nexthaler mají odlišné mechanismy účinku. Také u této kombinace, podobně jako u jiných kombinací inhalačních kortikosteroidů a beta2-agonistů, byly zjištěny aditivní účinky na snížení počtu exacerbací astmatu.
Beklometason-dipropionát
Beklometason-dipropionát podávaný inhalačně v doporučovaných dávkách má glukokortikoidní protizánětlivý účinek v plicích, což vede ke ztlumení příznaků a exacerbaci astmatu s méně závažnými nežádoucími účinky než při systémovém podání kortikosteroidů.
Formoterol
Formoterol je selektivní beta2-agonista vedoucí k relaxaci bronchiální hladké svaloviny u pacientů s reverzibilní obstrukcí dýchacích cest. Bronchodilatační účinky nastupují rychle do 1 až 3 minut po inhalaci a trvají 12 hodin po podání dávky.
Klinické zkušenosti
Účinnost dvou komponent prášku k inhalaci Combair Nexthaler byla hodnocena ve třech samostatných klinických hodnoceních ve srovnání se 100 mikrogramy / 6 mikrogramy inhalačního roztoku v tlakových aplikátorech u pacientů se středně těžkým až těžkým persistentním astmatem. Celkově se v klinické praxi očekává srovnatelná účinnost obou typů inhalátorů u 1 i 2 inhalací 2× denně.
-
V jednom klinickém hodnocení bylo primárním cílem vyhodnocení účinnosti inhalační kortikosteroidní komponenty na bronchodilataci (FEV1 před dávkou). Ke klinicky významnému zlepšení FEV1 před dávkou došlo u 696 pacientů se středně těžkým až těžkým symptomatickým astmatem na konci 3měsíčního léčebného období ve srovnání s výchozími hodnotami s 1 inhalací 2× denně a 2 inhalacemi 2× denně u obou formulací přípravku. Došlo ke střednímu nárůstu na úrovni minimálně 250 ml. Mezi FEV1 před dávkou u prášku k inhalaci Combair Nexthaler a inhalačním roztokem v tlakovém aplikátoru nebyl v žádné dávce pozorován klinicky relevantní rozdíl. U ranního PEF byla pozorována významná reakce na dávku. Statistická významnost pro odpověď na dávku nebyla dosažena u FEV1 před dávkou. Parametry kompenzace astmatu jako ranní a večerní skóre příznaků astmatu a procentuální podíl dní bez příznaků se při srovnání výchozí úrovně a konce léčebného období významně zlepšily, hlavně u dvou vysokých dávek obou formulací přípravku.
-
V druhém klinickém hodnocení bylo primárním cílem stanovit účinnost komponenty Combair Nexthaler s dlouhodobým beta2-adrenergním účinkem. V tomto klinickém hodnocení byla měřena bronchodilatace na začátku a až 12 hodin po podání jedné dávky sériovými spirometrickými hodnoceními FEV1 (FEV1 AUC během minimálně 80 % délky účinku formoterolu). Ve srovnání s placebem vedla jedna inhalace a čtyři inhalace obou účinných látek přípravku Combair Nexthaler k významnému zlepšení FEV1 AUC0–12. Obě dávky prášku k inhalaci Combair Nexthaler byly non-inferiorní k odpovídající dávce inhalačního roztoku v tlakovém aplikátoru. Statisticky významná odpověď na dávku byla pozorována u obou formulací mezi nízkou a vysokou dávkou.
-
V dalším otevřeném klinickém hodnocení s placebem bylo prokázáno analýzou inspiračního profilu pomocí systému Combair Nexthaler, že pacienti s mírnou až těžkou CHOPN, bez ohledu na jejich funkční omezení, byli schopni prostředek efektivně aktivovat a používat.
Pediatrická populace
Evropská léková agentura poskytla odklad povinnosti předložit výsledky klinických hodnocení u astmatu s přípravkem Combair Nexthaler u věkových podskupin pediatrické populace 5 až 11 a 12 až 17 let.
-
V době přípravy dokumentu nebyly k dispozici žádné klinické zkušenosti s přípravkem Combair Nexthaler u dětí ve věku 5 až 11 let. Dostupné jsou pouze omezené informace pro dospívající ve věku 12 až 17 let.
Ve 3měsíčním randomizovaném klinickém hodnocení dostávalo 162 dospívajících ve věku 12 až 17 let s diagnózou středně těžkého až těžkého astmatu přípravek Combair Nexthaler nebo odpovídající inhalační roztok v tlakovém aplikátoru, 1 nebo 2 inhalace 2× denně. Změna FEV1 před dávkou na konci léčby byla u dospívajících významnější než u dospělých.
Informace o pediatrickém použití naleznete také v bodech 4.2 a 4.8.
5.2 Farmakokinetické vlastnosti
5.2 Farmakokinetické vlastnostiBeklometason-dipropionát
Beklometasondipropionát je pro-léčivo se slabou vazebnou afinitou vůči receptoru pro glukokortikoidy, který se hydrolyzuje esterázovými enzymy na aktivní metabolit beklometason-17-monopropionát s potentnější topickou protizánětlivou aktivitou ve srovnání s pro-léčivem beklometason-dipropionátem.
Absorpce, distribuce a metabolismus
Inhalačně podaný beklometason-dipropionát se rychle absorbuje plícemi: před absorpcí probíhá intenzivní konverze na aktivní metabolit beklometason-17-monopropionát esterázovými enzymy, které se nachází ve většině tkání. Systémová dostupnost aktivního metabolitu pochází z plic a z gastrointestinální absorpce spolykané dávky. Biologická dostupnost spolykaného beklometason-dipropionátu je však zanedbatelná. Presystémová konverze na beklometason-17-monopropionát vede k absorpci části dávky v podobě aktivního metabolitu.
Se zvyšující se inhalovanou dávkou dochází k přibližně lineárnímu vzestupu systémové expozice. Absolutní biologická dostupnost po inhalaci z tlakového inhalátoru s odměřenou dávkou je přibližně 2 % nominální dávky nezměněného beklometason-dipropionátu a 62 % pro beklometason-17-monopropionát.
Po intravenózním podání jsou dispozice beklometason-dipropionátu a jeho aktivního metabolitu charakterizovány vysokou plazmatickou clearance (150, resp. 120 l/h), s malým distribučním objemem v rovnovážném stavu pro beklometason-dipropionát (20 l) a větší tkáňovou distribucí pro jeho aktivní metabolit (424 l). Metabolická dispozice beklometason-dipropionátu vede hlavně (82 %) ke vzniku jeho aktivního metabolitu beklometason-17-monopropionátu.
Vazba na plazmatické proteiny je středně vysoká (87 %).
Vylučování
Fekální vylučování je hlavní cestou eliminace beklometason-dipropionátu zejména v podobě polárních metabolitů. Renální vylučování beklometason-dipropionátu a jeho metabolitů je zanedbatelné. Poločasy terminální eliminace jsou 0,5 h pro beklometason-dipropionát a 2,7 h pro beklometason-17-monopropionát.
Zvláštní populace
Farmakokinetika beklometason-dipropionátu u pacientů s renální nebo jaterní dysfunkcí nebyla předmětem studií. Jelikož však beklometason-dipropionát prochází velice rychlým metabolismem esterázovými enzymy přítomnými ve střevní tekutině, séru, plicích a játrech za vzniku polárnějších produktů beklometason-21-monopropionátu, beklometason-17-monopropionátu a beklometasonu, jaterní dysfunkce pravděpodobně nepovede ke změně farmakokinetiky a bezpečnostního profilu beklometason-dipropionátu.
Jelikož beklometason-dipropionát nebo jeho metabolity nebyly zjištěny v moči, u pacientů s renální dysfunkcí se neočekává zvýšení systémové expozice.
Formoterol
Absorpce a distribuce
Po inhalaci se formoterol absorbuje z plic a z gastrointestinálního traktu. Frakce, která se po inhalaci spolkne po podání pomocí inhalátoru (MDI) může kolísat mezi 60 % – 90 %.
Nejméně 65 % frakce, která je spolknutá, se absorbuje z gastrointestinálního traktu. Nejvyšší koncentrace nezměněné látky v plasmě je dosaženo za 30 minut až za 1 hod po perorálním podání. Na plazmatické proteiny se váže 61 až 64 % (34 % na albuminy); při terapeutickém dávkování nejsou vazebná místa saturována. Eliminační biologický poločas po perorálním podání byl určen na 2 až 3 hodiny. Absorpce formoterolu po inhalaci 12 až 96 ^g formoterol-fumarátu je v závislosti na dávce lineární.
Biotransformace
Formoterol se primárně metabolizuje přímou konjugací na fenolovou hydroxylovou skupinu. Konjugace s kyselinou glukuronidovou metabolit inaktivuje. Další cesta biotransformace je O-demetylace na fenolovou 2-hydroxylovou skupinu s následnou konjugací.
Isoenzymy cytochromu CYP450 (CYP2D6, CYP2C19 a CYP2C9) se podílejí na O-demetylaci formoterolu. Hlavním místem metabolizace jsou tedy játra. Formoterol v terapeuticky relevantních koncentracích neinhibuje CYP450.
Eliminace
Kumulativní exkrece formoterolu se po jednorázovém inhalačním podání zvyšuje z práškového inhalátoru lineárně v rozmezí dávek 12 – 96 ^g. Průměrně je vyloučeno 8 % podané dávky jako nezměněný formoterol a 25 % jako celkový formoterol. Na základě plasmatické koncentrace měřené po inhalaci jednotlivé dávky 120 ^g 12 zdravým dobrovolníkům byl určen střední terminální eliminační poločas na 10 hodin. (R,R)- a (S,S)-enantioméry představují kolem 40 % a 60 % nezměněné látky vylučované do moče. Relativní proporce dvou enantiomérů zůstává ve studovaném dávkovém rozmezí konstantní a akumulace těchto enantiomerů po opakovaných dávkách nebyla zjištěna.
Po podání perorální dávky (od 40 do 80 |jg) bylo u zdravých dobrovolníků v moči zjištěno 6 – 10 % nezměněné látky a 8 % látky ve formě glukuronidu.
Celkově 67 % perorálně podané dávky formoterolu je vylučováno do moče (hlavně jako metabolity) a zbytek je vylučováno stolicí. Renální clearance formoterolu je 150 ml/min.
Zvláštní populace
Jaterní/renální postižení: farmakokinetika formoterolu u pacientů s jaterním nebo renálním postižením nebyla hodnocena.
Klinické zkušenosti
Systémová expozice beklometason-dipropionátu a formoterolu v kombinaci byla porovnána s jednotlivými složkami. Nebyly zjištěny žádné známky farmakokinetických nebo farmakodynamických (systémových) interakcí mezi beklometason-dipropionátem a formoterolem.
Farmakokinetika prášku k inhalaci Combair Nexthaler byla srovnána s farmakokinetikou odpovídajícího inhalačního roztoku v tlakovém aplikátoru. Analýza steroidní komponenty byla zaměřena na beklometason-17-monopropionát, hlavní aktivní metabolit beklometason-dipropionátu. Systémová absorpce a metabolismus beklometason-dipropionátu byly rychlé a Cmax byla dosažena 5 minut po podání dávky u obou léčeb, ale byla vyšší (+68 %) u prášku k inhalaci přípravku Combair Nexthaler. AUCt byla asi 3× vyšší po inhalaci přípravku Combair Nexthaler přes inhalátor Nexthaler ve srovnání s inhalačním roztokem v tlakovém aplikátoru. Cmax pro beklometason-17-monopropionát, hlavní aktivní metabolit představující asi 82 % celkové hladiny v krvi, byla dosažena v průměru po 30 minutách při použití systému Nexthaler a po 15 minutách po použití inhalačního roztoku v tlakovém aplikátoru. Plazmatická koncentrace beklometason-17-monopropionátu byla nižší (Cmax –49 % a AUCt –29 %) po inhalaci prášku k inhalaci než u inhalačního roztoku v tlakovém aplikátoru. Po inhalaci přípravku Combair Nexthaler pomocí inhalátoru Nexthaler byla maximální koncentrace (Cmax) formoterolu dosažena do 5 minut a byla vyšší (+47 %) pro prášek k inhalaci, kdežto celková expozice (AUCt) byla u obou terapií srovnatelná.
V jednom klinickém hodnocení bylo analyzováno relativní dodání do plic prostřednictvím blokády pomocí aktivního uhlí s cílem vyloučit absorpci léčiva z gastrointestinálního traktu. Byl použit schválený spacer AeroChamber Plus pro referenční přípravek (inhalační roztok v tlakovém aplikátoru). Za těchto podmínek se Nexthaler a inhalační roztok v tlakovém aplikátoru ukázaly jako ekvivalentní pro AUCt beklometason-17-monopropionátu i formoterolu (poměr pro prášek k inhalaci / inhalační roztok v tlakovém aplikátoru a 90% intervaly spolehlivosti spadaly do rozmezí 80125 %). Cmax beklometason-17-monopropionátu však byla nižší (-38 %) po inhalaci pomocí systému Nexthaler.
5.3 Předklinické údaje vztahující se k bezpečnosti
5.3 Předklinické údaje vztahující se k bezpečnostiNeklinické údaje individuálních komponen přípravku Combair Nexthaler založené na konvenčních studiích farmakologie bezpečnosti a toxicity po opakovaném podání neodhalují žádná speciální rizika pro člověka. Profil toxicity kombinace ukazuje, že jednotlivé komponenty nevedou ke zvýšení toxicity nebo neočekávaným zjištěním.
Reprodukční studie u potkanů prokázaly účinky závislé na dávce. Přítomnost beklometason-dipropionátu ve vysokých dávkách byla spojena se sníženou fertilitou samic, sníženým počtem implantací a embryofetální toxicitou. Vysoké dávky kortikosteroidů podávané březím zvířatům vedou k abnormalitám fetálního vývoje, včetně rozštěpu patra a zpomalení nitroděložního růstu. Je pravděpodobné, že účinky pozorované u kombinace beklometason-dipropionát/formoterol byly způsobené beklometason-dipropionátem. Tyto účinky byly pozorovány pouze u vysoké systémové expozice aktivnímu metabolitu beklometason-17-monopropionátu (více než 200násobek očekávané plazmatické hladiny u pacientů). Kromě toho byly ve zvířecích studiích pozorovány delší trvání gestace a porodu, vliv, který lze připsat známým tokolytickým účinkům beta2-sympatomimetik. Tyto účinky byly pozorovány u hladin formoterolu v plazmě samic nižších než hladiny očekávané u pacientů léčených přípravkem Combair Nexthaler.
Studie genotoxicity provedené s kombinací beklometason-dipropionát/formoterol neprokazují mutagenní potenciál. S navrhovanou kombinací nebyly provedeny žádné studie karcinogenity. Zvířecí údaje hlášené pro individuální složky nesvědčí pro žádné potenciální riziko karcinogenity u člověka.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Monohydrát laktózy (který obsahuje malé množství mléčných proteinů) Magnesium-stearát
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
3 roky.
Po prvním otevření foliového sáčku je nutné léčivý přípravek použít do 6 měsíců.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
Inhalátor vyjměte z fóliového sáčku až krátce před prvním použitím.
Před prvním otevřením foliového sáčku:
Tento léčivý přípravek nevyžaduje žádné zvláštní teplotní podmínky uchovávání.
Po prvním otevření foliového sáčku:
Neuchovávejte při teplotě nad 25 °C.
6.5 Druh obalu a velikost balení
Jedno balení obsahuje 1, 2 nebo 3 inhalátory Nexthaler, každý z nich obsahuje 1,50 g prášku k inhalaci a poskytuje 120 inhalací. Inhalátor je uložen v tepelně uzavřeném ochranném vaku (fóliovém sáčku) vyrobeném z PET/Al/PE (polyetylentereftalát/hliník/polyetylen) nebo PA/Al/PE (polyamid/hliník/polyetylen).
Na trhu nemusí být všechny velikosti balení.
Combair Nexthaler je vícedávkový inhalační prostředek. Inhalátor se skládá z obalu ze spodního krytu s okénkem zobrazujícím zbývající počet dávek a zabudovaným krytem. Po otevření krytu, kterým se také pohání mechanismus počítadla dávek, se odhalí náustek, přes který se léčivo inhaluje. Spodní kryt a náustek jsou vyrobeny z akrylonitrilbutadienstyrénu a kryt je vyroben z polypropylenu.
6.6 Zvláštní opatření pro likvidaci přípravku
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidovány v souladu s místními požadavky.
Níže je uveden návod k použití inhalátoru Nexthaler pro potřeby zdravotníků.
NÁVOD K POUŽITÍ INHALÁTORU NEXTHALER
Toto balení obsahuje:
- 1 informační leták s pokyny,
- 1 inhalátor Nexthaler uvnitř uzavřeného ochranného foliového sáčku.
Pokud obsah balení neodpovídá uvedenému seznamu, vraťte inhalátor osobě, která vám jej vydala, a pořiďte si nový.
- Nevytahujte inhalátor z foliového sáčku, pokud jej nechcete ihned použít.
- Svůj inhalátor používejte výhradně podle pokynů.
- Pokud si nejste jistý(á), jestli po jedné inhalaci pokleslo číslo na počítadlu dávek, počkejte na svou další plánovanou dávku a užijte ji jako normálně. Neužívejte dávku navíc.
- Ponechte kryt uzavřený, dokud nebudete potřebovat další dávku z inhalátoru.
- Když inhalátor nepoužíváte, uchovávejte jej na čistém a suchém místě.
- Nesnažte se ze žádného důvodu inhalátor Nexthaler rozebírat.
- Nepoužívejte inhalátor Nexthaler:
o po uplynutí data spotřeby,
o pokud od otevření foliového sáčku uplynulo více než 6 měsíců,
o pokud je poškozen,
o pokud je v okénku počítadla dávek uvedena hodnota „0“,
o pokud nelze odečíst okénko počítadla dávek.
V takových případech svůj inhalátor zlikvidujte nebo jej vraťte osobě, která vám jej vydala, a pořiďte si nový. Zeptejte se svého lékárníka, jak máte likvidovat inhalátory, které již nepotřebujete.
Vstup vzduchu
Okénko počítadla dávek
Kryt
náustek
1.
2.
3.
1. Zkontrolujte zbývající počet dávek: jakékoli číslo v rozmezí
1. NÁZEV PŘÍPRAVKU
Combair Nexthaler 100 mikrogramů/6 mikrogramů/dávka prášek k inhalaci
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna odměřená dávka 10 mg prášku k inhalaci obsahuje: beclometasoni dipropionas 100 mikrogramů, formoteroli fumaras dihydricus 6 mikrogramů.
To odpovídá podané dávce (z dávkovače) beclometasoni dipropionas 81,9 mikrogramů a formoteroli fumaras dihydricus 5,0 mikrogramů
Pomocná látka se známým účinkem:
Jedna odměřená dávka obsahuje 9,9 mg monohydrátu laktózy.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Prášek k inhalaci.
Vícedávkový inhalátor obsahuje bílý nebo téměř bílý prášek.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Astma
Combair Nexthaler je indikován pro pravidelnou udržovací léčbu astmatu, kde je vhodná kombinace léků (inhalačního kortikosteroidu a P2-mimetika s dlouhodobým účinkem):
-
– u pacientů, kde léčba inhalačními kortikosteroidy a P2-agonisty s rychlým účinkem podle potřeby nedosáhla dostatečné kontroly,
-
– u pacientů, kteří jsou adekvátně léčeni jak inhalačními kortikosteroidy, tak P2-agonisty s dlouhodobým účinkem.
Combair Nexthaler je indikován u dospělých pacientů.
Poznámka: Nejsou k dispozici relevantní klinické údaje k použití přípravku Combair Nexthaler v léčbě akutních astmatických záchvatů.
Chronická obstrukční plicní nemoc (CHOPN)
Symptomatická léčba pacientů s těžkou chronickou obstrukční plicní nemocí (FEV1 <50 % předpokládané normální hodnoty) s anamnézou opakujících se exacerbací, kteří mají významné příznaky navzdory pravidelné léčbě dlouhodobě působícími bronchodilatátory.
4.2 Dávkování a způsob podání
COMBAIR NEXTHALER JE URČEN K INHALAČNÍMU POUŽITÍ.
ASTMA
Dávkování přípravku Combair Nexthaler je individuální a má být upraveno podle závažnosti onemocnění. To by mělo platit nejen při zahájení kombinované léčby, ale také při každé úpravě dávky. Pokud pacient vyžaduje jinou kombinaci dávek, než je dostupná v kombinovaném inhalátoru, je nutné předepsat požadované dávky P2-agonistů a/nebo kortikosteroidů v samostatných inhalátorech.
Vzhledem k distribuci extrémně malých (extra fine) částic je nutná úprava dávkování při převádění pacientů na inhalační prášek Combair Nexthaler z lékové formy, která neobsahuje tyto velmi malé částice. Při přechodu z předchozí léčby je třeba vzít v úvahu, že doporučená celková denní dávka beklometasonu dipropionátu u přípravku Combair Nexthaler je nižší, než je současná celková denní dávka beklometasonu dipropionátu u produktů bez velmi malých částic, a dávka má být upravena podle individuálních potřeb pacienta. Nicméně pacienti převádění na prášek k inhalaci Combair Nexthaler z inhalačního roztoku v tlakovém obalu Combair Nexthaler nepotřebují úpravu dávky.
Doporučené dávkování pro dospělé ve věku 18 let a starší
-
1 nebo 2 inhalace dvakrát denně.
Maximální denní dávka jsou 4 inhalace denně.
Doporučené dávkování pro děti a dospívající mladší 18 let
Bezpečnost a účinnost přípravku Combair Nexthaler u dětí a dospívajících mladších 18 let nebyla dosud stanovena. Nejsou dostupné údaje u dětí mladších 11 let. Aktuálně dostupné údaje u dospívajících ve věku 12 až 17 let jsou shrnuty v bodech 4.8 a 5.1, nejedná se však o doporučení ohledně dávkování.
Pacienti musí být pravidelně kontrolováni lékařem, zda dávkování přípravku Combair Nexthaler zůstává optimální. Dávkování je povoleno upravit pouze na lékařské doporučení. Dávku je třeba titrovat na nejnižší dávku, při které se zachová účinná kontrola příznaků. Pokud je kontrola příznaků zajištěna při nejnižší doporučené dávce, další krok může zahrnovat použití samotného inhalačního kortikosteroidu.
Pacienty je nutné upozornit, aby užívali Combair Nexthaler každý den, a to i v případě, že jsou asymptomatičtí.
Chronická obstrukční plicní nemoc (CHOPN)
Doporučené dávkování pro dospělé ve věku 18 let a starší
-
2 inhalace dvakrát denně.
Zvláštní skupiny pacientů
U starších pacientů není nutné upravovat dávkování.
Nejsou k dispozici žádné údaje o použití přípravku Combair Nexthaler u pacientů s poruchou funkce jater nebo ledvin (viz bod 5.2).
Způsob podání
Nexthaler je vdechem ovládaný inhalátor. U pacientů se středně těžkým až těžkým astmatem a CHOPN se prokázalo, že jsou schopni vytvořit dostatečný nádech na uvolnění dávky ze systému Nexthaler (viz bod 5.1). Uvolněná dávka z přípravku Combair Nexthaler není závislá na rozmezí inspiračního průtoku, kterého je schopna tato skupina pacientů dosáhnout přes inhalátor.
Aby byla léčba úspěšná, je nezbytné správné použití inhalátoru Nexthaler. Pacienta je nutné poučit, aby si pozorně přečetl příbalovou informaci a postupoval podle pokynů k použití, jak jsou uvedeny v příbalové informaci. Pro potřebu předepisujícího lékaře jsou tyto pokyny uvedeny v části 6.6.
Při používání inhalátoru je třeba, aby pacient, pokud je to možné, seděl vzpřímeně nebo stál.
U inhalátoru Nexthaler je dávka k dispozici pro inhalaci pouze v případě, že je kryt zcela otevřený. Otevření krytu, inhalace a zavření krytu v tomto pořadí řídí mechanismus dávkovače. Pacienta je nutné poučit, aby kryt vždy zcela zavřel. Počet dávek uvedených v okénku pod krytem se nesníží uzavřením krytu, pokud pacient neinhaloval přes inhalátor.
Pacienta je nutné poučit, aby otvíral kryt inhalátoru pouze v případě potřeby. V případě, že pacient otevřel inhalátor, ale neprovedl inhalaci a kryt uzavřel, dávka se vrátí zpět do zásobníku prášku v inhalátoru; další dávku lze bezpečně inhalovat.
Optimálního dodání do plic se dosáhne, pokud pacient inhaluje přes inhalátor rychle a hluboko. Doporučená doba zadržení dechu před výdechem je 5–10 sekund (nebo tak dlouho, jak to pacient zvládne).
Pacienta je nutné upozornit, že nemá vydechovat přes Nexthaler před inhalací dávky nebo po ní, protože by to mohlo ovlivnit funkčnost inhalátoru.
Po inhalaci si pacienti musí vypláchnout ústa vodou, vykloktat si vodou nebo si vyčistit zuby (viz bod 4.4).
4.3 Kontraindikace
Přecitlivělost na beklometason-dipropionát, formoterol-fumarát nebo na kteroukoli pomocnou látku uvedenou v bodu 6.1.
4.4 Zvláštní upozornění a opatření pro použití
Při ukončení léčby se doporučuje dávkování snižovat postupně, léčba se nesmí náhle ukončit.
Při léčbě astmatu se musí dodržovat postupné kroky na základě klinické odpovědi pacienta a funkčních vyšetření plic.
Pokud se pacient domnívá, že je léčba neúčinná, musí vyhledat lékaře. Zvýšené použití záchranných bronchodilatátorů ukazuje na zhoršení kontroly astmatu a vyžaduje přehodnocení léčby astmatu. Náhlé a progresivní zhoršení kontroly astmatu může ohrožovat život a pacient se musí okamžitě podrobit lékařskému vyšetření. Je třeba zvážit potřebu zvýšit dávky kortikosteroidů, buď inhalační, nebo perorální léčbou, nebo v případě podezření na infekci přidat do léčby antibiotika.
U pacientů nesmí být zahájena léčba inhalátorem Combair Nexthaler během exacerbace nebo při výrazném či akutním zhoršení astmatu. Během léčby inhalátorem Combair Nexthaler se mohou vyskytnout závažné, s astmatem spojené nežádoucí účinky a exacerbace. Pacienty je třeba upozornit, aby pokračovali v léčbě, ale vyhledali lékařskou pomoc, pokud příznaky astmatu neustoupí nebo se při léčbě přípravkem Combair Nexthaler zhorší.
Podobně jako u jiných inhalačních terapií se může po podání dávky vyskytnout paradoxní bronchospazmus projevující se okamžitým zvýšením sípání, kašlem a dyspnoí. Takový stav je nutné okamžitě léčit inhalačním bronchodilatátorem s rychlým účinkem. Léčba inhalátorem Combair Nexthaler se má okamžitě přerušit, stav pacienta přehodnotit a podle potřeby se má podat alternativní léčba.
Combair Nexthaler není určen k úvodní léčbě astmatu.
Pacienty je nutné požádat, aby s sebou vždy nosili bronchodilatátor s krátkodobým účinkem pro případ potřeby léčby akutních astmatických záchvatů.
Pacienty je nutné upozornit, aby užívali Combair Nexthaler každý den podle předpisu, a to i v případě, že jsou asymptomatičtí.
Po dosažení kompenzace příznaků astmatu lze zvážit postupné snížení dávky přípravku Combair Nexthaler. Pravidelné kontroly pacientů při snižování dávky léčby jsou velice důležité. Používejte nejnižší účinnou dávku přípravku Combair Nexthaler (viz bod 4.2).
Pneumonie u pacientů s CHOPN
U pacientů s CHOPN používajících inhalační kortikosteroidy došlo ke zvýšení incidence pneumonie, včetně pneumonie vyžadující hospitalizaci. Existují určité důkazy pro zvýšené riziko pneumonie se zvyšující se dávkou steroidů, výsledky různých klinických hodnocení však nejsou přesvědčivé.
Žádné jednoznačně klinicky prokázané rozdíly ve výši rizika pneumonie mezi jednotlivými inhalačními kortikosteroidy neexistují.
Lékaři by měli pečlivě sledovat případný rozvoj pneumonie u pacientů s CHOPN, jelikož se klinické známky takových infekcí překrývají s příznaky exacerbací CHOPN.
Rizikové faktory pneumonie u pacientů s CHOPN zahrnují kouření v současnosti, vyšší věk, nižší body mass index (BMI) a závažnější CHOPN.
Mohou se rozvinout systémové účinky inhalačních kortikosteroidů, hlavně u vysokých dávek předepisovaných po delší dobu. Tyto účinky jsou výrazně méně pravděpodobné než u perorálních kortikosteroidů. Mezi možné systémové účinky patří: Cushingův syndrom, Cushingoidní rysy, suprese nadledvin, růstová retardace u dětí a dospívajících, snížená kostní denzita, katarakta, glaukom a vzácněji různé psychologické nebo behaviorální účinky, včetně psychomotorické hyperaktivity, poruch spánku, úzkosti, deprese nebo agrese (hlavně u dětí). Dávku inhalačního kortikosteroidu je tudíž nutné titrovat na nejnižší dávku zajišťující kontrolu příznaků astmatu.
Dlouhodobá léčba pacientů vysokými dávkami inhalačních kortikosteroidů může vést k supresi nadledvin a akutní adrenální krizi. Děti a dospívající mladší 16 let užívající inhalačně vyšší, než doporučované dávky beklometason-dipropionátu mohou mít zvláště zvýšené riziko. Situace, které by mohly potenciálně vést k akutní adrenální krizi, zahrnují trauma, operaci, infekci nebo jakékoli rychlé snížení dávky. Úvodní příznaky jsou typicky vágní a mohou zahrnovat anorexii, bolesti břicha, pokles hmotnosti, únavu, bolesti hlavy, nevolnost, zvracení, hypotenzi, sníženou úroveň vědomí, hypoglykemii a záchvaty. Další krytí systémovými kortikosteroidy je nutné zvážit během období spojených se stresem nebo plánovaným chirurgickým výkonem.
Pacienti převádění z perorálních na inhalační kortikosteroidy mohou mít po významnou dobu přetrvávající zvýšené riziko narušené adrenální rezervy. Vyšší riziko mohou mít také pacienti, kteří vyžadovali vysokou akutní kortikosteroidní terapii v minulosti nebo podstoupili delší léčbu vysokými dávkami inhalačních kortikosteroidů. . Na tuto možnost reziduálního postižení je nutné vždy myslet v akutních případech a plánovaných situacích, které budou pravděpodobně spojené se stresem, a je nutné zvážit vhodnou kortikosteroidní léčbu. Rozsah adrenálního postižení může před plánovanými zákroky vyžadovat konzultaci se specialistou.
Combair Nexthaler je nutné podávat s opatrností u pacientů s aktivní nebo latentní plicní tuberkulózou, mykotickými a virovými infekcemi v dýchacích cestách.
Combair Nexthaler je nutné používat opatrně (může zahrnovat sledování) u pacientů se srdečními arytmiemi, hlavně atrioventrikulární blokádou třetího stupně a tachyarytmiemi, idiopatickou subvalvulární aortální stenózou, hypertrofickou obstrukční kardiomyopatií, ischemickou chorobou srdeční, závažným srdečním selháním, závažnou arteriální hypertenzí a aneuryzmatem.
Při léčbě pacientů se známým nebo suspektním prodloužením intervalu QTc, kongenitálním nebo farmakogenním (QTc >0,44 s), je nutné postupovat také opatrně. Samotný formoterol může indukovat prodloužení intervalu QTc.
Opatrně je také nutné postupovat při použití přípravku Combair Nexthaler u pacientů s thyreotoxikózou, diabetem mellitem, feochromocytomem a neléčenou hypokalémií.
Důsledkem terapie beta2-agonisty může být potenciálně závažná hypokalémie. Zvláštní pozornost je nutná u závažného astmatu, protože hypoxie může tento účinek potencovat. Hypokalémie může být také akcentována souběžnou terapií jinými léky, které mohou hypokalémii vyvolávat, jako např. deriváty xantinu, steroidy a diuretika (viz část 4.5). U nestabilního astmatu, kdy lze používat několik „záchranných“ bronchodilatátorů, je také nutné postupovat opatrně. V takových situacích doporučujeme sledovat sérové hladiny draslíku.
Inhalace formoterolu může vést ke zvýšení glykemie. Z toho důvodu je u pacientů s diabetem nutné pečlivě sledovat glykemii.
Pokud je plánována anestezie halogenovanými anestetiky, je nutné zabránit podání přípravku Combair Nexthaler po dobu minimálně 12 hodin před zahájením anestezie, jelikož hrozí srdeční arytmie.
Pacientům je třeba doporučit, aby si po inhalaci předepsané dávky vypláchli ústa, vykloktali vodou nebo si vyčistili zuby kartáčkem a minimalizovali tak riziko orofaryngeálních mykotických infekcí a dysfonie.
Laktóza obsahuje malé množství mléčných proteinů, které mohou vést k alergickým reakcím.
-
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Farmakokinetické interakce
Beklometason-dipropionát prochází velice rychlým metabolismem esterázovými enzymy.
Beklometason je méně závislý na metabolismu CYP3A než některé jiné kortikosteroidy a obecně jsou interakce nepravděpodobné. Nelze však zcela vyloučit riziko systémových účinků při konkomitantním použití silných inhibitorů CYP3A (např. ritonavir, cobicistat) a z toho důvodu je při použití takových látek nutné příslušné sledování.
Farmakodynamické interakce
Astmatici nesmí užívat žádné beta-blokátory (včetně očních kapek). Pokud budou ze závažných důvodů podávány beta-blokátory, účinek formoterolu bude snížen nebo zcela zrušen.
Použití jiných beta-adrenergních léků může mít potenciálně aditivní účinky. Z toho důvodu je při léčbě teofylinem nebo jinými beta-mimetiky předepisovanými společně s formoterolem nutné postupovat opatrně.
Souběžná léčba chinidinem, disopyramidem, prokainamidem, fenothiaziny, určitými antihistaminiky (např. tefrenadinem), inhibitory monoaminooxidázy a tricyklickými antidepresivy může prodloužit interval QTc a zvýšit riziko komorových arytmií.
Kromě toho mohou L-dopa, L-thyroxin, oxytocin a alkohol narušit srdeční toleranci vůči beta2-sympatomimetikům.
Souběžná léčba inhibitory monoaminooxidázy, včetně látek s podobnými vlastnostmi jako např. furazolidon a prokarbazin, může vést k hypertenzním reakcím.
Pacienti postupující souběžnou anestezii halogenovanými uhlovodíky mají zvýšené riziko arytmií.
Souběžná léčba deriváty xantinu, steroidy nebo diuretiky může potencovat hypokalemické účinky beta2-agonistů (viz bod 4.4). Hypokalémie může zvýšit predispozici na arytmie u pacientů léčených digitalisovými glykosidy.
4.6 Fertilita, těhotenství a kojení
Fertilita
Nejsou k dispozici žádné údaje pro člověka. Ve zvířecích studiích u potkanů byla přítomnost beklometason-dipropionátu ve vysokých dávkách v kombinaci spojena se sníženou fertilitou samic a embryotoxicitou (viz bod 5.3).
Těhotenství
Neexistují žádné relevantní klinické údaje o použití přípravku Combair Nexthaler u těhotných žen. Zvířecí studie používající kombinaci beklometason-dipropionátu a formoterolu prokázaly při vysoké systémové expozici známky reprodukční a fetální toxicity (viz bod 5.3). Vysoké dávky kortikosteroidů podávané březím zvířatům vedou k abnormalitám vývoje plodu, včetně rozštěpu patra a zpomalení nitroděložního růstu. Vzhledem k tokolytickým účinkům beta2-sympatomimetik je nutné krátce před porodem postupovat zvláště opatrně. Formoterol se nedoporučuje k použití během těhotenství a hlavně na konci těhotenství nebo během porodu, ledaže by neexistovala žádná jiná (bezpečnější) zavedená alternativa.
Podání přípravku Combair Nexthaler během těhotenství je vhodné zvážit pouze za předpokladu, že očekávané benefity převáží potenciální rizika.
Kojení Neexistují žádné relevantní klinické údaje o použití přípravku Combair Nexthaler během kojení u člověka.
I když nejsou k dispozici žádné údaje ze zvířecích studií, racionálně lze předpokládat, že beklometason-dipropionát se vylučuje do mléka jako jiné kortikosteroidy.
I když není známo, jestli formoterol prochází do lidského mateřského mléka, byl zjištěn v mléku kojících zvířat.
Podání přípravku Combair Nexthaler u kojících žen je vhodné zvážit pouze za předpokladu, že očekávané benefity převáží potenciální rizika. Je nutné rozhodnout, jestli přestat s kojením, nebo vysadit přípravek Combair Nexthaler. Je třeba zvážit benefit kojení pro dítě a benefit terapie pro ženu.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Combair Nexthaler nemá žádný nebo má jenom minimální vliv na schopnost řídit a obsluhovat stroje.
4.8 Nežádoucí účinky
Nejčastější nežádoucí reakcí je třes. Ve 12týdenním klinickém hodnocení s přípravkem Combair Nexthaler byl třes pozorován pouze u nejvyššího dávkovacího režimu (2 inhalace 2× denně). Rozvinul se nejčastěji na začátku léčby a měl mírnou intenzitu. Žádný pacient nebyl kvůli třesu z klinického hodnocení vyřazen.
Klinická hodnocení - zkušenosti u pacientů s astmatem
Bezpečnost přípravku Combair Nexthaler byla hodnocena v klinických hodnoceních s aktivní kontrolou a kontrolou placebem, ve kterých bylo 719 pacientům ve věku 12 let a starších s astmatem různé závažnosti podáno léčivo. Incidence nežádoucích účinků v tabulce níže se vztahuje k pacientům s astmatem ve věku 12 let a starších a je založena na bezpečnostních zjištěních dvou pivotních klinických hodnocení, kde byl Combair Nexthaler podáván v dávkách doporučovaných v tomto souhrnu údajů o přípravku po dobu 8 až 12 týdnů. V klinických hodnoceních s přípravkem Combair Nexthaler nebyly pozorovány žádné psychiatrické poruchy, jsou však zařazeny do tabulky jako potenciální účinek skupiny inhalačních kortikosteroidů .
Nežádoucí účinky spojené s beklometason-dipropionátem a formoterolem podávaných ve fixní kombinaci (Combair Nexthaler) jsou uvedené níže v seznamu podle orgánových tříd. Frekvence jsou definovány následovně: velmi časté (^ 1/10), časté (^ 1/100 až <1/10), méně časté (1/1 000 až <1/100), vzácné 1/10 000 až <1/1 000) a velmi vzácné (<1/10 000), není známo (z dostupných údajů nelze určit).
| Třída orgánových systémů | Nežádoucí účinek | Frekvence |
| Infekce a infestace | Nasofaryngitida | Méně časté |
| Ústní kandidóza | Méně časté | |
| Pneumonie (u pacientů s CHOPN) | Časté | |
| Poruchy metabolismu a výživy | Hypertriglyceridémie | Méně časté |
| Psychiatrické poruchy | Psychomotorická hyperaktivita, poruchy spánku, úzkost, deprese, agresivita, behaviorální změny (především u dětí) | Frekvence není známa |
| Poruchy nervového systému | Třes | Časté |
| Bolest hlavy | Méně časté | |
| Srdeční poruchy | Tachykardie | Méně časté |
| Sinusová bradykardie | Méně časté | |
| Angina pectoris | Méně časté | |
| Ischemie myokardu | Méně časté | |
| Respirační, hrudní a mediastinální poruchy | Podráždění hrdla, exacerbace astmatu | Méně časté |
| Dyspnoe | Méně časté | |
| Orofaryngeální bolest | Méně časté | |
| Dysfonie | Méně časté | |
| Kašel | Méně časté | |
| Gastrointestinální poruchy | Nevolnost | Méně časté |
| Celkové poruchy a reakce v místě aplikace | Únava | Méně časté |
| Podrážděnost | Méně časté | |
| Vyšetření | Prodloužení QT podle elektrokardiogramu | Méně časté |
| Snížená hladina volného kortizolu v moči | Méně časté | |
| Snížená hladina kortizolu v krvi | Méně časté |
| Zvýšená kalémie | Méně časté | |
| Zvýšená glykemie | Méně časté | |
| Opožděný nárůst kmitu R na elektrokardiogramu | Méně časté |
Mezi pozorované nežádoucí účinky typicky spojené s formoterolem patří: třes, bolesti hlavy, tachykardie, sinusová bradykardie, angina pectoris, ischemie myokardu, prodloužení QT.
Mezi pozorované nežádoucí účinky typicky spojené s beklometason-dipropionátem patří: nasofaryngitida, ústní kandidóza, dysfonie, podráždění krku, iritabilita, snížená hladina volného kortizolu v moči, snížená hladina kortizolu v krvi, zvýšená glykemie.
Další nežádoucí účinky nepozorované v rámci klinického použití přípravku Combair Nexthaler, ale typicky spojené s inhalačním podáním beklometason-dipropionátu jsou ústní mykózy a pneumonie. Během terapie inhalačními kortikostereoidy byly vzácněji pozorovány poruchy chuti.
Opatření za účelem minimalizace ústních mykóz, ústní kandidózy a dysfonie naleznete v bodu 4.4.
Systémové účinky inhalačních kortikosteroidů (např. beklometason-dipropionát) se mohou rozvinout hlavně při podání ve vysokých dávkách předepisovaných po delší období. Mohou zahrnovat následující: Cushingův syndrom, Cushingoidní rysy, supresi nadledvin, sníženou kostní minerálovou denzitu, růstovou retardaci u dětí a dospívajících, kataraktu a glaukom (viz také bod 4.4).
Další nežádoucí účinky nebyly u terapeutických dávek přípravku Combair Nexthaler v klinické praxi pozorovány, jsou však typicky spojené s podáváním beta2-agonistů, jako je např. formoterol: palpitace, fibrilace síní, komorové extrasystoly, tachyarytmie, potenciálně závažná hypokalémie a zvýšení/snížení krevního tlaku. Insomnie, závratě, neklid a úzkost byly vzácněji hlášeny během inhalační terapie formoterolem. Formoterol může také způsobovat svalové křeče a myalgii.
Byly také hlášené reakce z přecitlivělosti, včetně vyrážky, kopřivky, svědění, zarudnutí a otoku očí, obličeje, rtů a hrdla (angioedém).
Podobně jako u jiných inhalačních terapií se může vyskytnout po podání dávky paradoxní bronchospazmus projevující se okamžitým zvýšením sípání, kašlem a dyspnoí (viz také bod 4.4).
Pediatrická populace
Nejsou k dispozici žádné informace o bezpečnosti přípravku Combair Nexthaler u dětí mladších 11 let. Dostupné jsou pouze omezené informace pro dospívající ve věku 12 až 17 let. Ve 12týdenním randomizovaném klinickém hodnocení u dospělých a dospívajících dostalo 162 dospívajících ve věku 12 až 17 let se středně závažným až závažným astmatem přípravek Combair Nexthaler nebo příslušný inhalační roztok v tlakovém aplikátoru, 1 nebo 2 inhalace 2× denně. Frekvence, typ a závažnost nežádoucích lékových reakcí se u dospívajících a dospělých nelišily.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
Webové stránky:
4.9 Předávkování
Nejvyšší doporučená dávka přípravku Combair Nexthaler v jednom podání jsou 2 inhalace. U pacientů s astmatem byly hodnoceny 4 kumulativní inhalace přípravku Combair Nexthaler (celková dávka beklometason-dipropionátu 400 mikrogramů, formoterolu 24 mikrogramů podaná v jedné dávce). Kumulativní léčba nevedla k abnormálním klinicky relevantním účinkům na životní funkce a nebyly pozorovány závažné ani těžké nežádoucí reakce (viz také bod 4.8).
U inhalačního roztoku v tlakovém aplikátoru byly u pacientů s astmatem hodnoceny inhalované dávky s až 12 kumulativními aktivacemi (celková dávka beklometason-dipropionátu 1 200 mikrogramů, formoterolu 72 mikrogramů). Kumulativní léčba nevedla k abnormálním účinkům na životní funkce a nebyly pozorovány závažné ani těžké nežádoucí reakce.
Nadměrné dávky formoterolu mohou vést k účinkům typickým pro beta2-agonisty, jako jsou: nauzea, zvracení, bolesti hlavy, třes, somnolence, palpitace, tachykardie, komorové arytmie, prodloužení intervalu QTc, metabolická acidóza, hypokalémie, hyperglykemie.
V případě předávkování formoterolem je indikována podpůrná a symptomatická léčba. Závažné případy je třeba hospitalizovat. Lze zvážit použití kardioselektivních beta-blokátorů. V takovém případě je nutné postupovat zvláště opatrně, jelikož použití beta-blokátorů může vyvolat bronchospazmus. Je třeba sledovat sérovou hladinu draslíku.
Akutní inhalace dávek beklometason-dipropionátu přesahujících doporučenou hodnotu může vést k dočasné supresi nadledvinových funkcí. Tato změna nevyžaduje akutní zásah, jelikož se nadledvinové funkce obnoví za několik dní, co lze ověřit podle plazmatické hladiny kortizolu. U těchto pacientů je potřeba pokračovat v léčbě v dávce dostatečné pro kontrolu astmatu.
Chronické předávkování inhalovaným beklometason-dipropionátem: riziko suprese nadledvin (viz bod 4.4). Může být nutné sledovat adrenální rezervu. V léčbě je třeba pokračovat v dávce dostatečné pro kontrolu astmatu.
Jednorázové supraterapeutické dávky beklometason-dipropionátu do 800 mikrogramů a do 48 mikrogramů formoterolu podané pomocí aplikátoru Combair Nexthaler jsou obecně bezpečné a dobře tolerované.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: adrenergní přípravky, inhalační přípravky: formoterol a jiná léčiva onemocnění spojených s obstrukcí dýchacích cest.
ATC kód: R03AK08.
Mechanismus účinku a farmakodynamické účinky
Přípravek Combair Nexthaler obsahuje beklometason-dipropionát a formoterol ve formulaci jako suchý prášek, díky čemu vzniká extra jemný (extra-fine) aerosol s průměrným hmotnostním mediánovým aerodynamickým průměrem (MMAD) v rozmezí 1,4 až 1,5 mikrometru a s ko-depozicí dvou komponent. Aerosolové částečky přípravku Combair Nexthaler jsou v průměru mnohem menší než částečky obsažené v jiných non-extra-fine formulacích přípravků.
Studie ukládání radiofarmaka u dospělých pacientů prokázaly, že vysoký podíl léku (odhadem 42 % nominální dávky) se ukládá v plicích s homogenním uložením v dýchacích cestách. Tyto charakteristiky aplikace podporují použití nízké dávky kortikosteroidu se zvýšenými lokálními farmakodynamickými účinky, které jsou prokazatelně ekvivalentní příslušnému inhalačnímu roztoku v tlakových aplikátorech (viz Klinické zkušenosti).
Dvě látky obsažené v přípravku Combair Nexthaler mají odlišné mechanismy účinku. Také u této kombinace, podobně jako u jiných kombinací inhalačních kortikosteroidů a beta2-agonistů, byly zjištěny aditivní účinky na snížení počtu exacerbací astmatu.
Beklometason-dipropionát
Beklometason-dipropionát podávaný inhalačně v doporučovaných dávkách má glukokortikoidní protizánětlivý účinek v plicích, což vede ke ztlumení příznaků a exacerbaci astmatu s méně závažnými nežádoucími účinky než při systémovém podání kortikosteroidů.
Formoterol
Formoterol je selektivní beta2-agonista vedoucí k relaxaci bronchiální hladké svaloviny u pacientů s reverzibilní obstrukcí dýchacích cest. Bronchodilatační účinky nastupují rychle do 1 až 3 minut po inhalaci a trvají 12 hodin po podání dávky.
Klinické zkušenosti
Účinnost dvou komponent prášku k inhalaci Combair Nexthaler byla hodnocena ve třech samostatných klinických hodnoceních ve srovnání se 100 mikrogramy / 6 mikrogramy inhalačního roztoku v tlakových aplikátorech u pacientů se středně těžkým až těžkým persistentním astmatem. Celkově se v klinické praxi očekává srovnatelná účinnost obou typů inhalátorů u 1 i 2 inhalací 2× denně.
-
V jednom klinickém hodnocení bylo primárním cílem vyhodnocení účinnosti inhalační kortikosteroidní komponenty na bronchodilataci (FEV1 před dávkou). Ke klinicky významnému zlepšení FEV1 před dávkou došlo u 696 pacientů se středně těžkým až těžkým symptomatickým astmatem na konci 3měsíčního léčebného období ve srovnání s výchozími hodnotami s 1 inhalací 2× denně a 2 inhalacemi 2× denně u obou formulací přípravku. Došlo ke střednímu nárůstu na úrovni minimálně 250 ml. Mezi FEV1 před dávkou u prášku k inhalaci Combair Nexthaler a inhalačním roztokem v tlakovém aplikátoru nebyl v žádné dávce pozorován klinicky relevantní rozdíl. U ranního PEF byla pozorována významná reakce na dávku. Statistická významnost pro odpověď na dávku nebyla dosažena u FEV1 před dávkou. Parametry kompenzace astmatu jako ranní a večerní skóre příznaků astmatu a procentuální podíl dní bez příznaků se při srovnání výchozí úrovně a konce léčebného období významně zlepšily, hlavně u dvou vysokých dávek obou formulací přípravku.
-
V druhém klinickém hodnocení bylo primárním cílem stanovit účinnost komponenty Combair Nexthaler s dlouhodobým beta2-adrenergním účinkem. V tomto klinickém hodnocení byla měřena bronchodilatace na začátku a až 12 hodin po podání jedné dávky sériovými spirometrickými hodnoceními FEV1 (FEV1 AUC během minimálně 80 % délky účinku formoterolu). Ve srovnání s placebem vedla jedna inhalace a čtyři inhalace obou účinných látek přípravku Combair Nexthaler k významnému zlepšení FEV1 AUC0–12. Obě dávky prášku k inhalaci Combair Nexthaler byly non-inferiorní k odpovídající dávce inhalačního roztoku v tlakovém aplikátoru. Statisticky významná odpověď na dávku byla pozorována u obou formulací mezi nízkou a vysokou dávkou.
-
V dalším otevřeném klinickém hodnocení s placebem bylo prokázáno analýzou inspiračního profilu pomocí systému Combair Nexthaler, že pacienti s mírnou až těžkou CHOPN, bez ohledu na jejich funkční omezení, byli schopni prostředek efektivně aktivovat a používat.
Pediatrická populace
Evropská léková agentura poskytla odklad povinnosti předložit výsledky klinických hodnocení u astmatu s přípravkem Combair Nexthaler u věkových podskupin pediatrické populace 5 až 11 a 12 až 17 let.
-
V době přípravy dokumentu nebyly k dispozici žádné klinické zkušenosti s přípravkem Combair Nexthaler u dětí ve věku 5 až 11 let. Dostupné jsou pouze omezené informace pro dospívající ve věku 12 až 17 let.
Ve 3měsíčním randomizovaném klinickém hodnocení dostávalo 162 dospívajících ve věku 12 až 17 let s diagnózou středně těžkého až těžkého astmatu přípravek Combair Nexthaler nebo odpovídající inhalační roztok v tlakovém aplikátoru, 1 nebo 2 inhalace 2× denně. Změna FEV1 před dávkou na konci léčby byla u dospívajících významnější než u dospělých.
Informace o pediatrickém použití naleznete také v bodech 4.2 a 4.8.
5.2 Farmakokinetické vlastnosti
Beklometason-dipropionát
Beklometasondipropionát je pro-léčivo se slabou vazebnou afinitou vůči receptoru pro glukokortikoidy, který se hydrolyzuje esterázovými enzymy na aktivní metabolit beklometason-17-monopropionát s potentnější topickou protizánětlivou aktivitou ve srovnání s pro-léčivem beklometason-dipropionátem.
Absorpce, distribuce a metabolismus
Inhalačně podaný beklometason-dipropionát se rychle absorbuje plícemi: před absorpcí probíhá intenzivní konverze na aktivní metabolit beklometason-17-monopropionát esterázovými enzymy, které se nachází ve většině tkání. Systémová dostupnost aktivního metabolitu pochází z plic a z gastrointestinální absorpce spolykané dávky. Biologická dostupnost spolykaného beklometason-dipropionátu je však zanedbatelná. Presystémová konverze na beklometason-17-monopropionát vede k absorpci části dávky v podobě aktivního metabolitu.
Se zvyšující se inhalovanou dávkou dochází k přibližně lineárnímu vzestupu systémové expozice. Absolutní biologická dostupnost po inhalaci z tlakového inhalátoru s odměřenou dávkou je přibližně 2 % nominální dávky nezměněného beklometason-dipropionátu a 62 % pro beklometason-17-monopropionát.
Po intravenózním podání jsou dispozice beklometason-dipropionátu a jeho aktivního metabolitu charakterizovány vysokou plazmatickou clearance (150, resp. 120 l/h), s malým distribučním objemem v rovnovážném stavu pro beklometason-dipropionát (20 l) a větší tkáňovou distribucí pro jeho aktivní metabolit (424 l). Metabolická dispozice beklometason-dipropionátu vede hlavně (82 %) ke vzniku jeho aktivního metabolitu beklometason-17-monopropionátu.
Vazba na plazmatické proteiny je středně vysoká (87 %).
Vylučování
Fekální vylučování je hlavní cestou eliminace beklometason-dipropionátu zejména v podobě polárních metabolitů. Renální vylučování beklometason-dipropionátu a jeho metabolitů je zanedbatelné. Poločasy terminální eliminace jsou 0,5 h pro beklometason-dipropionát a 2,7 h pro beklometason-17-monopropionát.
Zvláštní populace
Farmakokinetika beklometason-dipropionátu u pacientů s renální nebo jaterní dysfunkcí nebyla předmětem studií. Jelikož však beklometason-dipropionát prochází velice rychlým metabolismem esterázovými enzymy přítomnými ve střevní tekutině, séru, plicích a játrech za vzniku polárnějších produktů beklometason-21-monopropionátu, beklometason-17-monopropionátu a beklometasonu, jaterní dysfunkce pravděpodobně nepovede ke změně farmakokinetiky a bezpečnostního profilu beklometason-dipropionátu.
Jelikož beklometason-dipropionát nebo jeho metabolity nebyly zjištěny v moči, u pacientů s renální dysfunkcí se neočekává zvýšení systémové expozice.
Formoterol
Absorpce a distribuce
Po inhalaci se formoterol absorbuje z plic a z gastrointestinálního traktu. Frakce, která se po inhalaci spolkne po podání pomocí inhalátoru (MDI) může kolísat mezi 60 % – 90 %.
Nejméně 65 % frakce, která je spolknutá, se absorbuje z gastrointestinálního traktu. Nejvyšší koncentrace nezměněné látky v plasmě je dosaženo za 30 minut až za 1 hod po perorálním podání. Na plazmatické proteiny se váže 61 až 64 % (34 % na albuminy); při terapeutickém dávkování nejsou vazebná místa saturována. Eliminační biologický poločas po perorálním podání byl určen na 2 až 3 hodiny. Absorpce formoterolu po inhalaci 12 až 96 ^g formoterol-fumarátu je v závislosti na dávce lineární.
Biotransformace
Formoterol se primárně metabolizuje přímou konjugací na fenolovou hydroxylovou skupinu. Konjugace s kyselinou glukuronidovou metabolit inaktivuje. Další cesta biotransformace je O-demetylace na fenolovou 2-hydroxylovou skupinu s následnou konjugací.
Isoenzymy cytochromu CYP450 (CYP2D6, CYP2C19 a CYP2C9) se podílejí na O-demetylaci formoterolu. Hlavním místem metabolizace jsou tedy játra. Formoterol v terapeuticky relevantních koncentracích neinhibuje CYP450.
Eliminace
Kumulativní exkrece formoterolu se po jednorázovém inhalačním podání zvyšuje z práškového inhalátoru lineárně v rozmezí dávek 12 – 96 ^g. Průměrně je vyloučeno 8 % podané dávky jako nezměněný formoterol a 25 % jako celkový formoterol. Na základě plasmatické koncentrace měřené po inhalaci jednotlivé dávky 120 ^g 12 zdravým dobrovolníkům byl určen střední terminální eliminační poločas na 10 hodin. (R,R)- a (S,S)-enantioméry představují kolem 40 % a 60 % nezměněné látky vylučované do moče. Relativní proporce dvou enantiomérů zůstává ve studovaném dávkovém rozmezí konstantní a akumulace těchto enantiomerů po opakovaných dávkách nebyla zjištěna.
Po podání perorální dávky (od 40 do 80 |jg) bylo u zdravých dobrovolníků v moči zjištěno 6 – 10 % nezměněné látky a 8 % látky ve formě glukuronidu.
Celkově 67 % perorálně podané dávky formoterolu je vylučováno do moče (hlavně jako metabolity) a zbytek je vylučováno stolicí. Renální clearance formoterolu je 150 ml/min.
Zvláštní populace
Jaterní/renální postižení: farmakokinetika formoterolu u pacientů s jaterním nebo renálním postižením nebyla hodnocena.
Klinické zkušenosti
Systémová expozice beklometason-dipropionátu a formoterolu v kombinaci byla porovnána s jednotlivými složkami. Nebyly zjištěny žádné známky farmakokinetických nebo farmakodynamických (systémových) interakcí mezi beklometason-dipropionátem a formoterolem.
Farmakokinetika prášku k inhalaci Combair Nexthaler byla srovnána s farmakokinetikou odpovídajícího inhalačního roztoku v tlakovém aplikátoru. Analýza steroidní komponenty byla zaměřena na beklometason-17-monopropionát, hlavní aktivní metabolit beklometason-dipropionátu. Systémová absorpce a metabolismus beklometason-dipropionátu byly rychlé a Cmax byla dosažena 5 minut po podání dávky u obou léčeb, ale byla vyšší (+68 %) u prášku k inhalaci přípravku Combair Nexthaler. AUCt byla asi 3× vyšší po inhalaci přípravku Combair Nexthaler přes inhalátor Nexthaler ve srovnání s inhalačním roztokem v tlakovém aplikátoru. Cmax pro beklometason-17-monopropionát, hlavní aktivní metabolit představující asi 82 % celkové hladiny v krvi, byla dosažena v průměru po 30 minutách při použití systému Nexthaler a po 15 minutách po použití inhalačního roztoku v tlakovém aplikátoru. Plazmatická koncentrace beklometason-17-monopropionátu byla nižší (Cmax –49 % a AUCt –29 %) po inhalaci prášku k inhalaci než u inhalačního roztoku v tlakovém aplikátoru. Po inhalaci přípravku Combair Nexthaler pomocí inhalátoru Nexthaler byla maximální koncentrace (Cmax) formoterolu dosažena do 5 minut a byla vyšší (+47 %) pro prášek k inhalaci, kdežto celková expozice (AUCt) byla u obou terapií srovnatelná.
V jednom klinickém hodnocení bylo analyzováno relativní dodání do plic prostřednictvím blokády pomocí aktivního uhlí s cílem vyloučit absorpci léčiva z gastrointestinálního traktu. Byl použit schválený spacer AeroChamber Plus pro referenční přípravek (inhalační roztok v tlakovém aplikátoru). Za těchto podmínek se Nexthaler a inhalační roztok v tlakovém aplikátoru ukázaly jako ekvivalentní pro AUCt beklometason-17-monopropionátu i formoterolu (poměr pro prášek k inhalaci / inhalační roztok v tlakovém aplikátoru a 90% intervaly spolehlivosti spadaly do rozmezí 80125 %). Cmax beklometason-17-monopropionátu však byla nižší (-38 %) po inhalaci pomocí systému Nexthaler.
5.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické údaje individuálních komponen přípravku Combair Nexthaler založené na konvenčních studiích farmakologie bezpečnosti a toxicity po opakovaném podání neodhalují žádná speciální rizika pro člověka. Profil toxicity kombinace ukazuje, že jednotlivé komponenty nevedou ke zvýšení toxicity nebo neočekávaným zjištěním.
Reprodukční studie u potkanů prokázaly účinky závislé na dávce. Přítomnost beklometason-dipropionátu ve vysokých dávkách byla spojena se sníženou fertilitou samic, sníženým počtem implantací a embryofetální toxicitou. Vysoké dávky kortikosteroidů podávané březím zvířatům vedou k abnormalitám fetálního vývoje, včetně rozštěpu patra a zpomalení nitroděložního růstu. Je pravděpodobné, že účinky pozorované u kombinace beklometason-dipropionát/formoterol byly způsobené beklometason-dipropionátem. Tyto účinky byly pozorovány pouze u vysoké systémové expozice aktivnímu metabolitu beklometason-17-monopropionátu (více než 200násobek očekávané plazmatické hladiny u pacientů). Kromě toho byly ve zvířecích studiích pozorovány delší trvání gestace a porodu, vliv, který lze připsat známým tokolytickým účinkům beta2-sympatomimetik. Tyto účinky byly pozorovány u hladin formoterolu v plazmě samic nižších než hladiny očekávané u pacientů léčených přípravkem Combair Nexthaler.
Studie genotoxicity provedené s kombinací beklometason-dipropionát/formoterol neprokazují mutagenní potenciál. S navrhovanou kombinací nebyly provedeny žádné studie karcinogenity. Zvířecí údaje hlášené pro individuální složky nesvědčí pro žádné potenciální riziko karcinogenity u člověka.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Monohydrát laktózy (který obsahuje malé množství mléčných proteinů) Magnesium-stearát
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
3 roky.
Po prvním otevření foliového sáčku je nutné léčivý přípravek použít do 6 měsíců.
6.4 Zvláštní opatření pro uchovávání
Uchovávejte v původním obalu, aby byl přípravek chráněn před vlhkostí.
Inhalátor vyjměte z fóliového sáčku až krátce před prvním použitím.
Před prvním otevřením foliového sáčku:
Tento léčivý přípravek nevyžaduje žádné zvláštní teplotní podmínky uchovávání.
Po prvním otevření foliového sáčku:
Neuchovávejte při teplotě nad 25 °C.
6.5 Druh obalu a velikost balení
Jedno balení obsahuje 1, 2 nebo 3 inhalátory Nexthaler, každý z nich obsahuje 1,50 g prášku k inhalaci a poskytuje 120 inhalací. Inhalátor je uložen v tepelně uzavřeném ochranném vaku (fóliovém sáčku) vyrobeném z PET/Al/PE (polyetylentereftalát/hliník/polyetylen) nebo PA/Al/PE (polyamid/hliník/polyetylen).
Na trhu nemusí být všechny velikosti balení.
Combair Nexthaler je vícedávkový inhalační prostředek. Inhalátor se skládá z obalu ze spodního krytu s okénkem zobrazujícím zbývající počet dávek a zabudovaným krytem. Po otevření krytu, kterým se také pohání mechanismus počítadla dávek, se odhalí náustek, přes který se léčivo inhaluje. Spodní kryt a náustek jsou vyrobeny z akrylonitrilbutadienstyrénu a kryt je vyroben z polypropylenu.
6.6 Zvláštní opatření pro likvidaci přípravku
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidovány v souladu s místními požadavky.
Níže je uveden návod k použití inhalátoru Nexthaler pro potřeby zdravotníků.
NÁVOD K POUŽITÍ INHALÁTORU NEXTHALER
A. Obsah balení
Toto balení obsahuje:
- 1 informační leták s pokyny,
- 1 inhalátor Nexthaler uvnitř uzavřeného ochranného foliového sáčku.
Pokud obsah balení neodpovídá uvedenému seznamu, vraťte inhalátor osobě, která vám jej vydala, a pořiďte si nový.
B. Zvláštní upozornění a bezpečnostní opatření
- Nevytahujte inhalátor z foliového sáčku, pokud jej nechcete ihned použít.
- Svůj inhalátor používejte výhradně podle pokynů.
- Pokud si nejste jistý(á), jestli po jedné inhalaci pokleslo číslo na počítadlu dávek, počkejte na svou další plánovanou dávku a užijte ji jako normálně. Neužívejte dávku navíc.
- Ponechte kryt uzavřený, dokud nebudete potřebovat další dávku z inhalátoru.
- Když inhalátor nepoužíváte, uchovávejte jej na čistém a suchém místě.
- Nesnažte se ze žádného důvodu inhalátor Nexthaler rozebírat.
- Nepoužívejte inhalátor Nexthaler:
o po uplynutí data spotřeby,
o pokud od otevření foliového sáčku uplynulo více než 6 měsíců,
o pokud je poškozen,
o pokud je v okénku počítadla dávek uvedena hodnota „0“,
o pokud nelze odečíst okénko počítadla dávek.
V takových případech svůj inhalátor zlikvidujte nebo jej vraťte osobě, která vám jej vydala, a pořiďte si nový. Zeptejte se svého lékárníka, jak máte likvidovat inhalátory, které již nepotřebujete.
C. Hlavní součásti inhalátoru Nexthaler
Vstup vzduchu
Okénko počítadla dávek
Kryt
náustek
r
o o o
IXO O o o o o
o o o :
Užití dávky z inhalátoru Nexthaler vyžaduje pouze tři jednoduché kroky: otevřít, inhalovat, zavřít.
-
D. Před použitím nového inhalátoru Nexthaler
1.
o Nepoužívejte inhalátor, pokud foliový sáček není uzavřený nebo je poškozený -vraťte jej osobě, která vám jej vydala, a pořiďte si nový.
2.
o Pokud se váš inhalátor zdá být rozbitý nebo poškozený, vraťte jej osobě, která vám jej vydala, a pořiďte si nový.
3.
o Nepoužívejte nový inhalátor, pokud je uvedeno číslo nižší než „120“ – vraťte jej osobě, která vám jej vydala, a pořiďte si nový.
-
E.1. Vizuální kontrola
1. Zkontrolujte zbývající počet dávek: jakékoli číslo v rozmezí
o Pokud je v okénku počítadla dávek uvedena hodnota „0“, nezbývají žádné dávky -zlikvidujte svůj inhalátor a pořiďte si nový.
-
2. Před použitím se ujistěte, že je kryt zcela zavřený.
E.2. Otevřít
-
1. Pevně uchopte inhalátor ve vzpřímené poloze.
-
2. Zcela otevřete kryt.
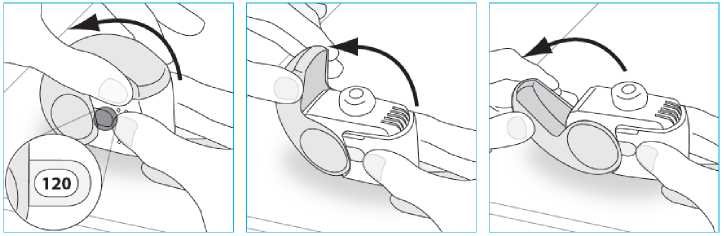
-
3. Před inhalací vydýchněte, jak nejvíce to půjde. o Nevydechujte přes inhalátor.
E.3. Inhalovat
Kdykoli to bude možné, při inhalaci seďte vzpřímeně nebo stůjte.
-
1. Zvedněte inhalátor, přiložte si jej k ústům a obemkněte náustek rty.
o Nezakrývejte vstup vzduchu, když budete držet inhalátor.
o Nevdechujte přes vstup vzduchu.
-
2. Rychle a zhluboka se nadechněte ústy.
o Při užívání dávky si můžete všimnout určité chuti.
o Když užijete dávku, můžete slyšet nebo pocítit cvaknutí.
o Neinhalujte přes nos.
o Neoddalujte inhalátor během inhalace od svých rtů.
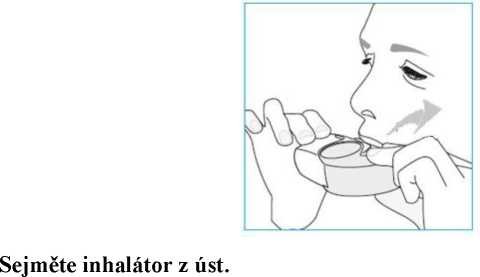
-
4. Zadržte dech na 5 až 10 sekund nebo co nejdéle to bude možné.
-
5. Pomalu vydechněte.
o Nevydechujte přes inhalátor.
E.4. Zavřít
-
1. Přesuňte inhalátor zpět do vzpřímené polohy a zcela zavřete kryt.
-
2. Zkontrolujte, že počítadlo dávek ukazuje číslo o jedno nižší než před inhalací.
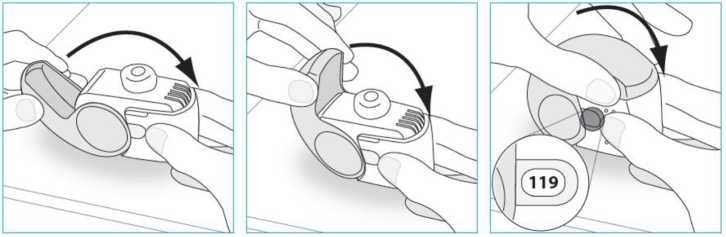
-
3. Pokud je třeba užít další dávku, zopakujte kroky E.1 až E.4.
- Za normálních okolností není nutné inhalátor čistit.
- V případě potřeby můžete inhalátor po použití vyčistit suchým hadříkem nebo papírovým kapesníkem.
- Když svůj inhalátor nepoužíváte, uchovávejte jej na čistém a suchém místě. Po použití jej můžete vložit zpět do foliového sáčku.
o Nevystavujte inhalátor horku ani přímému slunečnímu světlu.
o Nevystavujte inhalátor vlhkému ani mokrému prostředí.
- Uchovávejte mimo dohled a dosah dětí.
- Pokud byl inhalátor uchováván déle než 6 měsíců od otevření foliového sáčku, zlikvidujte jej a pořiďte si nový.
- Pokud číslo v okénku počítadla dávek ukazuje hodnotu „0“, svůj inhalátor Nexthaler zlikvidujte.
- Zeptejte se svého lékárníka, co dělat s léky, které jste doužívali nebo již nepotřebujete.
o Nevyhazujte léky do běžného domovního odpadu.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Chiesi Pharmaceuticals GmbH, Gonzagagasse16/16, 1010 Vídeň, Rakousko
8. REGISTRAČNÍ ČÍSLO
14/266/17-C
Další informace o léčivu COMBAIR NEXTHALER
Jak
se COMBAIR NEXTHALER
podává: inhalační podání - prášek k inhalaci
Výdej
léku: na lékařský předpis
Balení: Vícedávkový obal
Velikost
balení: 3X120DÁV
Držitel rozhodnutí o registraci daného léku v České republice:
Chiesi Pharmaceuticals GmbH, Vídeň
E-mail: chiesi-cz@chiesi.com
Telefon: 420 261 221 745
