Souhrnné informace o léku - BERODUAL N
1. NÁZEV PŘÍPRAVKU
Roztok k inhalaci v tlakovém obalu
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 odměřená dávka (střik) obsahuje ipratropii bromidum 0,020 mg, což odpovídá ipratropii bromidum monohydricum 0,021 mg, a fenoteroli hydrobromidum 0,050 mg.
Pomocné látky: 1 odměřená dávka (střik) obsahuje až 13,313 mg ethanolu.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Roztok k inhalaci v tlakovém obalu
Popis přípravku: čirá, bezbarvá až světležlutá nebo světlehnědá kapalina, bez viditelných částic.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Berodual N je bronchodilatační přípravek určený k prevenci a léčbě příznaků chronické bronchiální obstrukce spojené s reverzibilním zúžením dýchacích cest, jako je bronchiální astma, a zejména k prevenci a léčbě chronické obstrukční bronchitidy s emfyzémem či bez něj. U pacientů s bronchiálním astmatem nebo u pacientů s CHOPN, která reaguje na léčbu kortikosteroidními přípravky, je třeba uvažovat i o současné aplikaci protizánětlivé léčby.
4.2 Dávkování a způsob podání
1. NÁZEV PŘÍPRAVKU
BERODUAL N
Roztok k inhalaci v tlakovém obalu
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 odměřená dávka (střik) obsahuje ipratropii bromidum 0,020 mg, což odpovídá ipratropii bromidum monohydricum 0,021 mg, a fenoteroli hydrobromidum 0,050 mg.
Pomocné látky: 1 odměřená dávka (střik) obsahuje až 13,313 mg ethanolu.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Roztok k inhalaci v tlakovém obalu
Popis přípravku: čirá, bezbarvá až světležlutá nebo světlehnědá kapalina, bez viditelných částic.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Berodual N je bronchodilatační přípravek určený k prevenci a léčbě příznaků chronické bronchiální obstrukce spojené s reverzibilním zúžením dýchacích cest, jako je bronchiální astma, a zejména k prevenci a léčbě chronické obstrukční bronchitidy s emfyzémem či bez něj. U pacientů s bronchiálním astmatem nebo u pacientů s CHOPN, která reaguje na léčbu kortikosteroidními přípravky, je třeba uvažovat i o současné aplikaci protizánětlivé léčby.
4.2 Dávkování a způsob podání
Dávkování
Dávkování je nutno individuálně upravit. Není-li lékařem předepsáno jinak, je doporučeno následující dávkování pro dospělé a děti starší 6 let.
Akutní astmatický záchvat:
Podání 2 inhalačních dávek (vdechů) je ve většině případů dostačující k rychlému odstranění akutních příznaků. Nedošlo-li v těžších případech ke zmírnění nebo odstranění dýchacích potíží během následujících 5 minut, je možno opakovat stejnou dávku (2 vdechy).
Pokud se záchvat nepodaří zvládnout čtyřmi vdechy, je pravděpodobně nutné podání dalších dávek. V těchto případech by měl být pacient poučen, aby neprodleně vyhledal lékařskou pomoc.
Intermitentní a dlouhodobé podávání:
(Berodual N se užívá při astmatu pouze příležitostně).
1–2 vdechy při každém podání, maximálně 8 vdechů denně (zpravidla 1–2 vdechy 3× denně). Přípravek lze podávat dětem pouze po poradě s lékařem a pod dohledem dospělé osoby.
Způsob použití
Správný způsob použití inhalátoru je předpokladem úspěšné léčby.
Před
Odstraňte ochranný kryt a stiskněte dvakrát dávkovací ventil.
Před
-
1. Odstraňte ochranný kryt. Pokud nebyl přípravek použit 3 dny, je třeba před aplikací jednou stisknout dávkovací ventil.
-
2. Zhluboka vydechněte.
-
3. Inhalátor držte v poloze zobrazené na obrázku č. 1, ústní nástavec sevřete rty. Dno tlakového obalu (kovové tlakové nádobky) a šipka na ní směřuje vzhůru.
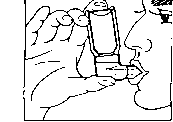
-
4. Zhluboka se nadechněte a na začátku tohoto nádechu stiskněte rázně dávkovací ventil, který uvolní jednu odměřenou dávku. Zadržte dech na několik sekund (nejlépe 5–10 s), vyjměte ústní nástavec z úst a vydechněte. Při podání druhé dávky, pokud je to potřebné, postupujte stejným způsobem (viz body 2 – 4).
-
5. Po použití nasaďte zpět ochranný kryt.
Kovová tlaková nádobka je neprůhledná, nelze tedy sledovat hladinu přípravku a zrakem zjistit, kdy je spotřebován. Přípravek obsahuje 200 dávek léku. Poté, co byly aplikovány, může kovová tlaková nádobka stále ještě obsahovat určité množství tekutiny. Je však nutno užít nové balení přípravku, protože při dalších aplikacích by dávka inhalovaného léku nemusela být správná.
Množství zbývajícího léku lze ověřit následovně:
Protřepáním kovové tlakové nádobky můžete zjistit, zda ještě obsahuje tekutinu. Nebo vyjměte kovovou tlakovou nádobku s roztokem z umělohmotného ústního nástavce a vložte ji do větší nádoby naplněné vodou. Obsah roztoku v kovové tlakové nádobce lze odhadnout podle pozice, kterou tato nádobka ve vodní lázni zaujme (viz obr. 2).

Obr. 2
Čištění ústního nástavce inhalátoru provádějte nejméně jednou týdně. Je důležité udržovat ústní nástavec inhalátoru v čistotě, aby nedošlo k poruše funkce spreje ucpáním nečistotami.
Při čištění nejprve sejměte ochranný kryt a vyjměte kovovou tlakovou nádobku z inhalátoru. Proplachujte teplou vodou ústní nástavec inhalátoru tak dlouho, dokud nejsou viditelné žádné nečistoty.
Obr. 3
Po vyčištění ústní nástavec inhalátoru vytřepejte a nechte volně uschnout na vzduchu. Při sušení nepoužívejte teplo.
Jakmile ústní nástavec inhalátoru vyschne, složte ochranný kryt a kovovou tlakovou nádobku opět dohromady.
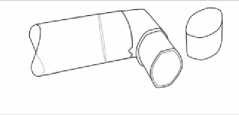
Obr. 4
Varování: Umělohmotný ústní nástavec inhalátoru byl vyroben pouze pro použití s roztokem k inhalaci v tlakovém obalu Berodual N tak, aby vždy byla zajištěna inhalace optimálního množství přípravku. Ústní nástavec inhalátoru proto nesmí být používán s jinými roztoky k inhalaci a roztok k inhalaci v tlakovém obalu Berodual N nesmí být používán s jiným ústním nástavcem, než který je dodáván spolu s přípravkem.
Kovová tlaková nádobka je pod stálým tlakem, nesmí být otevírána násilím a vystavena teplotě nad 50°C.
4.3 Kontraindikace
Berodual N je kontraindikován u pacientů se známou hypersenzitivitou na fenoterol-hydrobromid, látky podobné atropinu nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
Berodual N je také kontraindikován u pacientů s hypertrofickou obstrukční kardiomyopatií a tachyarytmií.
4.4 Zvláštní upozornění a opatření pro použití
Hypersenzitivita
Po podání přípravku Berodual N se mohou vyskytnout tzv. časné reakce hypersenzitivity, o čemž svědčí vzácné případy kopřivky, angioedému, vyrážky, bronchospazmu, orofaryngeálního edému a anafylaxe.
Paradoxní bronchospazmus
Stejně jako u jiných inhalačních léků může také Berodual N vést k paradoxnímu bronchospazmu, který může být život ohrožující. Pokud dojde k paradoxnímu bronchospazmu, léčba přípravkem Berodual N by měla být okamžitě přerušena a nahrazena jinou léčbou.
Oční komplikace
Přípravek Berodual N musí být podáván se zvýšenou opatrností u pacientů s dispozicí ke vzniku glaukomu s úzkým úhlem.
Při vniknutí aerosolové formy ipratropium-bromidu samotného nebo v kombinaci s beta2-agonisty do očí jsou ojediněle zmiňovány oční komplikace (mydriáza, zvýšení nitroočního tlaku, glaukom s úzkým úhlem, bolestivost očí).
Bolestivost očí, oční diskomfort, rozostřené vidění, vizuální haló nebo duhové vidění spojené se zčervenáním očí, které je způsobeno městnáním ve spojivkách, a otok rohovky, mohou být příznaky akutního glaukomu s úzkým úhlem. Objeví-li se jakákoliv kombinace uvedených příznaků, je nutno zahájit léčbu kapkami s miotickým účinkem a vyhledat pomoc odborného lékaře.
Pacienti proto musí být poučeni o správné technice podávání přípravku Berodual N. Zvýšenou opatrnost je třeba věnovat tomu, aby přípravek nevnikl do očí.
Systémové účinky
V následujících případech může být Berodual N podáván pouze po pečlivém zvážení terapeutického prospěchu a rizika, zvláště jsou-li podávány vyšší dávky než doporučované: nedostatečně kontrolovaný diabetes mellitus, nedávný infarkt myokardu, těžké organické srdeční a cévní onemocnění, hypertyreóza, feochromocytom nebo podezření na obstrukci močového ústrojí (např. hyperplazie prostaty nebo obstrukce hrdla močového měchýře).
Kardiovaskulární účinky
Kardiovaskulární účinky se mohou vyskytovat u sympatomimetik, včetně přípravku Berodual N. Existují důkazy z post-marketingových dat a publikované literatury o vzácných výskytech ischemie myokardu spojené s P-agonisty. Pacienti se závažným srdečním onemocněním (např. ischemickou chorobou srdeční, arytmií nebo závažným srdečním selháním), kteří užívají Berodual N, musí být upozorněni, aby vyhledali lékařskou pomoc, pokud se u nich objeví bolest na hrudi nebo jiné symptomy zhoršení srdečního onemocnění. Musí se dávat pozor na hodnocení takových příznaků jako je dyspnoe a bolest na hrudi, protože mohou být respiračního nebo kardiálního původu.
Hypokalémie
Podávání beta2-agonistů může mít za následek závažnou hypokalemii (viz také bod 4.9).
Poruchy gastrointestinální motility
Pacienti s cystickou fibrózou jsou náchylnější k poruchám gastrointestinální motility.
Dyspnoe
Při akutní a rychle se zhoršující dyspnoe musí být pacienti poučeni, aby okamžitě vyhledali lékaře.
Dlouhodobé podávání:
-
■ U pacientů s bronchiálním astmatem a mírnou formou CHOPN je upřednostňováno příležitostné podávání (při projevu příznaků) oproti pravidelnému podávání přípravku;
-
■ U pacientů s bronchiálním astmatem a u pacientů s CHOPN, která reaguje na kortikosteroidní přípravky, je třeba zvážit současné podávání protizánětlivých přípravků (nebo zvýšení jejich dávek) k dosažení kontroly zánětu v dýchacích cestách a k zabránění zhoršení klinického stavu.
Pravidelné užívání zvyšujících se dávek beta2-agonistů, jako je Berodual N, může znamenat snížení kontroly nad průběhem onemocnění. Pokud se bronchiální obstrukce zhoršuje, je nevhodné a případně riskantní podávat po delší dobu vyšší než doporučené dávky přípravků obsahujících beta2-agonisty (např. Berodual N). V takovém případě je vhodné přehodnotit terapeutický plán pacienta a zejména zvážit, zda je protizánětlivá léčba inhalačními kortikosteroidními přípravky dostatečná. Takto je možno předejít případným stavům ohrožujícím život pacienta.
Další bronchodilatancia s účinkem beta2-agonistů mohou být současně s přípravkem Berodual N podávána jen pod lékařským dohledem (viz bod 4.5).
Varování před zneužitím jako doping
Použití přípravku Berodual N může vést, vzhledem k obsahu fenoterolu, k pozitivním nálezům, pokud je přípravek podán sportovcům např. pro zvýšení atletického výkonu (doping).
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Chronické podávání přípravku Berodual N spolu s jinými anticholinergiky nebylo studováno. Proto se nedoporučuje.
Ostatní beta-agonisté, anticholinergika a xantinové deriváty (např. theofylin) mohou bronchodilatační účinek přípravku Berodual N zvyšovat. Při současném podávání jiných beta-agonistů, systémově působících anticholinergik a xantinových derivátů (např. theofylinu) mohou být nežádoucí účinky zvýrazněny.
K potenciálně závažnému oslabení bronchodilatačního účinku může docházet při současném podávání beta-blokátorů.
Hypokalemie vyvolaná podáním beta2-agonistů může být zhoršena současným podáváním xantinových derivátů, kortikosteroidů a diuretik. Zvýšená opatrnost je nutná zejména u pacientů s těžkou obstrukcí dýchacích cest.
Hypokalemie může zvyšovat riziko srdečních arytmií u pacientů léčených digoxinem. Účinek hypokalemie na srdeční rytmus může být navíc zvýrazněn současnou hypoxií. V uvedených situacích je doporučeno pravidelné monitorování hladiny draslíku v séru.
Účinek beta2-agonistů může být zvýšen u pacientů léčených inhibitory monoaminooxidázy nebo tricyklickými antidepresivy, proto je v těchto případech nutná zvýšená opatrnost.
Inhalace celkových anestetik na bázi halogenovaných uhlovodíků, jako jsou halothan, trichlorethylen a enfluran, může zvýšit pravděpodobnost vzniku nežádoucích účinků beta-agonistů na kardiovaskulární systém.
4.6 Fertilita, těhotenství a kojení
Těhotenství
Výsledky neklinických hodnocení spolu se zkušenostmi získanými při léčbě pacientů neprokázaly škodlivé účinky fenoterolu nebo ipratropia v těhotenství. Je však doporučena obvyklá opatrnost při podávání přípravků v těhotenství, zejména v prvním trimestru.
Je třeba vzít v úvahu, že fenoterol inhibuje děložní kontrakce.
Použití beta2-agonistů na konci těhotenství nebo ve vysokých dávkách může vést ke vzniku nežádoucích účinků u novorozeného dítěte (třes, tachykardie, kolísání glykémie, hypokalémie).
Kojení
Neklinické studie ukázaly, že fenoterol-hydrobromid je vylučován do mateřského mléka. Není známo, je-li do mateřského mléka vylučováno také ipratropium. Avšak je nepravděpodobné, že by hladina ipratropia dosáhla u kojenců významné úrovně, zejména při inhalačním podávání. Jelikož ale řada jiných léků je do mateřského mléka vylučována, měl by být přípravek Berodual N podáván kojícím ženám s opatrností.
Fertilita
Klinické údaje vztahující se k plodnosti nejsou ke kombinaci těchto léčivých látek ani k jednotlivým látkám k dispozici. Neklinické studie prováděné s jednotlivými léčivými látkami ipratropium-bromid a fenoterol-hydrobromid neprokázaly nežádoucí účinky na plodnost (viz bod 5.3).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Nebyly provedeny žádné studie vlivu přípravku Berodual N na schopnost řídit dopravní prostředky a obsluhovat stroje. Nicméně pacienti musí být poučeni, že se mohou vyskytnout nežádoucí účinky jako závrať, třes, poruchy akomodace, mydriáza a rozostřené vidění během léčby přípravkem Berodual N. Proto je nutná při řízení auta nebo obsluze strojů opatrnost. Pokud se u pacientů vyskytne některý z výše uvedených nežádoucích účinků, měli by se vyvarovat potenciálně nebezpečných úkonů, jako je řízení vozidel nebo obsluha strojů.
4.8 Nežádoucí účinky
Mnohé z uvedených nežádoucích účinků patří k vlastnostem anticholinergik a beta-adrenergik. Tak jako při každé inhalační terapii, také u přípravku Berodual N se mohou objevit příznaky lokálního podráždění. Nežádoucí účinky byly zjištěny z údajů získaných v klinických studiích a během poregistračního sledování přípravku (farmakovigilance).
Mezi nejčastějšími nežádoucími účinky hlášenými v klinických studiích byly kašel, sucho v ústech, bolesti hlavy, třes, faryngitida, nauzea, závrať, dysfonie, tachykardie, palpitace, zvracení, zvýšení systolického tlaku krve, nervozita.
Nežádoucí účinky byly rozděleny podle výskytu za použití následující konvence: velmi časté (> 1/10); časté (> 1/100, < 1/10); méně časté (> 1/1000, < 1/100);
vzácné (> 1/10 000, < 1/1000); velmi vzácné (< 1/10 000); není známo (z dostupných údajů nelze určit).
Poruchy imunitního systému
Vzácné: Hypersenzitivita*, anafylaktické reakce*
Poruchy metabolismu a výživy
Vzácné: Hypokalemie*
Psychiatrické poruchy
Méně časté: Nervozita
Vzácné: Agitovanost, duševní poruchy
Poruchy nervového systému
Méně časté: Bolest hlavy, závratě, třes
Není známo: Hyperaktivita
Poruchy oka
Vzácné: Glaukom*, zvýšení nitroočního tlaku*, poruchy akomodace* (zaostřování), rozšířené
zornice*, rozmazané vidění*, bolest očí*, edém rohovky*, překrvení spojivek*, vizuální haló*
Srdeční poruchy
Méně časté: Tachykardie, zvýšený srdeční tep, palpitace
Vzácné: Arytmie, atriální fibrilace, supraventrikulární tachykardie*, ischemie myokardu*
Respirační, hrudní a mediastinální poruchy
Časté: Kašel
Méně časté: Faryngitida, dysfonie
Vzácné: Podráždění hrdla, bronchospazmus, faryngeální edém, laryngospazmus*, paradoxní
bronchospazmus*, sucho v krku*
Gastrointestinální poruchy
Méně časté: Sucho v ústech, pocit na zvracení, zvracení
Vzácné: Stomatitida, zánět jazyka, poruchy motility střev, průjem, zácpa*, otok úst*
Poruchy kůže a podkožní tkáně
Méně časté: Kožní reakce
Vzácné: Kožní vyrážka, kopřivka, svědění, angioedém*, hyperhidróza (nadměrné pocení)*
Poruchy svalové a kosterní soustavy a pojivové tkáně
Vzácné: Myalgie, svalové křeče, svalová slabost
Poruchy ledvin a močových cest
Vzácné: Retence moči
Vyšetření:
Méně časté: Zvýšení systolického krevního tlaku
Vzácné: Snížení diastolického krevního tlaku
*Nežádoucí účinek nebyl pozorován v klinických studiích. Odhad je založen na horní hranici jeho intervalu spolehlivosti 95 %, počítáno od celkového počtu léčených pacientů v souladu s obecnými zásadami EU SmPC (3 / 4968 = 0,00060, který se týká „vzácné“).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
webové stránky:
4.9 Předávkování
Příznaky
Lze očekávat, že příznaky předávkování budou primárně způsobeny složkou fenoterol.
Příznaky předávkování odpovídají příznakům nadměrné stimulace beta-agonisty, nejvýznamnější je tachykardie, palpitace, tremor, hypertenze, hypotenze, rozšíření tlakové amplitudy, anginózní bolesti, arytmie a návaly. Při aplikaci fenoterolu v dávkách vyšších než jsou dávky terapeutické, doporučené pro schválené indikace přípravku Berodual N, byla pozorována metabolická acidóza.
Po předávkování fenoterolem se může objevit hypokalémie. Je nutno monitorovat sérové hladiny draslíku.
Příznaky z předávkování ipratropium-bromidem (sucho v ústech, poruchy oční akomodace) jsou mírné, protože systémová dostupnost inhalovaného ipratropia je velmi nízká.
Terapie
Léčba přípravkem Berodual N by měla být přerušena a zváženo monitorování elektrolytů a acidobazické rovnováhy.
Podávání sedativ, trankvilizérů a v závažných případech intenzívní léčba. Vhodnými antidoty jsou beta-blokátory, přednostně beta1-selektivní. Nicméně je třeba vzít v úvahu možné zhoršení bronchiální obstrukce a u pacientů postižených astmatem či CHOPN musí být jejich dávka pečlivě upravena kvůli riziku vzniku těžkého bronchospazmu, který může být fatální.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: adrenergika v kombinaci s anticholinergiky na obstrukční poruchy dýchacích cest; ATC kód: R03AL01
Berodual N obsahuje dvě léčivé bronchodilatační látky – ipratropium-bromid s anticholinergním účinkem a fenoterol-hydrobromid s účinkem beta-agonistů.
Ipratropium-bromid je kvartérní amoniová sloučenina s anticholinergními (parasympatolytickými) vlastnostmi. Z neklinických studií lze soudit, že inhibuje vagem zprostředkované reflexy tím, že antagonizuje účinek acetylcholinu – transmiteru, který je uvolňován vagovým nervem. Anticholinergní látky zabraňují zvýšení nitrobuněčné koncentrace Ca2+ , ke kterému dochází po interakci acetylcholinu s muskarinovým receptorem hladké svaloviny bronchů. Uvolnění Ca2+ je zprostředkováno sekundárním přenašečem, který se skládá z IP3 (inositol-trifosfát) a DAG (diacylglycerol).
Bronchodilatace po inhalaci ipratropium-bromidu je primárně lokálním, místně specifickým a nikoliv systémovým účinkem.
Výsledky neklinických a klinických studií neprokázaly žádné škodlivé účinky ipratropium-bromidu na slizniční sekreci v dýchacích cestách, mukociliární clearance nebo výměnu plynů.
Fenoterol-hydrobromid je přímo působící beta-agonista, v terapeutických dávkách selektivně stimulující beta2-receptory. Při vyšší dávce stimuluje též beta1-receptory. Stimulace beta2-receptorů aktivuje adenylcyklázu přes stimulační protein GS. Zvýšení nitrobuněčné koncentrace cAMP aktivuje proteinkinázu A, která fosforyluje řadu cílových proteinů v buňkách hladké svaloviny. Následně pak dochází k fosforylaci myosinkinázy, inhibici fosfoinositidové hydrolýzy a otevření kalciem aktivovaných draslíkových kanálů s vysokou vodivostí.
Fenoterol-hydrobromid relaxuje bronchiální a vaskulární hladkou svalovinu a chrání ji proti bronchokonstrikčním podnětům jako je histamin, metacholin, studený vzduch a alergeny (časná odpověď). Po akutním podání přípravku je inhibováno uvolňování bronchokonstrikčních látek a mediátorů zánětu žírnými buňkami. Po aplikaci vyšších dávek fenoterolu (0,6 mg) bylo popsáno zvýšení mukociliární aktivity.
Vyšší plazmatické koncentrace, které jsou častěji dosahovány po perorálním nebo spíše nitrožilním podání, mohou inhibovat motilitu dělohy. Při vyšších dávkách byly rovněž popsány metabolické účinky jako lipolýza, glykogenolýza, hyperglykemie a hypokalemie, která je způsobena zvýšeným vychytáváním draslíkových iontů kosterními svaly. Účinek beta-agonistů na srdeční sval (zvýšená srdeční frekvence a kontraktilita) je způsoben účinkem fenoterolu na cévy, stimulací srdečních beta2-receptorů, a při vyšší než terapeutické dávce i stimulací beta1-receptorů. Jako u jiných beta-agonistů bylo hlášeno prodloužení intervalu QT (zvýšení hodnoty QTc). U fenoterolu inhalovaného prostřednictvím inhalátoru s odměřeným dávkováním se jednalo o jednotlivé případy, které byly pozorovány v dávkách vyšších než doporučených. Systémová expozice by však po podání nebulizátory (ampule s jednotlivou dávkou roztoku pro inhalaci) mohla být vyšší než u dávek doporučených k aplikaci inhalátorem. Klinická významnost nebyla stanovena. Třes patří mezi častější nežádoucí účinky beta-agonistů. Na rozdíl od účinků beta-agonistů na hladkou svalovinu bronchů se na účinky na kosterní svalovinu vyvíjí tolerance.
Současné podávání dvou léčivých látek v přípravku dilatuje bronchy působením na farmakologicky odlišná místa účinku. Obě léčivé látky se navzájem doplňují ve spazmolytickém účinku na bronchiální svalovinu a představují tak přípravek s rozsáhlým terapeutickým využitím při léčbě bronchopulmonálních onemocnění, provázených konstrikcí dýchacích cest. Komplementární účinek obou léčivých látek způsobuje, že k dosažení efektu postačuje malá koncentrace beta-agonisty, což usnadňuje individuální úpravu dávky a minimalizaci nežádoucích účinků.
Klinická účinnost a bezpečnost
U pacientů s astmatem a s CHOPN bylo zjištěno, že účinnost přípravku Berodual N odpovídá dvojnásobné dávce fenoterolu, podávaného bez ipratropium-bromidu, a to při lepší toleranci ve studiích, sledujících odpověď na kumulativní dávku. Ve studiích s průkazným počtem pacientů s astmatem a s CHOPN byla zjištěna vyšší účinnost přípravku Berodual N ve srovnání s účinky jednotlivých složek tohoto přípravku.
Při akutní bronchokonstrikci nastupuje účinek přípravku Berodual N krátce po podání, a je proto vhodným přípravkem k léčení akutních záchvatů bronchospazmu.
5.2 Farmakokinetické vlastnosti
Terapeutický účinek kombinace ipratropium-bromid s fenoterol-hydrobromidem je dán jeho lokálním působením v dýchacích cestách. Farmakodynamika bronchodilatace proto nemá vztah k farmakokinetice léčivých složek přípravku.
10 – 39 % dávky po inhalačním podání je obvykle uloženo v plicích, v závislosti na složení přípravku, inhalační technice a inhalačním zařízení, zatímco zbytek podané dávky zůstane v náustku, ústech a horní části dýchacích cest (orofaryngu). Stejná část dávky je uložena v dýchacích cestách po inhalaci odměřených dávek aerosolu s HFA náplní. Část dávky uložené v plicích dosáhne oběhu rychle (během několika minut). Množství účinné látky uložené v orofaryngu je pomalu polknuto a prochází zažívacím traktem. Proto je systémová expozice funkcí jak perorální, tak i plicní biologické dostupnosti.
Nejsou k dispozici důkazy, jež by ukazovaly rozdílnou farmakokinetiku léčivých látek přípravku při podávání obou složek jednotlivě nebo v kombinaci.
Fenoterol-hydrobromid
Polknutá část léčivé látky je metabolizována hlavně na sulfátové konjugáty. Absolutní biologická dostupnost po perorálním podání je nízká (přibližně 1,5 %).
Po nitrožilním podání se volný respektive konjugovaný fenoterol blíží k 15 % respektive 27 % podané dávky v moči získané za 24 hodin. Po inhalaci pomocí inhalátoru s odměrným dávkováním Berodual je přibližně 1 % inhalované dávky vyloučeno ve formě volného fenoterolu do moči v průběhu
24 hodin. Na základě těchto údajů je odhadována celková systémová biologická dostupnost inhalovaných dávek fenoterol-hydrobromidu na 7 %.
Kinetické parametry popisující osud fenoterolu byly vypočítány z koncentrací v plazmě po nitrožilním podání. Po nitrožilním podání lze koncentrace v plazmě v průběhu času popsat tříkompartmentovým modelem, podle něhož trvá terminální poločas přibližně 3 hodiny. V tomto tříkompartmentovém modelu je zdánlivý distribuční objem fenoterolu v rovnovážném stavu (Vdss) přibližně 189 litrů (~2,7 litru/kg).
Přibližně 40 % léčivé látky je vázáno na proteiny plazmy. V neklinických studiích s potkany se zjistilo, že fenoterol a jeho metabolity nepřestupují hematoencefalickou bariéru. Celková clearance fenoterolu je 1,8 l/min a clearance renální je 0,27 l/min.
V bilanční studii exkrece tvořilo kumulativní renální vylučování (za 2 dny) s lékem spojené radioaktivity (včetně mateřské sloučeniny a všech metabolitů) 65 % dávky po nitrožilním podání, celková radioaktivita vyloučená stolicí představovala 14,8 % dávky. Po perorálním podání tvořila celková radioaktivita vyloučená do moči přibližně 39 % dávky, celková radioaktivita vyloučená stolicí po 48 hodinách představovala 40,2 % dávky.
Ipratropium-bromid
Kumulativní renální exkrece ipratropia (jako mateřské sloučeniny) se po 24 hodinách blíží k 46 % intravenózně podané dávky, tvoří méně než 1 % perorálně podané dávky a přibližně 3–13 % dávky inhalované prostřednictvím inhalátoru s odměrným dávkováním Berodual. Na základě těchto údajů je celková systémová biologická dostupnost ipratropium-bromidu po perorálních dávkách odhadována na 2 %, po inhalovaných dávkách na 7–28 %. Pokud toto vezmeme v úvahu, spolykaná část dávky ipratropium-bromidu k systémové expozici významně nepřispívá.
Kinetické parametry popisující osud ipratropia byly vypočítány z koncentrací v plazmě po nitrožilním podání. Je pozorován rychlý bifázický pokles koncentrací v plazmě. Zdánlivý distribuční objem v rovnovážném stavu (Vdss) je přibližně 176 litrů (~2,4 litru/kg). Léčivá látka je minimálně (méně než 20 %) vázán na proteiny plazmy. V neklinických studiích s potkany a psy se zjistilo, že kvartérní amoniová sůl ipratropia nepřestupuje hematoencefalickou bariéru.
Poločas terminální eliminační fáze je přibližně 1,6 hodiny. Ipratropium má celkovou clearance
-
2.3 l/min a renální clearance 0,9 l/min. Po nitrožilním podání se přibližně 60 % dávky metabolizuje, pravděpodobně z větší části oxidací v játrech.
V bilanční studii exkrece tvořilo kumulativní renální vylučování (za 6 dní) s lékem spojené radioaktivity (včetně mateřské sloučeniny a všech metabolitů) 72,1 % dávky po nitrožilním podání,
-
9.3 % po perorálním podání a 3,2 % po inhalaci. Celková radioaktivita vyloučená stolicí byla 6,3 % po nitrožilní aplikaci, 88,5 % po perorálním podání a 69,4 % po inhalaci. Pokud jde o vylučování
5.3 Předklinické údaje vztahující se k bezpečnosti
Studie toxicity po podání jednotlivé dávky kombinace ipratropium-bromidu a fenoterol-bromidu v poměru 1/2,5 (ipratropium-bromid/fenoterol-bromid) u myší a potkanů po perorálním, nitrožilním a inhalačním podání zjistily nízkou úroveň akutní toxicity. Ve srovnání s individuálními komponentami byly hodnoty LD50 pro kombinaci určovány více komponentou ipratropium-bromid než fenoterol-hydrobromid, a to bez jakýchkoliv známek potenciace.
Studie toxicity s opakovaným podáváním kombinace ipratropium-bromidu a fenoterol-hydrobromidu byly provedeny u potkanů (perorální, inhalační) a psů (nitrožilní, inhalační) s délkou trvání až
13 týdnů. Byly pozorovány jen menší toxické účinky při koncentracích až několik setkrát vyšších, než jaké jsou doporučovány u člověka. Byly pozorovány jizvy v myokardu levé komory pouze u jediného zvířete ze skupiny s nejvyšší dávkou (84 ^g/kg/den) při čtyřtýdenní nitrožilní studii u psů. 13týdenní perorální studie u potkanů a 13týdenní inhalační studie u psů neprokázaly žádné toxikologické změny přesahující ty, které odpovídaly individuálním léčivým látkám.
Nedošlo k žádným známkám potenciace u kombinace ve srovnání s individuálními komponentami. Všechny pozorované nežádoucí účinky jsou u fenoterol-hydrobromidu a ipratropium-bromidu dobře známy.
Po inhalačním podání kombinace ipratropium-bromidu a fenoterol-hydrobromidu se u potkanů a králíků neobjevily žádné teratogenní účinky. Žádné teratogenní efekty nebyly pozorovány také po ipratropium-bromidu a po inhalačním podání fenoterol-hydrobromidu. Po perorálním podávání při dávkách > 25 mg/kg/den (u králíků) a > 38,5 mg/kg/ den (u myší) vedl fenoterol-hydrobromid ke zvýšení frekvence malformací.
Pozorované malformace jsou považovány za účinek celé třídy beta-agonistů. Fertilita nebyla narušena u potkanů v perorálních dávkách až do 90 mg/kg/den ipratropium-bromidu, a do 40 mg/kg/den fenoterol-hydrobromidu.
Studie genotoxicity pro kombinaci nebyly provedeny. In vitro a in vivo testy nezjistily mutagenní potenciál ani u fenoterol-hydrobromidu ani u ipratropium-bromidu.
Studie kancerogenity pro kombinaci nebyly provedeny. Nebyly prokázány žádné tumorigenní nebo kancerogenní účinky v dlouhodobých studiích u myší a potkanů s ipratropium-bromidem.
U fenoterol-hydrobromidu byly provedeny studie kancerogenity po perorálním (u myší 18 měsíců, u potkanů 24 měsíců) a inhalačním podání (u potkanů 24 měsíců). V perorálních dávkách
25 mg/kg/den byl pozorován u myší zvýšený výskyt děložních leiomyomů s proměnlivou mitotickou aktivitou a u potkanů mesovariální leiomyomy. Tyto nálezy jsou známé jako účinky, jejichž příčinou je místní působení beta-adrenergních přípravků na buňky hladké svaloviny dělohy myší a potkanů.
Při zvážení současné úrovně výzkumu nelze tyto výsledky aplikovat na člověka. Veškeré jiné zjištěné nádory byly považovány za běžné druhy nádorů, které se spontánně objevují u použitých kmenů zvířat a nevykazovaly biologicky významně zvýšený výskyt vyplývající z léčby fenoterol-hydrobromidem.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Norfluran, bezvodý ethanol, čištěná voda, kyselina citronová
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
3 roky
6.4 Zvláštní opatření pro uchovávání
Uchovávejte při teplotě do 25°C.
Přípravek je nutno chránit před přímým slunečním světlem, horkem a mrazem.
6.5 Druh obalu a velikost balení
Tlaková kovová nádobka s dávkovacím ventilem, vložená do rozprašovače z umělé hmoty, krabička. Velikost balení: 10 ml, 200 odměřených dávek.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Žádné zvláštní požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Boehringer Ingelheim International GmbH
Ingelheim am Rhein, Německo
8. REGISTRAČNÍ ČÍSLO
14/080/02-C
9. DATUM PRVNÍ REGISTRACE / PRODLOUŽENÍ REGISTRACE
3.4.2002 / 30.6.2010
Další informace o léčivu BERODUAL N
Jak
se BERODUAL N
podává: inhalační podání - roztok k inhalaci v tlakovém obalu
Výdej
léku: na lékařský předpis
Balení: Dávkovací ventil
Velikost
balení: 200DÁV
Držitel rozhodnutí o registraci daného léku v České republice:
Boehringer Ingelheim International GmbH, Ingelheim am Rhein
E-mail: infocz@boehringer-ingelheim.com
