Souhrnné informace o léku - AIRBUFO FORSPIRO
1. NÁZEV PŘÍPRAVKU
Airbufo Forspiro 160 mikrogramů/4,5 mikrogramů dávkovaný prášek k inhalaci
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna podaná dávka (inhalovaná dávka) obsahuje budesonidum 160 mikrogramů a formoteroli fumaras dihydricus 4,5 mikrogramů.
Jedna odměřená dávka (předem odměřená dávka obsažena v blistru) obsahuje budesonidum 194,7 mikrogramů a formoteroli fumaras dihydricus 6,1 mikrogramů.
Pomocná látka se známým účinkem
Monohydrát laktosy: 5,4 mg v jedné odměřené dávce a 4,4 mg v jedné podané dávce.
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Dávkovaný prášek k inhalaci.
Bílý až téměř bílý nebo světle žlutý prášek bez hrudek.
4. KLINICKÉ ÚDAJE4.1 Terapeutické indikace
Airbufo Forspiro je indikován u dospělých a dospívajících od 12 let k pravidelné léčbě pacientů s astmatem, u kterých je vhodné použití kombinované léčby (inhalační kortikosteroid a dlouhodobě působící p2-sympatomimetikum), tj.:
-
– pacienti, kteří nejsou adekvátně kontrolováni inhalačními kortikosteroidy a „podle potřeby“ podávanými krátkodobě působícími p2-sympatomimetiky.
-
– pacienti již dobře kontrolovaní kombinací inhalačního kortikosteroidu a dlouhodobě působícího p2-sympatomimetika.
Airbufo Forspiro je indikován u dospělých pacientů od 18 let k symptomatické léčbě pacientů s těžkou chronickou obstrukční plicní nemocí s usilovnou vitální kapacitou za jednu sekundu (FEV1) <70 % normální předpovědní hodnoty (po bronchodilataci) a s anamnézou exacerbace bez ohledu na pravidelnou bronchodilatační léčbu (viz též bod 4.4).
4.2 Dávkování a způsob podání
Cesta podání: inhalační podání.
Dávkování
Airbufo Forspiro není určen pro zahajovací léčbu astmatu. Požadovaná dávka každé složky přípravku Airbufo Forspiro je individuální a má být přizpůsobena závažnosti onemocnění. Toto je nutné mít na paměti v době, kdy se léčba kombinovaným přípravkem zahajuje, ale i v době, kdy dochází k nastavení udržovací dávky. Pokud léčba pacienta vyžaduje kombinaci dávek jinou než jsou tyto dostupné v kombinovaném inhalátoru, je třeba předepsat vhodné dávky p2-sympatomimetika a/nebo kortikosteroidu v jednotlivých inhalátorech.
Dávka přípravku má být titrována na nejnižší možnou dávku, při které je zachována účinná kontrola symptomů onemocnění. Lékař má pacienta pravidelně sledovat tak, aby dávka budesonide/formoterolu byla stále optimální. Pokud je astma dlouhodobě kontrolováno nejnižší doporučenou dávkou, lze v dalším kroku uvažovat o podávání samotného inhalačního kortikosteroidu.
V případě, že je vhodné titrovat dolů na nižší sílu, nebo předepsat vyšší sílu, než je dostupná pro přípravek Airbufo Forspiro, je třeba změnit přípravek Airbufo Forspiro za alternativní přípravek obsahující fixní kombinaci budesonidu a formoterol-fumarátu s nižší nebo vyšší dávkou inhalačního kortikosteroidu.
Airbufo Forspiro lze podávat podle dvou léčebných přístupů:
-
A. Udržovací léčba přípravkem Airbufo Forspiro: Airbufo Forspiro je podáván pravidelně jako udržovací léčba se zvláštním bronchodilatans s rychlým nástupem účinku jako úlevová léčba.
-
B. Udržovací a úlevová léčba přípravkem Airbufo Forspiro: Airbufo Forspiro je podáván pravidelně jako udržovací léčba a dle potřeby podle vývoje symptomů.
Pacienti mají být poučeni, aby měli úlevovou medikaci, tj. bronchodilatans s rychlým nástupem účinku vždy k dispozici.
Doporučené dávkování:
Dospělí (od 18 let): 1–2 inhalace dvakrát denně. U některých pacientů může být zapotřebí dávkování až maximálně 4 inhalace dvakrát denně.
Dospívající (12 až 17 let): Jedna až dvě inhalace dvakrát denně.
V klinické praxi, pokud je dosaženo kontroly symptomů astmatu při dávkování dvakrát denně, je při titraci dávky na nejnižší účinnou dávku možno uvažovat i o podávání přípravku Airbufo Forspiro jednou denně, pokud je předepisující lékař přesvědčen, že dlouhodobě působící bronchodilatans v kombinaci s inhalačním kortikosteroidem je žádoucí k udržení kontroly astmatu.
Zvýšená spotřeba krátkodobě působícího bronchodilatans ukazuje na zhoršení kontroly astmatu a má být doprovázena přehodnocením léčby.
Děti do 12 let: Vzhledem k tomu, že nejsou dostupné žádné údaje, nedoporučuje se podávat Airbufo Forspiro dětem mladším 12 let.
Pacienti používají denně udržovací dávku přípravku Airbufo Forspiro, a dále Airbufo Forspiro dle potřeby podle vývoje symptomů. Pacienti mají být poučeni, aby měli pro úlevové užití Airbufo Forspiro vždy k dispozici.
Udržovací a úlevová léčba přípravkem Airbufo Forspiro má být zvažována především u pacientů:
- s neadekvátní kontrolou astmatu, kteří často používají úlevovou léčbu.
- u kterých vyžadovala exacerbace astmatu v minulosti lékařský zásah.
Pacienti, kteří často užívají vyšší počet dávek přípravku Airbufo Forspiro dle potřeby, mají být pečlivě sledováni pro možnost rozvoje nežádoucích účinků závislých na dávce.
Doporučené dávkování:
Dospělí a dospívající (od 12 let): Doporučená udržovací dávka je 2 inhalace denně, tj. jedna inhalace ráno a jedna inhalace večer, nebo 2 inhalace ráno či večer. Pro některé pacienty může být vhodná udržovací dávka 2 inhalace dvakrát denně. Při zhoršení má pacient inhalovat další 1 dávku dle potřeby. Pokud symptomy přetrvávají i po několika minutách po podání, je třeba inhalovat další dávku. Nedoporučuje se inhalovat více než 6 dávek najednou.
Obvykle není potřeba inhalovat více než 8 dávek za den, ale po omezenou dobu lze připustit i 12 inhalací za den. Pacienti, kteří užívají více než 8 inhalací za den, mají být poučeni, že v tomto případě je nutné, aby vyhledali ošetřujícího lékaře. Lékař má zhodnotit stávající léčbu astmatu a znovu nastavit udržovací léčbu.
Děti (do 12 let): Udržovací a úlevová léčba přípravkem Airbufo Forspiro není doporučena pro děti.
Doporučené dávkování:
Dospělí: 2 inhalace dvakrát denně.
Zvláštní skupiny pacientů:
U starších pacientů není nutné upravovat doporučené dávkování. Nejsou dostupné klinické údaje o použití přípravku Airbufo Forspiro u pacientů s poruchou funkce jater nebo ledvin. Vzhledem k tomu, že jsou obě léčivé látky metabolizovány v játrech, lze očekávat zvýšenou orgánovou expozici u pacientů s těžkou cirhózou jater.
Způsob podání
Pacient má být poučen jak používat inhalátor Forspiro a správné používání má být pravidelně kontrolováno.
Inhalátor obsahuje 60 dávek práškového léčiva ve stočeném hliníkovém stripu. Má počítadlo dávek, které ukazuje kolik dávek ještě zbývá, počítáno směrem dolů od 60 k 0. Po dosažení posledních 10 dávek se čísla objeví na červeném pozadí.
Inhalátor není doplnitelný – po vyprázdnění má být zlikvidován a nahrazen novým.
Ochranný kryt
Postranní komůrka:
Hliníkový strip se zde ukládá k vyjmutí.
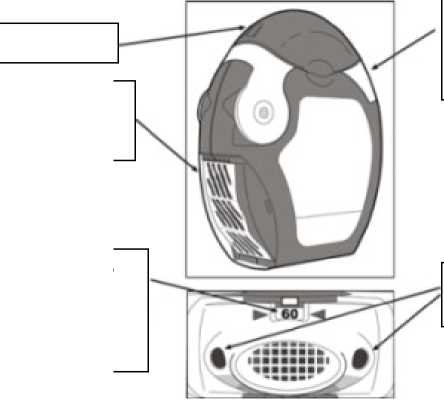
Bílá páčka: Používejte tuto páčku pouze, když j ste připraveni k inhalaci dávky.
Přívody vzduchu po obou stranách náustku
Počítadlo dávek: Po otevření ochranného krytu můžete zkontrolovat, kolik dávek ještě zbývá.
Před použitím inhalátoru
- Průhledná dvířka postranní komůrky se mají otevřít.
- Hliníkový strip se má vyjmout z postranní komůrky tak, že se opatrně odtrhne celá délka stripu o “zuby” postranní komůrky, jak je znázorněno níže. Strip se nemá tahat nebo škubat.
Poznámka: V průběhu používání inhalátoru se bude postranní komůrka postupně plnit použitým stripem. Hliníkové stripy s černými proužky neobsahují léčivo. Nakonec se v postranní komůrce objeví očíslované díly stripu. V postranní komůrce by nikdy neměly být více než 2 díly hliníkového stripu, jelikož by se inhalátor mohl zaseknout. Strip má být opatrně odtržen tak, jak je znázorněno výše, a bezpečně zlikvidován.
Použití inhalátoru
Inhalátor se má držet v rukou tak, jak je znázorněno na obrázcích.
1. Otevření
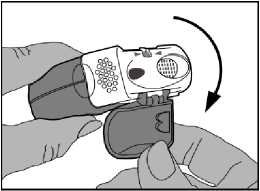
- Ochranný kryt se otevře směrem dolů, aby se odkryl náustek.
- Je třeba zkontrolovat počítadlo dávek, aby se zjistilo, kolik dávek ještě zbývá.
2. Příprava dávky
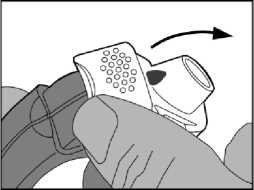
- Konec bílé páčky se pozvedne. Postranní komůrka má být uzavřena.
Poznámka: s bílou páčkou se má manipulovat pouze v případě, že se pacient chystá k inhalaci dávky léčiva. Pokud bude pacient s bílou páčkou zbytečně manipulovat, vyplýtvají se dávky bez užitku.
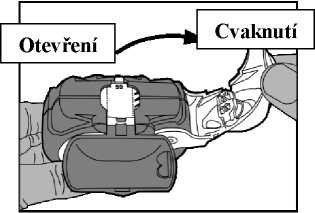
Otevření: Bílá páčka se má zcela uvolnit tak, jak nejvíce to půjde, až je slyšet cvaknutí. Tento pohyb umístí novou dávku do pozice s číslem na vrchu.
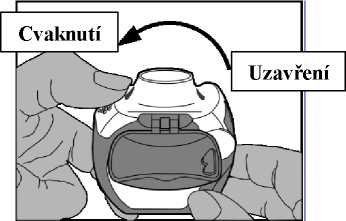
- Uzavření: Poté se má bílá páčka úplně uzavřít tak, že zaklapne zpět do původní pozice. Inhalátor je nyní připraven k okamžitému použití.
3. Inhalace dávky
- Pacient má vydechnout mimo inhalátor, jak nejvíce je to pro něj přijatelné. Nikdy se nemá dýchat přímo do inhalátoru, jelikož to může mít vliv na dávku.
- Inhalátor se má držet v horizontální poloze s ochranným krytem mířícím dolů.
- Rty mají být pevně sevřené kolem náustku.
- Pacient se má nadechnout plynule a hluboce přes inhalátor, ne nosem.
- Inhalátor má být vyjmut z úst a dech zadržen na 5 – 10 vteřin nebo na tak dlouho, jak je to možné bez způsobení nepohodlí.
- Poté má pacient pomalu vydechnout, ale ne do inhalátoru.
- Ochranný kryt se má zavřít přes náustek.
- Ústa se mají vypláchnout vodou, která se pak má vyplivnout. Toto může pomoci předejít vzniku plísňové infekce v ústech a chrapotu.
Čištění
- Vnější strana náustku se v případě potřeby má otřít čistým, suchým papírovým kapesníkem.
- Inhalátor se nemá rozebírat ani kvůli čištění, ani z jakýchkoli jiných důvodů!
- Součásti inhalátoru nesmí být čištěny vodou nebo vlhkými ubrousky, jelikož vlhkost může mít vliv na dávku!
- Do náustku nebo jakékoli jiné části inhalátoru nesmí nikdy být vkládány špendlíky nebo jiné ostré předměty, jelikož mohou poškodit inhalátor!
4.3 Kontraindikace
Hypersenzitivita na léčivé látky nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
4.4 Zvláštní upozornění a opatření pro použití
Při přerušování léčby se doporučuje vysazovat přípravek postupně a nikoliv náhle.
Pokud pacient pokládá léčbu za neúčinnou, nebo je nutné podávat vyšší než nejvyšší doporučené dávky přípravku Airbufo Forspiro, je nutné, aby vyhledal ošetřujícího lékaře (viz bod 4.2). Náhlé nebo progredující zhoršování astmatu nebo CHOPN potenciálně ohrožuje život pacienta a je nutný neodkladný lékařský zásah. V této situaci je nutné uvažovat o zintenzívnění léčby kortikosteroidy, např. nasazením perorálních kortikosteroidů nebo antibiotické, léčby, pokud je přítomna infekce.
Pacienti mají mít úlevovou medikaci vždy k dispozici, buďto Airbufo Forspiro (pro pacienty
s astmatem používající Airbufo Forspiro k udržovací i úlevové léčbě) nebo bronchodilatans s rychlým nástupem účinku (u všech pacientů, kteří používají Airbufo Forspiro pouze k udržovací léčbě).
Pacient má být poučen, aby používal předepsanou udržovací dávku přípravku Airbufo Forspiro i v období, kdy je bez příznaků základního onemocnění. Profylaktické použití přípravku Airbufo Forspiro, např. před fyzickou zátěží, nebylo studováno. Dávky úlevové medikace přípravkem Airbufo Forspiro jsou určeny ke kontrole symptomů astmatu a nikoliv k profylaxi, např. před fyzickou zátěží. K takovému použití je vhodné bronchodilatans s rychlým nástupem účinku.
Jakmile je dosaženo kontroly symptomů astmatu, je na místě uvažovat o postupném snižování dávky přípravku Airbufo Forspiro. Přitom je důležité pravidelně sledovat pacienta. Cílem je podávat nejmenší účinnou dávku přípravku Airbufo Forspiro (viz bod 4.2).
Léčba přípravkem Airbufo Forspiro nemá být zahajována v průběhu exacerbace a při výrazném či akutním zhoršení astmatu.
Závažné, s léčbou astmatu související nežádoucí účinky a exacerbace, se mohou objevit v průběhu léčby přípravkem Airbufo Forspiro. Pacienti mají být poučeni, že je nutné pokračovat v léčbě a současně vyhledat lékařskou pomoc v případě, že se příznaky astmatu nedaří kontrolovat či se dokonce zhoršují po zahájení léčby přípravkem Airbufo Forspiro.
Neexistují žádné údaje z klinických studií s budesonidem/formoterolem u pacientů s CHOPN s FEV1 > 50 % normální předpovědní hodnoty před bronchodilatací a s FEV1 < 70 % normální předpovědní hodnoty po bronchodilataci (viz bod 5.1).
Inhalační léčba obecně může někdy paradoxně vyvolat bronchospasmus s pískoty a dušností těsně po inhalaci. Pokud paradoxně dojde k projevům bronchospasmu, je třeba léčbu přípravkem Airbufo Forspiro ihned ukončit, pacienta vyšetřit a pokud je to nezbytné, zahájit alternativní léčbu. Paradoxní bronchospasmus odpovídá na bronchodilatans s rychlým nástupem účinku a má být léčen okamžitě (viz bod 4.8).
Inhalační kortikosteroidy mohou mít systémové účinky, zvláště pokud jsou podávány ve vysokých dávkách po dlouhou dobu. Tyto účinky jsou daleko méně pravděpodobné při inhalačním podávání ve srovnání s perorálním podáním kortikosteroidů. Systémové účinky se mohou projevit Cushingovým syndromem, Cushingoidními znaky, potlačením činnosti kůry nadledvin, zpomalením růstu u dětí a dospívajících, snížením kostní denzity, kataraktou a glaukomem. Méně často se může objevit celá řada účinků na psychiku nebo chování zahrnujících psychomotorickou hyperaktivitu, poruchy spánku, úzkost, depresi nebo agresi (zvláště u dětí) (viz bod 4.8).
Potenciální vliv na kostní denzitu má být brán v úvahu zvláště u pacientů s rizikovými faktory pro osteoporózu a současně léčených vysokými dávkami přípravku po delší období. Dlouhodobé studie s inhalačním budesonidem u dětí na průměrné denní dávce 400 mikrogramů (odměřená dávka) a u dospělých na průměrné denní dávce 800 mikrogramů (odměřená dávka) neprokázaly významný vliv na kostní denzitu. Nejsou dostupné informace pro budesonid/formoterol ve vyšších dávkách.
Pokud existuje podezření, že funkce nadledvin je po předchozí léčbě systémovými kortikosteroidy snížena, je třeba těmto pacientům věnovat zvýšenou pozornost při převodu na Airbufo Forspiro.
Přínosem inhalačního budesonidu má být minimální potřeba perorálních kortikosteroidů. Ovšem pacienti převádění z perorálních kortikosteroidů mohou mít sníženou rezervu kůry nadledvin, někdy přetrvávající značně dlouho. Obnovení stavu může trvat značně dlouho po ukončení léčby perorálními kortikosteroidy, a tedy pacienti závislí na perorálních steroidech mohou mít riziko snížené rezervy kůry nadledvin po značně dlouhou dobu. V takovém případě je třeba pravidelně kontrolovat funkci osy hypotalamus-hypofýza-nadledviny.
Dlouhodobá léčba vysokými dávkami inhalačních kortikosteroidů, zvláště dávkami vyššími než doporučenými, může vést ke klinicky významné supresi kůry nadledvin. V období zvýšeného stresu, jako je např. těžká infekce nebo elektivní chirurgický zákrok, je třeba uvažovat o přídavné dávce systémových kortikosteroidů. Náhlé snížení dávky steroidů může vyvolat akutní nedostatečnost nadledvin. Příznaky a projevy, které lze pozorovat v průběhu této krize jsou poněkud špatně vyjádřené, ale mohou zahrnovat anorexii, bolest břicha, ztrátu tělesné hmotnosti, únavu, bolest hlavy, nevolnost, zvracení, sníženou úroveň vědomí, křeče, hypotenzi a hypoglykemii.
Léčbu přídatnými systémovými steroidy nebo inhalovaným budesonidem je třeba ukončovat postupně a nikoliv náhle.
V průběhu převodu z perorální léčby na přípravek Airbufo Forspiro je obvykle aktivita systémových steroidů nižší, což se může projevit alergickými či artritickými příznaky, např. rinitidou, ekzémem a bolestí svalů a kloubů. V těchto případech je třeba zahájit specifickou léčbu. Obecně lze uvažovat o nedostatečném účinku glukokortikosteroidů v těch vzácných případech, kdy se objeví příznaky jako je únava, bolest hlavy, nevolnost a zvracení. V těchto případech je někdy nezbytné dočasně zvýšit dávku perorálních glukokortikosteroidů.
K minimalizaci rizika kandidové infekce nosohltanu (viz bod 4.8) se doporučuje vypláchnout ústa vodou po každé inhalaci udržovací dávky přípravku. Pokud se již soor nosohltanu objeví, je žádoucí provádět výplach vodou i po každé inhalaci dle potřeby.
Je třeba se vyhnout současné léčbě s itrakonazolem, ritonavirem a jinými účinnými inhibitory CYP3A4 (viz bod 4.5). Pokud to není možné, je nutné maximálně prodloužit časový interval mezi podáním interagujích léčiv. Současné podávání přípravku Airbufo Forspiro v udržovací a úlevové léčbě se nedoporučuje, pokud jsou podávány i účinné inibitory CYP3A4.
Očekává se, že souběžná léčba s inhibitory CYP3A, včetně léčivých přípravků obsahujících kobicistat, zvyšuje riziko systémových nežádoucích účinků. Je třeba se vyvarovat používání této kombinace, pokud přínos nepřeváží zvýšené riziko vzniku systémových nežádoucích účinků kortikosteroidů.
Airbufo Forspiro je třeba podávat opatrně pacientům s thyreotoxikózou, feochromocytomem, s onemocněním diabetes mellitus, neléčenou hypokalémií, hypertrofickou obstruktivní kardiomyopatií, idiopatickou subvalvulární stenózou aorty, těžkou hypertenzí, aneurysmatem a jinými závažnými kardiovaskulárními poruchami, např. ischemickou chorobou srdeční, tachyarytmií nebo dekompenzovaným srdečním selháním.
Opatrně je třeba přistupovat k léčbě pacientů s prodlouženým intervalem QTc. Podávání formoterolu může vyvolat prodloužení intervalu QTc.
Potřebu podávat inhalační kortikosteroidy, resp. velikost podávané dávky, je nutné pečlivě uvážit u pacientů s aktivní či němou formou plicní tuberkulózy, plísňovými a virovými infekcemi respiračního traktu.
Při vysokém dávkování p2-sympatomimetik se může vyvinout potenciálně závažná hypokalemie. Současná léčba p2-sympatomimetiky s léčivými přípravky, které mohou vyvolat hypokalemii nebo potencovat hypokalemický účinek, např. s xantinovými deriváty, steroidy a diuretiky, může zvětšit možný hypokalemický účinek p2-sympatomimetik. Zvláštní pozornost je třeba věnovat pacientům s nestabilním astmatem s variabilní spotřebou úlevové medikace, pacientům s akutním těžkým astmatickým záchvatem, neboť současná hypoxie může riziko hypokalemie zvýšit. Doporučuje se monitorovat kalémii v průběhu léčby těžkého akutního astmatického záchvatu.
Podobně jako u jiných p2-sympatomimetik je u diabetiků potřeba myslet na dodatečnou kontrolu glykemie.
Porucha zraku
U systémového i lokálního použití kortikosteroidů může být hlášena porucha zraku. Pokud se u pacienta objeví symptomy, jako je rozmazané vidění nebo jiné poruchy zraku, má být zváženo odeslání pacienta k očnímu lékaři za účelem vyšetření možných příčin, mezi které patří katarakta, glaukom nebo vzácná onemocnění, např. centrální serózní chorioretinopatie (CSCR), která byla hlášena po systémovém i lokálním použití kortikosteroidů.
Airbufo Forspiro obsahuje monohydrát laktosy (4,4 mg/inhalace). Toto množství obvykle nevede k projevům nesnášenlivosti při intoleranci laktosy. Laktosa obsahuje malá množství mléčných proteinů, které mohou vyvolat alergickou reakci.
Pediatrická populace
Doporučuje se, aby lékař pravidelně sledoval růst u dětí a dospívajících, kteří dlouhodobě používají inhalační kortikosteroidy. Pokud dojde ke zpomalení růstu, léčba má být přehodnocena s cílem možného snížení dávky inhalačního kortikosteroidu na nejnižší dávku, na které je dosaženo efektivní kontroly astmatu, pokud je to možné. Vždy je nutné vážit mezi přínosem kortikosteroidní léčby ke kontrole astmatu a možným zpomalením růstu. Kromě toho je třeba zvážit odeslání pacienta ke specialistovi na pediatrická respirační onemocnění.
Omezené údaje z dlouhodobých studií ukazují, že děti a dospívající léčení inhalačním budesonidem dorůstají v dospělosti do své normální výšky. Na počátku léčby je však patrné přechodné zpomalení růstu (přibližně o 1 cm). Toto se obvykle vyskytuje v průběhu prvního roku léčby.
Pneumonie u pacientů s CHOPN
U pacientů s CHOPN, kterým byly podávány inhalační glukokortikoidy, byl pozorován vyšší výskyt pneumonie, včetně pneumonie vyžadující hospitalizaci. Existují určité důkazy o tom, že zvýšené riziko pneumonie souvisí se zvyšováním dávky steroidu, avšak tuto závislost se nepodařilo definitivně prokázat ve všech studiích.
Neexistují jednoznačné klinické důkazy o rozdílech mezi léčivými přípravky ze skupiny inhalačních glukokortikoidů ohledně výše rizika pneumonie.
Lékaři mají sledovat možný vývoj pneumonie u pacientů s CHOPN, neboť klinické známky těchto infekcí se mohou překrývat se symptomy, které doprovázejí exacerbaci CHOPN.
Rizikovými faktory pro pneumonii u pacientů s CHOPN jsou současné kouření, vyšší věk, nízký index tělesné hmotnosti (BMI) a těžká CHOPN.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Farmakokinetické interakce
Účinné inhibitory CYP3A4 (např. ketokonazol, itrakonazol, vorikonazol, posakonazol, klarithromycin, telithromycin, nefazodon, kobicistat a HIV proteázové inhibitory) pravděpodobně značně zvyšují plazmatické koncentrace budesonidu a souběžné podávání má být vyloučeno. Pokud to není možné, má by být časový interval mezi podáním inhibitoru a budesonidem co možná nejdelší (viz bod 4.4). Současné podávání přípravku Airbufo Forspiro k udržovací a úlevové léčbě se nedoporučuje, pokud jsou podávány i účinné inibitory CYP3A4.
Účinný inhibitor CYP3A4 ketokonazol, 200 mg jednou denně, zvýšil plazmatické koncentrace souběžně podaného budesonidu (jednotlivá dávka 3 mg) v průměru 6násobně. Když byl ketokonazol podán 12 hodin po podání budesonidu, byla koncentrace zvýšena v průměru 3násobně, což ukazuje, že oddálení času podání může snížit zvýšené plazmatické koncentrace. Omezená data týkající se této interakce s vysokými dávkami inhalačního budesonidu ukazují, že může dojít ke značnému zvýšení plazmatických koncentrací (v průměru 4násobnému), pokud je itrakonazol, 200 mg jednou denně, podán souběžně s inhalačním budesonidem (jednotlivá dávka 1000 |ig).
Farmakodynamické interakce
Betablokátory mohou částečně nebo úplně antagonizovat účinek formoterolu. Přípravek Airbufo Forspiro nemá být podáván současně s betablokátory (včetně očních kapek), pokud k tomu nejsou vážné důvody.
Současná léčba chinidinem, disopyramidem, prokainamidem, fenothiaziny, antihistaminiky (terfenadin) a tricyklickými antidepresivy může prodlužovat interval QTc, a tak zvyšovat riziko komorových arytmií.
Levodopa, L-thyroxin, oxytocin a alkohol mohou mít negativní vliv na toleranci srdce k p2-sympatomimetikům.
Současná léčba inhibitory monoaminooxidázy včetně látek s podobnými vlastnostmi, jako je furazolidon a prokarbazin, může vyvolat hypertenzní reakce.
Existuje zvýšené riziko arytmií u pacientů, kterým je současně podávána anestezie halogenovanými uhlovodíky.
Současná léčba jinými beta-sympatomimetiky nebo anticholinergiky může mít potenciálně aditivní bronchodilatační účinek.
Hypokalemie může zvyšovat dispozici k arytmiím u pacientů, kteří jsou léčeni digitalisovými glykosidy.
Hypokalemie může být výsledkem podávání p2-sympatomimetik a může být potencována souběžným podáváním xantinových derivátů, kortikosteroidů a diuretik (viz bod 4.4).
U budesonidu a formoterolu nebyly pozorovány interakce s jinými léčivými přípravky používanými k léčbě astmatu.
Pediatrická populace
Interakční studie byly provedeny pouze u dospělých.
4.6 Fertilita, těhotenství a kojení
Těhotenství
Klinické údaje o použití budesonidu/formoterolu nebo současném použití formoterolu a budesonidu v průběhu těhotenství nejsou k dispozici. Data získaná ze studie zaměřené na embryofetální vývoj u potkanů ukazují, že u fixní kombinace není žádný nový dodatečný účinek.
Neexistují odpovídající údaje hodnotící podávání formoterolu u těhotných žen. Ve studiích na zvířatech měl formoterol při velmi vysokých systémových koncentracích nežádoucí účinky na reprodukci (viz bod 5.3).
Podávání inhalačního budesonidu u přibližně 2000 žen v průběhu těhotenství nevedlo ke zvýšení rizika teratogenity. Ve studiích na zvířatech vedlo podávání kortikosteroidů k vývoji malformací (viz bod 5.3). Při doporučeném dávkování je riziko u lidí nepravděpodobné.
Studie na zvířatech též prokázaly zvýšené riziko zpomalení intrauterinního růstu, kardiovaskulárních onemocnění v dospělosti, trvalých změn hustoty receptorů pro kortikosteroidy, životního cyklu neurotransmiterů a chování, pokud došlo k nadměrné expozici kortikosteroidům v průběhu prenatálního vývoje a to v dávkovém rozmezí nižším než dávky, které mají teratogenní účinky.
Airbufo Forspiro lze podat v průběhu těhotenství pouze tehdy, pokud očekávaný přínos převáží potenciální rizika. Podávána má být nejnižší účinná dávka budesonidu potřebná k udržování adekvátní kontroly astmatu.
Kojení
Budesonid je vylučován do mateřského mléka. V rozmezí terapeutických dávek se nepředpokládá, že by došlo k ovlivnění kojence. Není známo, zda formoterol přechází do mateřského mléka u lidí.
V mateřském mléce potkanů bylo zjištěno malé množství formoterolu. O podávání přípravku Airbufo Forspiro kojícím ženám lze uvažovat pouze tehdy, když očekávaný přínos pro matku převáží nad jakýmkoliv možným rizikem pro kojence.
Fertilita
Nejsou dostupné údaje o potenciálním vlivu budesonidu na fertilitu. Reprodukční studie u zvířat s formoterolem prokázaly při vysokých systémových expozicích poněkud sníženou fertilitu u samců potkanů (viz bod 5.3).
4.7 Účinky na schopnost řídit a obsluhovat stroje
Airbufo Forspiro nemá vliv, nebo má zanedbatelný vliv, na schopnost řídit motorová vozidla a na schopnost obsluhovat stroje.
4.8 Nežádoucí účinky
Jelikož Airbufo Forspiro obsahuje budesonid a formoterol, lze očekávat stejný typ a intenzitu nežádoucích účinků jako u odpovídajících monokomponentních přípravků. Výskyt nežádoucích účinků se nezvyšuje při podávání obou účinných látek ve fixní kombinaci. Nejčastější nežádoucí účinky mající vztah k obsaženým účinným látkám jsou předvídatelné farmakologické účinky p2-sympatomimetik, jako je třes a palpitace. Tyto nežádoucí účinky jsou mírné ve své intenzitě a obvykle odeznívají v průběhu několika dnů léčby.
Nežádoucí účinky, které se mohou objevit při podávání budesonidu nebo formoterolu jsou uvedeny dále, seřazeny podle tříd orgánových systémů a frekvence. Frekvence jsou definovány následovně: velmi časté (> 1/10); časté (> 1/100 až < 1/10); méně časté (> 1/1000 až < 1/100); vzácné (> 10 000 až < 1/1000); velmi vzácné (< 1/10 000); není známo (z dostupných údajů nelze určit).
Četnosti jsou odvozeny z dat z klinických studií. Incidence u placeba nebyla brána v potaz.
Tabulka 1
| Třídy orgánových systémů | F rekvence | Nežádoucí účinek |
| Infekce a infestace | Časté | Kandidové infekce nosohltanu Pneumonie (u pacientů s CHOPN) |
| Poruchy imunitního systému | Vzácné | Časné a pozdní hypersenzitivní reakce, např. exantém, kopřivka, pruritus, dermatitida, angioedém a anafylaktická reakce |
| Endokrinní poruchy | Velmi vzácné | Cushingův syndrome Suprese kůry nadledvin Zpomalení růstu Snížení kostní minerální denzity |
| Poruchy metabolismu a výživy | Vzácné | Hypokalemie |
| Velmi vzácné | Hyperglykemie | |
| Psychiatrické poruchy | Méně časté | Agrese Psychomotorická hyperaktivita Úzkost Poruchy spánku |
| Velmi vzácné | Deprese Změny chování (zejména u dětí) | |
| Poruchy nervového systému | Časté | Bolest hlavy Tremor |
| Méně časté | Závratě | |
| Velmi vzácné | Poruchy chuti | |
| Poruchy oka | Méně časté | Rozmazané vidění (viz také bod 4.4) |
| Velmi vzácné | Katarakta a glaukom | |
| Srdeční poruchy | Časté | Palpitace |
| Méně časté | Tachykardie | |
| Vzácné | Srdeční arytmie, např. síňové fibrilace, supraventrikulární tachakardie, extrasystoly | |
| Velmi vzácné | Angina pectoris Prodloužení intervalu QTc | |
| Cévní poruchy | Velmi vzácné | Kolísání krevního tlaku |
| Respirační, hrudní a mediastinální poruchy | Časté | Mírné podráždění v krku Kašel Chrapot |
| Vzácné | Bronchospasmus | |
| Gastrointestinální poruchy | Méně časté | Nauzea |
| Poruchy kůže a podkožní tkáně | Méně časté | Modřiny |
| Poruchy svalové a kosterní soustavy a pojivové tkáně | Méně časté | Svalové křeče |
Kandidové infekce v nosohltanu jsou důsledkem depozice léčivého přípravku. Pokud si bude pacient vyplachovat ústa po každé udržovací dávce, dojde k minimalizaci rizika. Kandidové infekce nosohltanu obvykle dobře reagují na lokální protiplísňovou léčbu bez nutnosti přerušit léčbu inhalačními kortikosteroidy. Pokud se objeví kandidová infekce nosohltanu, pacienti si mají vyplachovat ústa vodou i po každé úlevové inhalaci.
Podobně jako při jiné inhalační léčbě se může velmi vzácně objevit paradoxní bronchospasmus, který postihuje méně než 1 z 10 000 pacientů. Projevuje se okamžitým zesílením pískotů a dušností bezprostředně po inhalaci. Paradoxní bronchospasmus reaguje na podání rychle působících inhalačních bronchodilatans a má být léčen okamžitě. Léčba přípravkem Airflusan Forspiro má být okamžitě přerušena, pacient má být vyšetřen a má být zahájena alternativní léčba, pokud je to nezbytné (viz bod 4.4).
Může se objevit systémový účinek inhalačních kortikosteroidů, zvláště při podávání vysokých dávek po dlouhou dobu. Tyto nežádoucí účinky jsou daleko méně pravděpodobné než u perorálních kortikosteroidů. Možné systémové účinky zahrnují Cushingův syndrom, Cushingoidní projevy, supresi kůry nadledvin, zpomalení růstu u dětí a dospívajících, snížení minerální kostní denzity, kataraktu a glaukom. Může se objevit zvýšená citlivost k infekcím a snížená schopnost adaptace na stres. Tyto účinky jsou pravděpodobně závislé na dávce, době expozice, souběžné a dřívější expozici steroidům a individuální vnímavosti.
Léčba p2-sympatomimetiky může vést ke zvýšení plazmatických koncentrací insulinu, volných mastných kyselin, glycerolu a ketonů.
Pediatrická populace
Doporučuje se sledovat pravidelně výšku dětí, které jsou dlouhodobě léčeny inhalačními kortikosteroidy (viz bod 4.4).
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
Webové stránky:
4.9 Předávkování
Předávkování formoterolem vede pravděpodobně k projevům typickým pro p2-sympatomimetika: třes, bolest hlavy a palpitace. Může se též objevit tachykardie, hypokalemie, hyperglykemie, prodloužení intervalu QTc, arytmie, nauzea a zvracení. Indikována je podpůrná a symptomatická léčba. Dávka 90 mikrogramů formoterolu podaná v průběhu 3 hodin pacientům s akutní bronchokonstrikcí nevyvolala žádné nežádoucí účinky.
Akutní předávkování budesonidem, včetně vysokých dávek, nepředstavuje klinický problém. Při chronickém předávkování se mohou projevit systémové účinky kortikosteroidů, tj. hyperkorticismus a suprese kůry nadledvin.
Pokud je léčba přípravkem Airbufo Forspiro vysazována kvůli předávkování formoterolem, je třeba učinit vhodná opatření k suplementaci kortikosteroidní složky přípravku.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: léčiva k terapii onemocnění spojených s obstrukcí dýchacích cest: sympatomimetika, inhalační léčivé přípravky
ATC kód: R03AK07
Mechanismus účinku a farmakodynamické účinky
Tento léčivý přípravek obsahuje formoterol a budesonid, které mají různý mechanismus účinku a vykazují aditivní účinky, pokud jde o snížení četnosti exacerbací astmatu. Specifické vlastnosti budesonidu a formoterolu umožňují buďto použití k udržovací i úlevové léčbě, nebo k samotné udržovací léčbě astmatu.
Budesonid
Budesonid je glukokortikosteroid a pokud je podáván inhalační cestou má na dávce závislý protizánětlivý účinek v dýchacích cestách, který se projevuje snížením frekvence symptomů a exacerbací astmatu. Inhalovaný budesonid má méně závažných nežádoucích účinků ve srovnání se sytémovým podáním kortikosteroidů. Přesný mechanismus protizánětlivého účinku glukokortikosteroidů není znám.
Formoterol
Formoterol je selektivní p2-sympatomimetikum. Po inhalaci vyvolává rychlou a dlouhodobou relaxaci hladkého svalstva bronchů u pacientů s reverzibilní obstrukcí dýchacích cest. Bronchodilatační účinek je závislý na podané dávce, nastupuje 1–3 minuty po inhalaci. Přetrvává alespoň 12 hodin po podání jednotlivé dávky.
Klinická účinnost a bezpečnost
Klinická účinost budesonidu/formoterolu v udržovací léčbě
V klinických studiích u dospělých bylo prokázáno, že přidání formoterolu k budesonidu zlepšuje kontrolu příznaků astmatu i hodnoty plicních funkcí a snižuje počet exacerbací. Ve dvou 12týdenních studiích byl účinek budesonidu/formoterolu stejný jako účinek prosté kombinace budesonid a formoterol a lepší než účinek samotného budesonidu. Ve všech studijních ramenech byla používána krátkodobě působící p2-sympatomimetika dle potřeby. V průběhu sledování nedošlo ke snižování antiastmatického účinku.
Byly provedeny dvě 12týdenní klinické studie u dětí, ve kterých bylo celkem 265 dětí ve věku 6–11 let léčeno udržovací dávkou budesonidu/formoterolu (2 inhalace 80 mikrogramů/4,5 mikrogramů v jedné inhalaci dvakrát denně) a krátkodobě působící p2-sympatomimetikum podle potřeby. V obou studiích došlo ve srovnání s odpovídající dávkou samotného budesonidu ke zlepšení plicních funkcí a léčba byla dobře tolerována.
Klinická účinnost budesonide/formoterolu v udržovací a úlevové léčbě
V pěti dvojitě zaslepených klinických studiích v trvání 6 nebo 12 měsíců zaměřených na sledování účinnosti a bezpečnosti bylo zařazeno celkem 12076 pacientů (z toho bylo 4447 pacientů randomizováno k léčbě budesonid/formoterol v udržovací a úlevové léčbě). Zařazeni byli symptomatičtí pacienti bez ohledu na prováděnou léčbu inhalačními glukokortikosteroidy.
Podávání budesonidu/formoterolu v udržovací a úlevové léčbě vedlo ve všech pěti studiích ke statisticky i klinicky významnému poklesu počtu těžkých exacerbací. Toto srovnání zahrnovalo budesonid/formoterol ve vyšší udržovací dávce s terbutalinem jako úlevovou medikací (studie 735) a budesonid/formoterol ve stejné udržovací dávce buď s formoterolem nebo terbutalinem jako úlevovou medikací (studie 734) (Tabulka 2). Ve studii 735 byly plicní funkce, kontrola symptomů a použití úlevové medikace podobné ve všech sledovaných skupinách. Ve studii 734 byly symptomy a použití úlevové medikace méně časté a plicní funkce zlepšené ve srovnání s oběma komparátory. Hodnocení všech pěti studií prokázalo, že pacienti léčení kombinací budesonid/formoterol v udržovací a úlevové léčbě nepotřebovali žádnou úlevovou medikaci v průměru 57 % z celkového počtu dnů léčby. V průběhu sledování se neprokázal vývoj tolerance k prováděné léčbě.
Tabulka 2 Přehled těžkých exacerbací v klinických studiích
| Studie č. Trvání | Léčebné skupiny | n | Těžké exacerbacea | |
| Počet | Počet/ paciento-rok | |||
| Studie 735/ 6 měsíců | Budesonid/formoterol 160/4,5 gg 2× denně + dle potřeby | 1103 | 125 | 0,23b |
| Budesonid/formoterol 320/9 gg 2× denně + terbutalin 0,4 mg dle potřeby | 1099 | 173 | 0,32 | |
| Salmeterol/flutikason 2 × 25/125 gg 2× denně + terbutalin 0,4 mg dle potřeby | 1119 | 208 | 0,38 | |
| Studie 734/ 12 měsíců | Budesonid/formoterol 160/4,5 gg 2× denně + dle potřeby | 1107 | 194 | 0,19 b |
| Budesonid/formoterol 160/4,5 gg 2× denně + formoterol 4,5 gg dle potřeby | 1137 | 296 | 0,29 | |
| Budesonid/formoterol 160/4,5 2× denně + terbutalin 0,4 mg dle potřeby | 1138 | 377 | 0,37 | |
a Definováno jako hospitalizace/léčba na jednotce intenzivní péče či léčba perorálními steroidy. b Snížení frekvence exacerbací je statisticky významné (P-hodnota < 0,01) pro obě srovnání.
Srovnatelná účinnost a bezpečnost u dospívajících a dospělých byla prokázána v 6 dvojitě zaslepených studiích, včetně 5 studií zmíněných výše a v další studii s vyšší udržovací dávkou 160/4,5 mikrogramu, dvě inhalace dvakrát denně. Tato hodnocení byla provedena na celkem 14385 pacientech s astmatem, z toho bylo 1847 dospívajících. Počet dospívajících, kteří používali více než 8 inhalací alespoň jeden den v průběhu udržovací a úlevové léčby budesonidem/formoterolem byl omezený. Takové použití bylo málo časté.
V jiných 2 klinických studiích s pacienty, kteří vyhledali lékařskou péči v důsledku akutní exacerbace astmatu, mělo podání budesonid/formoterol za následek rychlou a účinnou bronchodilataci podobně jako podání salbutamolu či formoterolu.
Ve dvou 12měsíčních klinických studiích byl hodnocen vliv na plicní funkce a frekvenci exacerbací (exacerbace byla definována jako potřeba podávat perorálně steroid a/nebo antibiotikum a/nebo hospitalizace v důsledku exacerbace) u pacientů se středně těžkou až těžkou chronickou obstrukční plicní nemocí. V obou studiích bylo zařazovací kritérium FEV1 < 50 % normální předpovědní hodnoty před bronchodilatací. Střední hodnota FEV1 po bronchodilataci při vstupu do studií byla 42 % normální předpovědní hodnoty.
Průměrný počet exacerbací za rok (jak je definováno výše) při podávání budesonid/formoterol byl ve srovnání se samotným formoterolem nebo placebem významně nižší (průměrná frekvence exacerbací 1,4 vs. 1,8–1,9 ve skupině placebo/formoterol). Průměrný počet dnů na perorální léčbě steroidy v průběhu 12 měsíců byl mírně nižší ve skupině budesonid/formoterol (7–8 dnů/paciento-rok vs. 11–12 dnů, resp. 9–12 dnů ve skupině placebo, resp. formoterol). Pokud jde o změny plicních funkcí, např. FEV1, nebyla léčba kombinací budesonid/formoterol lepší než léčba samotným formoterolem.
5.2 Farmakokinetické vlastnosti
Absorpce
Fixní kombinace budesonid a formoterol a odpovídající monokomponentní přípravky jsou bioekvivalentní, pokud jde o systémovou dostupnost budesonidu a formoterolu. Nehledě na tuto skutečnost byla po podání fixní kombinace pozorována poněkud vyšší suprese kortisolu ve srovnání s monokomponentními přípravky. Rozdíl není považován za klinicky významný z hlediska bezpečnosti přípravku.
Není důkaz o tom, že by docházelo k farmakokinetické interakci mezi budesonidem a formoterolem.
Farmakokinetické ukazatele účinných složek byly srovnatelné po podání budesonidu a formoterolu jako monoprodukty a po podání fixní kombinace. U budesonidu ve fixní kombinaci byla zjištěna mírně vyšší hodnota plochy plazmatických koncentrací v závislosti na čase (AUC), rychlost absorpce a maximální plazmatická koncentrace. U formoterolu byla hodnota maximální plazmatické koncentrace podobná po podání ve fixní kombinaci. Inhalovaný budesonid se rychle absorbuje a maximální plazmatické koncentrace je dosaženo v průběhu 30 minut po inhalaci. Průměrná plicní depozice budesonidu po inhalaci z práškového inhalátoru byla ve studiích 32–44 % podané dávky. Biologická dostupnost je asi 49 % z podané dávky. U dětí ve věku 6–16 let je plicní depozice při podání stejné dávky ve stejném rozmezí jako u dospělých. Výsledné plazmatické koncentrace nebyly stanoveny.
Inhalovaný formoterol se rychle absorbuje a maximální plazmatické koncentrace je dosaženo v průběhu 10 minut po inhalaci. Průměrná plicní depozice formoterolu z práškového inhalátoru zjištěná v průběhu klinického hodnocení je 28 až 49 % podané dávky. Biologická dostupnost formoterolu je asi 61 % z podané dávky.
Distribuce a biotransformace
Vazba na plazmatické bílkoviny je asi 50 % pro formoterol a 90 % pro budesonid. Distribuční objem je asi 4 l/kg pro formoterol a 3 l/kg pro budesonid. Formoterol je inaktivován konjugací (aktivní O-demetylovaný a deformylovaný metabolit vytvářejí farmakologicky neúčinné konjugáty). Budesonid podléhá extenzivní biotransformaci (asi 90 %) prvním průchodem játry na metabolity s nízkou kortikosteroidní aktivitou. Kortikosteroidní aktivita hlavních metabolitů, 6-beta-hydroxy-budesonidu a 16-alfa-hydroxy-prednisolonu, je menší než 1 % aktivity budesonidu. Nic nenasvědčuje tomu, že by mezi budesonidem a formoterolem docházelo k metabolické nebo jiné interakci.
Eliminace
Převážná část podané dávky formoterolu je přeměňována v játrech a poté se eliminuje ledvinami. 8% až 13 % inhalované dávky formoterolu se vylučuje močí v nezměněné formě. Formoterol má vysokou hodnotu celkové clearance (asi 1,4 l/min) a terminální eliminační poločas průměrně 17 hodin.
Budesonid je vylučován ve formě metabolitů tvořených převážně enzymovým systémem CYP3A4. Metabolity budesonidu jsou vylučovány ledvinami jako takové nebo konjugované. V moči byla nalezena pouze nepatrná množství nezměněného budesonidu. Budesonid má vysokou hodnotu celkové clearance (asi 1,2 l/min) a biologický eliminační poločas po i.v. podání je v průměru 4 hodiny.
Není známa farmakokinetika formoterolu a budesonidu u pacientů s renální insuficiencí. U pacientů s hepatální insuficiencí může být zvýšena systémová expozice budesonidu i formoterolu.
Linearita/nelinearita
Systémová expozice budesonidu a formoterolu koreluje podle lineárního vztahu s podanou dávkou.
5.3 Předklinické údaje vztahující se k bezpečnosti
Výsledky experimentálních toxikologických studií u zvířat ukazují, že toxicita budesonidu, formoterolu nebo obou látek v kombinaci je výsledkem jejich zesíleného farmakologického účinku.
V reprodukčních studiích u zvířat byly v experimentu po podání kortikosteroidů jako je budesonid zjištěny malformace (rozštěp patra a malformace skeletu). Tyto experimentální výsledky u zvířat se však nezdají být relevantní pro člověka v doporučovaných dávkách. Reprodukční studie u zvířat s formoterolem odhalily poněkud sníženou plodnost u samců potkanů při vysoké systémové expozici a zvýšenou ztrátu březosti, sníženou schopnost přežívání v časném postnatálním stádiu a nižší porodní hmotnost při značně vyšší systémové expozici ve srovnání s klinickým použitím. Tyto experimentální výsledky u zvířat se však nezdají být relevantní pro člověka.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Monohydrát laktosy (obsahuje mléčné proteiny)
6.2 Inkompatibility
Neuplatňuje se.
6.3 Doba použitelnosti
2 roky.
6.4 Zvláštní opatření pro uchovávání
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
6.5 Druh obalu a obsah balení
Červeno-bílý umělohmotný inhalátor obsahující OPA/Al/PVC-Al blistr s 60 odměřenými dávkami inhalačního prášku.
Velikosti balení: 1, 2, 3, 4 nebo 6 inhalátorů, každý obsahující 60 dávek.
Na trhu nemusí být všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Veškerý nepoužitý léčivý přípravek nebo odpad musí být zlikvidován v souladu s místními požadavky.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Sandoz s.r.o., Na Pankráci 1724/129, 140 00 Praha 4 – Nusle, Česká republika
8. REGISTRAČNÍ ČÍSLO
14/152/17-C
9. DATUM PRVNÍ REGISTRACE/PRODLOUŽENÍ REGISTRACE
Datum první registrace: 20. 6. 2018
Další informace o léčivu AIRBUFO FORSPIRO
Jak
se AIRBUFO FORSPIRO
podává: inhalační podání - dávkovaný prášek k inhalaci
Výdej
léku: na lékařský předpis
Balení: Blistr
Velikost
balení: 6X60DÁV
Držitel rozhodnutí o registraci daného léku v České republice:
Sandoz s.r.o., Praha
E-mail: office.cz@sandoz.com
Telefon: 221 421 611
