Souhrnné informace o léku - 0,9% SODIUM CHLORIDE KABI
1. NÁZEV PŘÍPRAVKU
0,9% Sodium chloride Kabi
rozpouštědlo pro parenterální použití
2. KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Složení ve 100 ml:
| Elektrolyty | mmol/l | mEq/l | ||
| Natrii chloridum | 0,9 g | Na+ | 154 | 154 |
| Aqua pro injectione ad | 100 ml | Cl- | 154 | 154 |
Jeden ml roztoku obsahuje 9 mg natrii chloridum.
Osmolarita: 308 mOsmol/l
Úplný seznam pomocných látek viz bod 6.1.
3. LÉKOVÁ FORMA
Rozpouštědlo pro parenterální použití.
Čirý, bezbarvý roztok, bez nebo prakticky bez částic
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikace
Vehikulum nebo rozpouštědlo pro parenterální podání léčivých přípravků k intravenóznímu, intramuskulárnímu nebo subkutánnímu podání.
4.2 Dávkování a způsob podání
Dávkování
Použité množství před podáním je závislé na požadované koncentraci léku k rozpuštění.
Způsob podání
Intravenózní, intramuskulární nebo subkutánní podání.
4.3 Kontraindikace
Vzhledem k indikacím přípravku jsou kontraindikace závislé na rozpouštěném léku.
Obecně podávání toho přípravku je kontraindikováno v následujících situacích:
- Hypernatremie
- Hypertonie
- Srdeční insuficience
- Edematózní stavy u pacientů se srdečními, jaterními nebo renálními poruchami
- Závažná hypertenze
- Metabolická acidóza
4.4 Zvláštní upozornění a opatření pro použití
Jednou otevřené balení roztoku musí být okamžitě spotřebováno.
V případě subkutánního podání by se neměl přidávat žádný suplement, který by mohl změnit isotonii. Nepoužívejte roztok, pokud není čirý, anebo má sraženiny.
Před přidáním obsahu ampulky k léku musí být zkontrolována kompatibilita dané substance s roztokem chloridu sodného.
Novorozenci, donošení nebo nedonošení, mohou mít vysoké hladiny sodíku, vzhledem k nezralosti renální funkce. Proto novorozenci, donošení nebo nedonošení, mohou dostávat opakovaně injekce chloridu sodného pouze v případě, kdy hladiny sodíku byly určeny.
Chlorid sodný by měl být podáván s opatrností pacientům s hypertenzí, srdečním selháním, plicním nebo periferním edémem, renálním poškozením, preeklampsií, hyperaldosteronismem, cirhózou a jiným poškozením jater, hypervolemií, obstrukcí močového ústrojí, hypoproteinemií a při jiném onemocnění a léčbě (např. kortikosteroidy) spojenými s retencí sodíku.
4.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Interakce závisejí na léku, který má být rozpuštěn.
Chlorid sodný je inkompatibilní s uhličitanem lithným, jehož vylučování ledvinami je přímo úměrné hladinám sodíku v organizmu. Podávání chloridu sodného urychluje renální vylučování lithia a tím snižuje jeho terapeutickou účinnost.
Je nutné se vyvarovat přidání alkoholu k roztokům chloridu sodného.
4.6 Fertilita, těhotenství a kojení
Vzhledem k charakteru léčivého přípravku by se při doporučeném a kontrolovaném podávání neměl očekávat žádný účinek na těhotné nebo kojící ženy.
Údaje, které se objevily ve vědecké literatuře o četných těhotenstvích, ukazují, že infuze chloridu sodného během těhotenství nevyvolávají nežádoucí účinky s vlivem na zdraví plodu nebo novorozence. Není žádná evidence o škodlivosti podávání roztoku chloridu sodného 9 mg/ml během kojení pro novorozence. Až doposud nejsou žádné relevantní epidemiologické údaje k dispozici, týkající se těhotenství i kojení; proto se doporučuje, aby byl tento roztok používán s opatrností, pokud je podáván během těchto období.
4.7 Účinky na schopnost řídit a obsluhovat stroje
Není relevantní.
4.8 Nežádoucí účinky
Mohou být vyvolány celkové poruchy a reakce v místě aplikace.
Neadekvátní nebo nepřiměřené podání roztoku chloridu sodného 9 mg/ml může vyvolat hyperhydrataci, hypernatremii, hyperchloremii a příznaky jako je metabolická acidóza vzhledem ke snížení koncentrace bikarbonátu a tvorbě edému.
Při nadbytku chloridu sodného se může objevit nausea, zvracení a bolest hlavy.
Pokud se přípravek 0,9% Sodium chloride Kabi, rozpouštědlo pro parenterální použití, používá jako rozpouštědlo pro injekční přípravky, povaha přidaného přípravku určuje pravděpodobnost nežádoucích účinků, které se mohou objevit.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky po registraci léčivého přípravku je důležité. Umožňuje to pokračovat ve sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu:
Státní ústav pro kontrolu léčiv
Šrobárova 48
100 41 Praha 10
Webové stránky: http://
4.9 Předávkování
Vzhledem k povaze přípravku, je-li jeho podání správné a kontrolované, není riziko intoxikace.
Přesto však nadbytek chloridu sodného v jeho nejakutnější formě způsobuje dehydrataci vnitřních orgánů, nauzeu, zvracení, průjem, křeče v břiše, žízeň, sníženou tvorbu slin a slz, pocení, teplotu, hypotenzi, tachykardii, renální selhání, plicní edém, acidózu, respirační insuficienci, bolest hlavy, vertigo, podrážděnost, svalové spasmy, rigiditu, kóma a smrt.
Pediatrická populace
U dětí může kóma a křeče přetrvávat z důvodu dehydratace buněk. Může se objevit respirační krize s tachypnoe a zrudnutí nosu.
-
V případě nadměrného požití chloridu sodného se doporučuje v krátké době po požití vyvolat zvracení nebo provést výplach žaludku. Křeče se léčí intravenózním podáním diazepamu.
-
V případě závažného renálního poškození, jestliže pacient umírá nebo koncentrace sodíku v séru je vyšší než 200 mmol/l, je nutná léčba dialýzou.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Rozpouštědla a ředidla, včetně irigačních roztoků, ATC kód: V07AB
Chlorid sodný, hlavní sůl tvořící napětí v extracelulárních tekutinách, se používá k léčbě redukce extracelulárních objemů, v případě dehydratace a při nedostatku sodíku, to se může stát v případech masivní diurézy, gastroenteritidy nebo při redukci konsumace soli.
Sodík je základní a nenahraditelný hlavní kation v extracelulární tekutině a nejdůležitější osmotická komponenta při řízení volemie. Chloridový iont může substituovat bikarbonát, vždy přítomný jako oxid uhličitý v celulárním metabolizmu.
Přípravek 0,9% Sodium chloride Kabi, rozpouštědlo pro parenterální použití, má stejný osmotický tlak jako tělní tekutiny.
-
V případě mírné alkalózy, podání fyziologického roztoku způsobí obnovu ztraceného chloridového iontu, zatímco nadbytek bikarbonátu se vyloučí močí, s následným snížením a normalizací alkalické rezervy.
Isotonický roztok chloridu sodného je rovněž vhodným vehikulem pro podávání četných léků a elektrolytů.
5.2 Farmakokinetické vlastnosti
Absorpce
-
V důsledku intravenózního podání přípravku nedochází k absorpci.
5.3 Předklinické údaje vztahující se k bezpečnosti
Bezpečnost isotonických roztoků chloridu sodného je dostatečně uznávaná v oblasti léčby infuzními přípravky po celém světě, díky zkušenostem s používáním tohoto roztoku pro obnovení vodní a elektrolytové bilance.
6. FARMACEUTICKÉ ÚDAJE
6.1 Seznam pomocných látek
Kyselina chlorovodíková (k úpravě pH)
Hydroxid sodný (k úpravě pH)
Voda pro injekci
6.2 Inkompatibility
Před přidáním obsahu ampulky k léku musí být ověřena kompatibilita mezi přidanými přípravky.
Je inkompatibilní s hydrokortisonem, amfotericinem B, tetracykliny, cefalotinem, erytromycinem, laktobionátem a solemi lithia.
Je inkompatibilní s léčivými látkami, které nejsou rozpustné v roztoku chloridu sodného, neboť může dojít k vysrážení léčivé látky. Je inkompatibilní také s léky, pro jejichž stabilitu a rozpouštění je důležité příliš kyselé nebo alkalické prostředí.
6.3 Doba použitelnosti
2 roky
Doba použitelnosti po prvním otevření: spotřebovat okamžitě.
6.4 Zvláštní opatření pro uchovávání
Pro tento léčivý přípravek nejsou požadovány žádné zvláštní podmínky pro uchovávání.
6.5 Druh obalu a obsah balení
Ampulka z polyetylenu o nízké hustotě (LDPE)
Balení s 20 ampulkami obsahující 5 ml
Balení s 50 ampulkami obsahující 5 ml
Balení s 20 ampulkami obsahující 10 ml
Balení s 50 ampulkami obsahující 10 ml
Balení s 20 ampulkami obsahující 20 ml
Na trhu nemusí být k dispozici všechny velikosti balení.
6.6 Zvláštní opatření pro likvidaci přípravku a pro zacházení s ním
Není třeba sterilizovat ampulku před jejím otevřením.
Není třeba používat nástroje k řezání k otevření ampulky.
Jakmile se ampulka otevře, její horní část je perfektně uzpůsobena kónusu injekční stříkačky (Luer kónus), se kterým je nutné použít jehlu.
Instrukce pro zacházení s přípravkem
Ampulku odlomíte tak, že ji budete odtrhávat kroutivým pohybem od ostatních ampulek v balení, přičemž se nesmíte dotýkat hlavičky a krčku žádné z ampulek (1). Protřepejte ampulku jedním pohybem, jak je ukázáno níže, abyste setřepali tekutinu zachycenou ve víčku (2). Ampulku otevřete tak, že budete kroutit tělem a hlavičkou ampulky v protichůdných směrech do doby, dokud nedojde k odlomení krčku ampulky (3). Napojte ampulku na Luer injekční stříkačku nebo na Luer-lock injekční stříkačku, tak jak je ukázáno na obrázku (4)
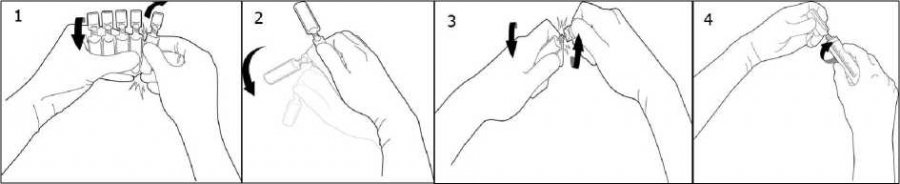
Pro natáhnutí roztoku není tedy potřeba použítí jehly. Natáhněte tekutinu.
Roztok neobsahuje žádné konzervační nebo baktericidní přísady, proto otevřené a nespotřebované ampulky musí být okamžitě znehodnoceny.
7. DRŽITEL ROZHODNUTÍ O REGISTRACI
Fresenius Kabi s.r.o., Na Strži 1702/65, Nusle, 140 00 Praha 4, Česká republika
8. REGISTRAČNÍ ČÍSLO(A)
76/689/09-C
9. DATUM PRVNÍ REGISTRACE / PRODLOUŽENÍ REGISTRACE
21. 10. 2009/21. 6. 2012
Další informace o léčivu 0,9% SODIUM CHLORIDE KABI
Jak
se 0,9% SODIUM CHLORIDE KABI
podává: subkutánní/intramuskulární/intravenózní podání - rozpouštědlo pro parenterální použití
Výdej
léku: na lékařský předpis
Balení: Ampulka
Velikost
balení: 20X5ML
Držitel rozhodnutí o registraci daného léku v České republice:
Fresenius Kabi s.r.o., Praha
E-mail: marina.svobodova@fresenius-kabi.com
Telefon: +420 225 270 583
